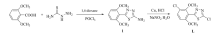
以2,6-二甲氧基苯甲酸为起始原料得到氨基噻二唑衍生物,通过Gattermann反应合成一种杂环芳族卤化物2-氯-5-(3-氯-2,6-二甲氧基苯基)-1,3,4-噻二唑(L),利用核磁共振波谱仪(NMR)和高分辨率质谱仪(HRMS)等测试手段确定了结构,并将其用作小分子荧光探针检测2,4,6-三硝基苯酚(TNP),系统地研究了其荧光特性,并且结合理论计算,探究了其可能的猝灭机制。 研究结果表明,探针L对TNP具有高选择性、高灵敏度、抗干扰能力强,在较宽的pH值范围内,仍然表现出良好的荧光性能。 具有较低的检测限(4.2×10-7 mol/L),可用于实际水样中TNP的检测。
The heterocyclic aromatic halide, 2-chloro-5-(3-chloro-2,6-dimethoxyphenyl)-1,3,4-thiadiazole (L), was synthesized by Gattermann reaction from the aminothiadiazole derivative. Its structure was characterized by nuclear magnetic resonance spectroscopy (NMR) and high resolution mass spectrometry (HRMS). Probe L was used as a small molecule fluorescent probe to detect 2,4,6-trinitrophenol (TNP), and its fluorescence characteristics were systematically studied. Furthermore, combined with theoretical calculations, the possible quenching mechanism was explored. The results showed that the probe L had high seletivity, high sensitivity and strong anti-interference ability to TNP, and exhibited good fluorescence performance in a wide pH range. It has lower detection limit (4.2×10-7 mol/L) and can be used for the detection of TNP in actual water samples.
2,4,6-三硝基苯酚(TNP),俗称苦味酸(PA),是一种常见的爆炸物,有剧毒[1]。 在水中具有较好的溶解性,暴露的TNP很容易污染土壤和地下水,在生物系统和环境中难以降解,对水生生物有很大的危害[2]。 《地表水环境质量标准》(GB3838-2002)指出集中式生活饮用水地表水源地中TNP的质量浓度不得超过0.5 mg/L。 因此,对TNP的检测愈发受到重视。 随着现代仪器的发展,荧光探针技术因其灵敏度高、专一性强、检测速度快等优势,渐渐地应用于各种水样检测[3,4,5,6]以及生物体内检测[7,8]。
近年来,已有很多关于识别TNP的探针的报道,如荧光共轭聚合物(cps)[9]、小分子荧光团[10,11]、金属有机骨架(MOFs)[12]以及聚集诱导的发光材料[13,14,15]等。 而有机小分子荧光探针因其具有合成简便、成本低、不需要预处理、溶解性好等特点,备受重视[16]。 例如,但是目前报道的检测TNP的有机小分子荧光探针多数存在着检测限过高的问题。 例如,2015年,Pandith等[17]报道了一种基于蒽羧酰胺的荧光探针,检测限为1 μmol/L;2018年,Ma等[18]报道了一种利用萘二甲酰亚胺作为荧光团的小分子荧光探针,其检测限为0.47 μmol/L,因此,研究开发高效灵敏、低检测限特异性检测TNP的有机小分子荧光探针仍然具有重要的意义[19]。
本文在前期工作基础上[20],基于Gattermann反应,采用一种简单的合成方法,获得一种杂环芳族卤化物2-氯-5-(3-氯-2,6-二甲氧基苯基)-1,3,4-噻二唑(L)(Scheme 1),并将其用作检测TNP的小分子荧光探针。 探针L具有灵敏度高、检测限低的特点,可以在较宽的pH值范围内使用。
2,6-二甲氧基苯甲酸(≥98%)购自阿拉丁试剂有限公司;二氧六环、盐酸、苯酚(Phe)购自天津市科密欧化学试剂有限公司,分析纯;硫代氨基脲购自中国医药(集团)上海化学试剂公司,分析纯;三氯氧磷(POCl3,≥98.5%)购自天津试剂厂;间二硝基苯(1,3-DNB)购自北京化工厂,分析纯;2,4-二硝基氯苯(2,4-DNT)购自新中化学厂股份有限公司,化学纯;对硝基苯甲醛(4-NBA)购自上海笛柏化学品技术有限公司,分析纯;邻硝基苯酚(2-NP)购自天津市化学试剂一厂,化学纯;间三羟基苯( m-Thb)购自北京工业学院制药厂,化学纯;对二硝基苯(1,4-DNB)和邻二硝基苯(1,2-DNB)购自北京化工厂,化学纯;硝基苯(NB)购自沈阳市新华化工厂,化学纯;实验用水为二次蒸馏水。
UV-240型紫外-可见分光光度计(UV-Vis,日本岛津公司);X-5型显微熔点测定仪(北京泰克仪器仪表有限公司);Burker Avance-500 MHz型核磁共振波谱仪(NMR,德国Burker公司);HITACHI F-7000型荧光光谱仪(日本日立公司);Q-TOF-6540型液相色谱高分辨飞行时间质谱(美国Agilent公司);使用 Gaussian 09程序通过密度泛函理论(DFT)计算相应化合物的能量。 使用6-31+G(d)基组在具有B3LYP功能的水中进行几何优化和频率计算。
1.2.1 2-氨基-5-(2,6-二甲氧基苯基)-1,3,4-噻二唑(1)的合成
参照文献[21]方法,取2,6-二甲氧基苯甲酸(5.46 g,30 mmol)、硫代氨基脲(2.73 g,30 mmol)和40 mL二氧六环于圆底烧瓶中,室温搅拌溶解,在0~5 ℃冰水浴条件下搅拌,同时向上述溶液中逐滴加入7 mL POCl3,加热回流0.5 h,冷却至室温,缓慢加入20 mL水,再回流4 h。 将反应液趁热倒入装有碎冰的烧杯中,用浓氨水调节pH值至8~9,抽滤,干燥,用乙酸乙酯热溶,趁热过滤得乳白色固体2.85 g。 产率:40.1%,mp 236~238 ℃;1H NMR(500 MHz,DMSO- d6), δ:7.40(t,1H, J=8.4 Hz),7.10(s,2H),6.74(d,2H, J=8.5 Hz),3.73(s,6H )。
1.2.2 2-氯-5-(3-氯-2,6-二甲氧基苯基)-1,3,4-噻二唑(L)的合成
向圆底烧瓶中加入化合物1(1.42 g,6 mmol),新制备的铜粉(0.38 g,6 mmol)和浓盐酸(25 mL)。 在0~5 ℃的条件下,搅拌15 min,然后将在冰水浴中冷却的NaNO2(2.06 g,30 mmol)溶液逐滴加到上述溶液中。 混合物在0~5 ℃下搅拌1.5 h后,加热至70 ℃。 5 h后停止反应,将混合物过滤。 所得粗产品用硅胶柱分离[ V(乙酸乙酯): V(石油醚)=1:15],得白色固体0.87 g。 产率50.1%,mp 120~122 ℃;1H NMR(500 MHz,DMSO- d6), δ:7.70(d,1H, J=9.1 Hz),7.08(d,1H, J=9.1 Hz),3.84(s,3H),3.75(s,3H );13C NMR(125 MHz,DMSO- d6), δ:162.0,157.3,155.5,154.8,133.7,119.6,114.3,109.6,62.3,57.1;HRMS(ESI-MS)计算值C10H8Cl2N2O2S [M+H]+:290.9762,实测值290.9758。
1.2.3 荧光光谱测量方法
在二甲基亚砜(DMSO)中配制1 mmol/L的探针L储备液和10 mmol/L的TNP 储备液。 一系列的硝基芳族化合物(NACs),2,4-DNT、1,4-DNB、4-NBA、1,3-DNB、1,2-DNB、2-NP、NB、Phe和 m-Thb储备液的浓度为10 mmol/L。 测试荧光光谱时,用移液枪移取30 μL的探针L储备液,加入含有3 mL DMSO-H2O溶液体系[ V(DMSO): V(H2O)=2:1]的荧光比色皿中,分别加入各种小分子等检测液,混合均匀,测定探针的荧光光谱。 用UV-Vis测出探针L的最大吸收波长为280 nm(图S5)。 狭缝宽度为5 nm/5 nm。
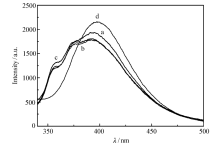
在 V(DMSO): V(H2O)=1:1、1:2、3:7和2:1这4种不同溶剂中对比探针L的荧光强度。 结果如图1所示,当溶剂为 V(DMSO): V(H2O)=2:1时,探针L显示出较好的荧光强度,选择此溶剂对探针L进行荧光测试。
如图2所示,当向10 μmol/L的探针溶液中加入少量的TNP时,初始荧光强度大幅度下降,因此系统地建立探针L在检测硝基芳族化合物(NACs)方面的适用性。
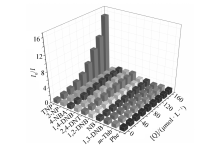 | 图2 探针L加入不同浓度(0~160 μmol/L)分析物荧光强度降低的3D图Fig.2 A 3D representation of the reduction in fluorescence intensity over a concentration range of analytes(from 0 to 160 μmol/L) for probe L |
将20 μmol/L至160 μmol/L的TNP溶液逐渐添加到10 μmol/L探针溶液中,TNP的荧光滴定如图3所示,其余化合物的荧光滴定见辅助材料图S6。 当向溶液中逐渐添加TNP时,探针L的荧光发射峰在397 nm处逐渐减弱,发生明显的荧光猝灭。
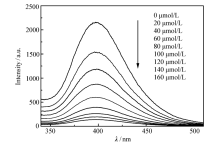 | 图3 加入TNP(0~160 μmol/L)后探针L(10 μmol/L)荧光强度( I397nm)Fig.3 Fluorescence intensity( I397nm) of probe L(10 μmol/L) upon addition of TNP(0~160 μmol/L) |
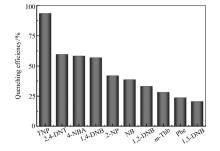
图4为在最大滴定浓度下各种硝基化合物的猝灭效率。 探针L对TNP有良好的选择性,猝灭效率达到93.5%。
通过Stern-Volmer方程(1)来评估探针的灵敏度,
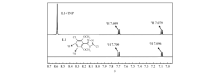
式中, Ksv为Stern-Volmer常数; I0和 I分别是添加分析物前后的荧光强度; c是分析物的浓度(mol/L)。 探针L的猝灭常数( Ksv)如表1所示,较大的 Ksv值显示出探针L检测TNP具有较高的灵敏度。 各个Stern-Volmer常数的确定表明荧光猝灭主要通过电子转移发生[22]。 此外,图5的核磁滴定可见,由于 π-π相互作用,当将TNP添加到探针L的DMSO- d6溶液中时,探针L中1H和2H质子的化学位移略有变化,表明TNP与探针L之间存在电子转移相互作用。
| 表1 探针L的Stern-Volmer常数( Ksv) Table 1 Different quenchers' Stern-Volmer constant( Ksv) of the probe L |
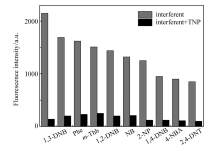
将TNP的最大滴定浓度分别添加到含有其它分析物的待测溶液中,结果如图6所示,观察到所有探针溶液的荧光强度均发生了变化。 因此,探针L在其它NACs存在的情况下仍然可以检测TNP,具有较强的抗干扰能力。
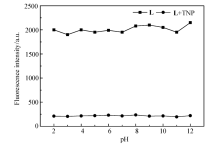
考察了探针L在不同pH值下的荧光强度的变化情况,如图7所示,在 V(DMSO): V(PBS)=2:1溶液中,pH值2~12的范围内,添加TNP前后探针的荧光强度均无明显变化,表明探针L在较宽的pH值范围内具有稳定的荧光特性。
通过式(2)来计算探针L的检测限(LOD):
式中, σ是测量空白样品的标准偏差, k是荧光强度与TNP浓度之间线性拟合直线的斜率。 结果如图8所示,在397 nm处探针的荧光强度对TNP浓度显示出良好的线性响应。 经计算,其检测限为0.42 μmol/L。
以硫酸奎宁(荧光量子产率 Фs=0.427)为参考[23],并根据式(3)计算加入TNP前后的荧光量子产率变化:
式中, Ф是荧光量子产率, A是激发波长对应的吸光度, F是校正发射曲线下的积分面积, n是所用溶剂的折射率。 下角标s和x分别代表标准和未知。 计算结果显示于表2中。 这些数据表明探针L在加入TNP之后变化明显,对TNP有较好的检测效果。
| 表2 探针L的荧光激发,发射波长和荧光量子产率 Table 2 Fluorescence excitation, emission wavelength and fluorescence quantum yield of probe L |
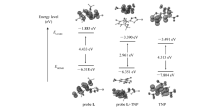
利用密度泛函理论(DFT)研究TNP对探针L的荧光猝灭过程如图9所示,探针L的最高能量占有轨道(HOMO)和最低能量空轨道(LUMO)的能量差为4.433 eV,明显看到,在TNP存在下,降低至2.961 eV。 探针L的LUMO能量为-1.885 eV,新形成的[探针L+TNP]复合物的能量为-3.390 eV,降低了1.505 eV,但是HOMO能量没有明显的变化。 因此,电子从探针L的HOMO轨道激发到LUMO轨道时,由于TNP的LUMO轨道能级介于探针L的HOMO和LUMO之间,此时被激发到探针L的LUMO轨道上的电子转移到了TNP的LUMO轨道上,而无法回到自身的HOMO轨道上,导致荧光猝灭。 由此可推测,TNP对探针L的荧光猝灭过程为光诱导电子转移(PET)机制。
分别测试了在实验室自来水、渤海海水和生活污水中探针L对TNP的响应。 根据荧光强度曲线(图10)和曲线方程(图8)计算出实际水样中的TNP浓度。 通过加标回收率方法对方法的可靠性进行了评估,列入表4中。 可以看出,回收率在96.6%~102.5%范围内,与计算结果相符,表明该探针可用于检测实际水样中的TNP,具有实际应用价值。
 | 图10 探针L(10 μmol/L)在海水,自来水和生活污水中的荧光响应Fig.10 Fluorescence response of probe L(10 μmol/L) to sea water(a), tap water(b) and domestic sewage(c) |
| 表3 通过加标回收法测定实际水样中的TNP浓度 Table 3 Determination of TNP concentration in actual water samples by spike recovery |
利用Gattermann反应合成了一种可用于检测TNP的有机小分子荧光探针2-氯-5-(3-氯-2,6-二甲氧基苯基)-1,3,4-噻二唑(L),探针L在 V(DMSO): V(H2O)=2:1溶液中显示较强的荧光性能,在加入TNP前后发射峰强度有非常明显的变化。 探针L可以定量识别检测TNP,具有高选择性和灵敏度,强抗干扰能力,在pH值2~12范围内,加入TNP前后荧光性能均比较稳定。 最低检测限达到4.2×10-7 mol/L,可以特异性识别TNP。 理论计算表明,其荧光猝灭过程为光诱导电子转移机制(PET)。 可用于实际水样中TNP的检测,具有一定的实际应用参考价值。
辅助材料(Supporting Information)[化合物1的核磁氢谱图,化合物L的核磁氢谱、核磁碳谱、高分辨质谱以及紫外吸收光谱图、其它硝基芳族化合物的荧光滴定图]可以免费从本刊网站(http://yyhx.ciac.jl.cn/)下载。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|