采用溶胶-凝胶法制备了 n(Cu): n(Zr)=1:1、1:2、1:4和1:8的Cu/ZrO2催化剂。 实验结果表明,当 n(Cu): n(Zr)=1:4时,催化剂表现出较高的CO2转化率(8.0%)和甲醇选择性(59.5%),为了增加CO2的转化率,提高甲醇选择性,在 n(Cu): n(Zr)=1:4的催化剂中添加质量分数1%的Pd,采用浸渍法制备了Pd-Cu/ZrO2催化剂。 在250 ℃、2 MPa、12000 mL/(g·h)和 V(H2): V(CO2)=3:1的反应条件下,CO2转化率和CH3OH收率相比Cu/ZrO2催化剂( n(Cu): n(Zr)=1:4)分别提高了40.0%和80.9%。 通过X射线衍射仪(XRD)、傅里叶变换红外光谱仪(FT-IR)、N2吸附-脱附(BET)、X射线光电子能谱仪(XPS)和程序升温还原化学吸附仪(H2-TPR)等仪器表征证明Pd的添加提高了催化剂的分散性和比表面积。 催化剂中Pd和Cu之间强相互作用,使Cu2 p轨道结合能向低处偏移,还原温度的降低,说明Pd-Cu/ZrO2催化剂还原能力增强,使得CO2加氢活性提高。
Cu/ZrO2 catalysts with the Cu/Zr molar ratio of 1:1, 1:2, 1:4 and 1:8 were prepared by the sol-gel method. When n(Cu): n(Zr)=1:4, a high CO2 conversion (8.0%) with methanol selectivity of 59.5% was achieved. To increase CO2 conversion and CH3OH selectivity, Pd-Cu/ZrO2 catalyst with the Cu/Zr molar ratio of 1:4 and 1 % mass fraction of Pd was synthesized by the impregnation method. The results showed that CO2 conversion and CH3OH yield over the Pd-Cu/ZrO2 catalyst were 40.0% and 80.9% higher than that over the Cu/ZrO2 catalyst at 250 ℃, 2 MPa, 12000 mL/(g·h) and V(H2): V(CO2)=3:1. Powder X-ray diffraction (XRD), Fourier transform infrared spectroscopy analysis (FT-IR), N2 adsorption-desorption (BET), X-ray photoelectron spectroscopy (XPS) and temperature-programmed reduction of H2(H2-TPR) results indicated that addition of Pd improved the dispersion and surface area of the catalyst. The strong interaction between Pd and Cu species leads to the shift of Cu2 p to low binding energies and decreases the catalyst reduction temperature, which exhibits high catalytic performance for hydrogenation of CO2.
随着化石能源的过度消耗,CO2排放量持续上升,由此引发的大气环境污染和“温室效应”问题日益严重。 捕集和利用CO2,可以减少大气中CO2含量[1,2]。 CO2加氢合成甲醇是化学固碳的一种有效途径,不仅可以有效减少空气中的CO2排放,而且可以制备出甲醇清洁能源[3]。 甲醇作为一种化工原料,广泛用于制备甲醛[4]、醋酸[5]等产品。 工业上,合成气采用传统的Cu/ZnO/Al2O3催化剂合成甲醇[6],该催化剂同样对CO2加氢合成甲醇体系适用。 然而,传统的Cu/ZnO/Al2O3催化剂由于逆水煤气反应(rWGS),生成的水加速了铜活性组分的烧结团聚[7],催化剂微晶的迁移和聚集也会导致催化剂烧结和团聚[8],促使催化剂表现出有限的催化活性和选择性。
目前,Cu基催化剂广泛用于CO2加氢合成甲醇体系,研究人员对催化剂的助剂及载体均有详细的研究[9,10,11,12],如ZnO、ZrO2、Al2O3和SiO2等。 采用ZrO2制备出的催化剂具有更高的催化剂活性[9]。 催化剂的制备方法[10]和组分含量的变化[11]均对其活性产生影响,利用溶胶-凝胶法制备出的催化剂具有较大的比表面积[12],表现出较好的催化性能。
本文采用溶胶-凝胶法制备了不同Cu、Zr物质的量比( n(Cu): n(Zr))的Cu/ZrO2催化剂,旨在探究不同 n(Cu): n(Zr)对Cu/ZrO2催化剂的分散性和催化活性的影响。 通过性能评价详细探究了不同催化剂在加氢反应中对CO2转化率和甲醇选择性的影响,以确定最佳 n(Cu): n(Zr)。 进一步选取最佳 n(Cu): n(Zr)的催化剂,采用浸渍法制备出Pd-Cu/ZrO2催化剂,本文通过X射线衍射(XRD)、比表面检测(BET)、傅里叶变换红外光谱(FT-IR)、X射线光电子能谱(XPS)和H2-TPR等方法对不同催化剂的结构和性质进行分析,探究贵金属Pd对催化剂的分散度、比表面积、孔径和表面羟基等性质的影响,还探究了Pd-Cu/ZrO2催化剂在不同反应温度下对CO2转化率和甲醇选择性的影响。
Cu(NO3)2·3H2O、Zr(NO3)4·5H2O、C6H8O7·H2O、丙酮和Pd(O2CCH3)2均为分析纯试剂,购自国药集团化学试剂有限公司。 去离子水购自上海阿拉丁生化科技股份有限公司。
X'Pert3 Powder型X射线衍射仪(XRD,荷兰PANalytical 公司),检测条件:衍射光源为Cu Kα( λ=0.154 nm);工作电压和电流分别为40 kV和100 mA;扫描速度为8°/min;步长为0.02°;扫描角度2 θ范围为20°~80°。 NEXUS-670型傅里叶变换红外光谱仪(FT-IR,美国NICOLET公司),采用高灵敏度MCT检测器。 Beckman Coulter SA3100型比表面检测仪(BET,美国贝克曼库尔特公司),样品做真空脱气200 ℃预处理,然后在液氮低温(77 K)下做N2吸附解吸检测。 ESCALAB 250Xi型X射线光电子能谱仪(XPS,美国热电公司)。 AutoChem II 2920型化学吸附仪分析(H2-TPR,美国麦克公司),测试温度范围为50~800 ℃。
采用溶胶-凝胶法制备( n(Cu): n(Zr)=1:1,1:2,1:4,1:8)的金属氧化物催化剂。 其操作步骤如下:按照不同摩尔比,称取一定质量的Cu(NO3)2·3H2O和Zr(NO3)4·5H2O溶于去离子水中,使其完全溶解,制成两种金属硝酸盐混合溶液。 在90 ℃的反应条件下,将预先配置好的柠檬酸溶液滴加到金属硝酸盐混合溶液中( n(Cu2++Zr4+): n(柠檬酸)=1:1.2)。 为确保金属离子与柠檬酸的完全螯合,继续在90 ℃的条件下搅拌至一种无定型粘稠状的深蓝色溶胶。 将深蓝色溶胶移至250 ℃的马弗炉处理2 h,溶胶起泡发生自燃,设置程序升温,以5 ℃/min的速度从室温升到350 ℃,焙烧4 h,冷却后研磨,压片成型(厚度425~850 μm),得到Cu/ZrO2催化剂样品。
采用浸渍法制备Pd质量分数1%的Pd-Cu/ZrO2催化剂。 其操作步骤如下:称取0.013 g的Pd(C2H3O2)2,溶于丙酮溶液中,超声30 min,将超声后溶液滴加到0.6 g Cu/ZrO2催化剂上,静置24 h,静置后的样品在110 ℃烘箱中干燥12 h,得到Pd-Cu/ZrO2催化剂前驱体,最后将前驱体放入马弗炉中焙烧,设置程序升温,以5 ℃/min的速度从室温升到350 ℃,焙烧4 h,冷却后研磨,压片成型(厚度425~850 μm),得到1%Pd-Cu/ZrO2催化剂样品。 将 n(Cu): n(Zr)=1:1、 n(Cu): n(Zr)=1:2、 n(Cu): n(Zr)=1:4、 n(Cu): n(Zr)=1:8和1%Pd-Cu/ZrO2分别记为Cu1Zr-O、Cu0.5Zr-O、Cu0.25Zr-O、Cu0.125Zr-O和1%Pd-Cu0.25Zr-O。
催化剂的活性测试在HP-WF51型固定床反应器上进行(不锈钢反应器内径10 mm),催化剂装填量为0.5 g催化剂(压片厚度425~850 μm)和0.5 g石英砂(压片厚度425~850 μm)混合。 反应在温度为250℃,压力为2 MPa,空速为12000 mL/(h·g),原料气组分比为 V(H2): V(CO2): V(N2)=69:23:8的条件下进行。 反应前催化剂预先在 V(H2): V(N2)=10:40混合气中还原,温度280 ℃,压力0.1 MPa下预处理4 h,结束后待温度降到250 ℃时,将气体切换到原料气组分开始反应。 反应的产物采用气相色谱仪进行分析,利用TCD检测器检测CO2和CO气体的浓度(填充柱采用TDX-01)。 利用FID检测器检测甲醇等烃类气体(毛细管柱采用Porapak Q),采用矫正面积归一法定量分析尾气中气体的浓度。
2.1.1 XRD分析
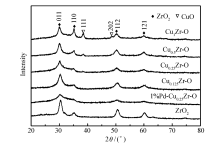
不同金属氧化物催化剂XRD图谱如图1所示。 由图1可见,2 θ为30.3°、35.3°、50.4°和60.2°的衍射峰归属于 t-ZrO2的(011)、(110)、(112)和(121)晶面(JCPDS-050-1089)[13]。 2 θ为38.7°和48.7°的衍射峰归属于CuO的(111),(202)晶面(JCPDS-89-2529)[14]。图1表明,CuO的添加明显减弱了ZrO2的衍射峰强度,说明CuO的添加减弱了ZrO2结晶度[15,16]。 随着Cu摩尔分数的逐渐降低,CuO的衍射峰强度逐渐减弱,Cu0.25Zr-O催化剂XRD图谱中观察到CuO微弱的衍射峰,而Cu0.125Zr-O催化剂XRD图谱中未能观察到CuO的衍射峰,表明CuO主要以无定形状态分散在ZrO2载体上[17]。 1%Pd-Cu0.25Zr-O催化剂的XRD图谱对比Cu0.25Zr-O催化剂,其衍射峰强度明显降低,峰形变宽,说明添加Pd提高了催化剂的分散性,从而表现出较好的催化活性[18]。 1%Pd-Cu0.25Zr-O催化剂XRD图谱中未观察到Pd的衍射峰,其原因可能是较低的负载量,Pd以无定形状态分散在催化剂表面[19]。
2.1.2 FT-IR分析
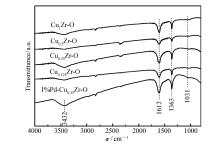
为进一步研究不同催化剂的结构,对焙烧后样品进行FT-IR分析。 如图2所示,所有焙烧后样品的3432和1612 cm-1处吸收峰归属于溶剂和物理表面吸附水中游离—OH的伸缩振动[20],1363 cm-1处出现一个较强的峰归属于Zr—OH基团的伸缩振动,1031 cm-1处出现一个较弱的峰归属于Cu—O伸缩振动[21]。 Cu0.25Zr-O和1%Pd-Cu0.25Zr-O催化剂对比其他3种催化剂,在3432和1612 cm-1峰形变大并且位于1363 cm-1处Zr—OH的吸收峰峰形强度较高,说明表面羟基较多。 已有研究[22]表明,催化剂表面羟基含量影响催化活性,催化剂表面羟基有利于反应过程中CO2表面吸附,从而表现出较好的催化活性,与1%Pd-Cu0.25Zr-O催化剂活性较好相对应。
2.1.3 BET分析
图3为焙烧后样品的N2吸附-脱附曲线和孔径分布图。 如图3A所示,根据IUPAC分类,所有催化剂均显示出具有H2型滞后环的IV型等温线,且脱附等温线位于吸附等温线之上,表明所有催化剂均具有介孔材料的特征[23]。 在图3B中,由焙烧后样品的孔径分布图(孔半径)可以看出所有样品均具有一个最可几孔径,分别为3.8、3.6、3.8、3.6和3.6 nm,说明样品的微孔和大孔较少[24]。 由表1可见,1%Pd/Cu0.25Zr-O催化剂具有最大比表面积,较大的表面积说明该催化剂具有更多的催化活性位点,表现出较好的催化活性。 此外,1%Pd-Cu0.25Zr-O催化剂还具有较大孔容的特征,催化剂较大的比表面积和较大的孔容,与1%Pd-Cu0.25Zr-O催化剂具有较高的活性相对应。
 | 图3 不同催化剂N2吸附-脱附曲线(A)和孔半径分布图(B)Fig.3 N2 adsorption-desorption(A) and pore size distribution(B) of different catalysts |
| 表1 不同催化剂的比表面积、孔容和平均孔径 Table 1 BET surface area, pore volume and average pore size of different catalysts |
2.2.1 XPS分析
采用XPS技术分析焙烧后催化剂表面元素的价态和电子结合能。图4A为Cu2 p轨道上XPS谱图,Cu2 p3/2的结合能在933.5 eV左右,Cu2 p1/2的结合能在954.0 eV左右,且940~945 eV出现一个卫星(shake-up)峰,表明所有焙烧后催化剂Cu元素主要以Cu2+存在[25]。 Cu0.25Zr-O对比Cu1Zr-O催化剂,Cu2 p3/2的结合能向低结合能处偏移0.3 eV,这表明催化剂的还原能力的增强[26],虽然Cu0.125Zr-O催化剂Cu2 p3/2的结合能最低,但由于其较低的负载量,导致活性位点较少,表现出较差的催化活性。图4B为Zr元素在3 d轨道上XPS谱图,Zr3 d5/2和Zr3 d3/2电子结合能分别在181.6和184.0 eV左右,表明Zr元素以Zr4+形式存在[27]。图4C为不同催化剂的O1 s的谱图,分峰拟合后的O1 s谱图由两个非对称的峰组成,证明了催化剂表面存在两种不同O类型。 其中,低结合能处归属于晶格氧,高结合能处归属于吸附氧[27]。图4D为1%Pd-Cu0.25Zr-O催化剂Pd3 d轨道上XPS谱图,Pd3 d5/2和Pd3 d3/2电子结合能分别在337.6和342.5 eV左右,表明Pd元素以Pd2+形式存在[28]。
2.2.2 H2-TPR分析
采用H2-TPR研究催化剂的还原能力。 从图5中可以看出,Cu0.25Zr-O和1%Pd-Cu0.25Zr-O催化剂均在200~350 ℃有一个宽的氢气消耗峰,该H2消耗峰不对称,由于ZrO2在该温度下不会被还原[12,29],此H2消耗峰归属于不同类型的CuO的还原。 对其进行分峰拟合,根据还原温度的高低,可分为 α、 β和 γ 3个峰: α峰归属于表面高分散状CuO的还原, β峰归属于嵌入到ZrO2晶格中CuO的还原峰, γ峰归属于块状CuO的还原[30]。 观察到Cu0.25Zr-O催化剂H2消耗峰由 α峰(226.4 ℃)、 β峰(256.8 ℃)和 γ峰(285.9 ℃)3个峰组成,而1%Pd-Cu0.25Zr-O催化剂的H2消耗峰只有 α峰(220.8 ℃)和 β峰(249.3 ℃),且 α峰和 β峰的还原温度对比Cu0.25Zr-O催化剂降低了5.6和7.5 ℃,1%Pd-Cu0.25Zr-O催化剂中并未拟合出 γ峰,说明Pd的添加增强了催化剂的还原能力,提高了Cu的分散性,表现出较好的催化活性[31]。
 | 图5 Cu0.25Zr-O和1%Pd-Cu0.25Zr-O催化剂的H2-TPR图Fig.5 H2-TPR profiles of Cu0.25Zr-O and 1%Pd-Cu0.25Zr-O catalysts |
2.2.3 催化活性测试
参考文献[32]对不同催化剂活性评价进行了测试,实验结果列于表2中。 对比不同 n(Cu): n(Zr)的Cu/ZrO2催化剂,Cu0.25Zr-O催化剂的CO2转化率、甲醇选择性和甲醇收率均达到最高。 而Cu0.125Zr-O催化剂,CO2的转化率和甲醇的选择性在所有催化剂中均最低,其原因可能是铜含量过低产生的活性位点较少,表现出较差的催化性能。 负载贵金属Pd后的Pd-Cu/ZrO2催化剂催化活性显著提高,1%Pd-Cu0.25Zr-O催化剂的CO2转化率和甲醇的收率在Cu0.25Zr-O催化剂的基础上提高了40%和80%。
| 表2 不同催化剂活性评价结果 Table 1 The catalytic tests of different catalysts |
图6为Cu0.25Zr-O和1%Pd-Cu0.25Zr-O催化剂在不同反应温度(210~270 ℃)下的活性评价结果。 从图6A可以看出,两种催化剂的CO2转化率均随着温度的升高而升高,CH3OH的选择性均随着温度的升高而降低。 在图6B中,当反应温度在250 ℃时,1%Pd-Cu0.25Zr-O甲醇的最高收率为8.5%。
通过溶胶-凝胶法制备出不同 n(Cu): n(Zr)的催化剂,当 n(Cu): n(Zr)=1:4时,形成一种高分散Cu/ZrO2催化剂;对高分散Cu/ZrO2催化剂的结构进行了表征,表征结果与其具有良好的催化性能相对应;通过浸渍法制备出1%Pd-Cu/ZrO2催化剂,Pd的添加大大提高了Cu/ZrO2催化剂的分散性和催化剂性能,对Cu0.25Zr-O和1%Pd-Cu0.25Zr-O催化剂在不同温度下活性测试,结果表明,在250 ℃、2 MPa、12000 mL/(g·h), V(H2): V(CO2)=3:1的反应条件下,1%Pd-Cu0.25Zr-O催化剂CH3OH最高收率达到8.5%,而Cu0.25Zr-O催化剂CH3OH最高收率仅达到4.7%,CH3OH的收率提高了80%。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|