设计合成了基于蒽-苯并咪唑鎓的受体分子1和2,通过荧光发射光谱研究了受体分子1和2对F-、Cl-、Br-、I-、AcO-、HSO4-、H2PO4-、NO3-、ClO4-等阴离子的识别性能。 研究发现,在受体分子1和2的乙腈溶液(5.0×10-6 mol/L)中加入10倍化学计量的H2PO4-时,受体分子1的荧光猝灭百分数为13%,受体分子2的荧光猝灭百分数高达94%,表明受体分子2在构型上与H2PO4-更匹配,可作为H2PO4-的荧光关闭型(turn-off)探针。 受体分子2与H2PO4-的结合比为1:1,结合常数为(3.70±0.16)×104 L/mol,检出限为3.77×10-6 mol/L。
Two novel anthracene-benzimidazolium based receptors 1 and 2 were synthesized. The anion (F-, Cl-, Br-, I-, AcO-, HSO4-, H2PO4-, ClO4-,NO3-) binding properties of receptors 1 and 2 were evaluated in acetonitrile by fluorescence spectroscopy. The receptors 1 and 2 display fluorescent quenching effect with H2PO4-, the quench percentage for receptor 1 is 13%,and for receptor 2 is as much as 94%. The results indicate that receptor 2 is more closely matched to H2PO4- in configuration, and receptor 2 can behave as a “turn-off” fluorescence sensor for H2PO4-. Job-plot shows that receptor 2 and H2PO4- form a 1:1 complex, the binding constant is (3.70±0.16)×104 L/mol, and the detection limit is 3.77×10-6 mol/L.
近来年,阴离子的识别和检测受到了广泛的关注[1,2,3,4]。 磷酸根阴离子是生命体系中重要的组成物质,参与DNA构建、能量存储和信息转录等过程,其中,磷酸氢根和磷酸二氢根(H2PO4-)是体内重要的酸碱平衡缓冲对,因此,此类物质的识别和检测受到了广泛的关注[5,6,7,8]。 目前,已报道的可用于识别H2PO4-的荧光探针主要有:荧光开启型(“Turn-on” fluorescence)[9,10]、荧光关闭型(“Turn-off” fluorescence)[11,12]以及比率型荧光探针(Ratiometric fluorescence)[13],其识别位点主要为酰胺[14,15,16]、亚胺[17]、腙[18]、羟基黄酮[19]、羟基[20]、铽-聚氨酯泡沫材料(Tb-PUFs)[21]、硫脲[22]等基团。 咪唑鎓中2位H作为识别位点,可与阴离子形成特殊的C—H••••X氢键,而由于咪唑环的共轭性,这种氢键作用可以被更好地理解为(C—H)+••••X-作用[23]。 由于存在这种离子型氢键,咪唑鎓作为识别位点已引起人们的广泛兴趣。 Liu等[24]合成的以咪唑鎓为识别位点的化合物对F-具有专属选择性识别性能。 因此,本文用简单的方法设计合成了两种苯并咪唑鎓受体分子1和2(Scheme 1),以苯并咪唑环上的C(2)—H作为阴离子结合位点,对阴离子的识别。
苯并咪唑、1-溴戊烷、多聚甲醛、氢化钠、蒽、9-蒽甲醇、氯化亚砜、十六烷基三甲基溴化铵、氢溴酸、 N, N-二甲基甲酰胺、二氯甲烷、乙酸乙酯、甲苯和无水乙醚购自阿拉丁试剂公司;六氟磷酸铵、乙腈和阴离子(F-、Cl-、Br-、I-、AcO-、HSO4-、H2PO4-、ClO4-、NO3-)的四丁基铵盐购自国药集团化学试剂有限公司,以上均为分析纯试剂;光谱测试溶剂使用前均经4A分子筛干燥;阴离子的四丁基铵盐使用前在60 ℃真空干燥。
Hitachi F-4600型荧光光谱仪(日本日立公司);Bruker400 MHz型核磁共振波谱仪(NMR,德国布鲁克公司);LCMS-8030型液相色谱质谱联用仪(日本岛津公司);Vario EL Cube型元素分析仪(德国元素分析系统有限公司)。
1-戊基苯并咪唑 N2气保护下,在配有回流冷凝管和搅拌器的100 mL两口烧瓶中加入氢化钠(60%在矿物油中,0.60 g,15 mmol),0 ℃下,滴入溶于30 mL N, N-二甲基甲酰胺的苯并咪唑(1.42 g,12 mmol),搅拌至无气泡产生,缓慢滴入1-溴正戊烷(1.51 g,10 mmol),室温下反应24 h。 反应结束后加入30 mL去离子水,二氯甲烷萃取(50 mL×3),有机相用饱和碳酸钠水溶液洗涤,水洗,无水硫酸钠干燥,旋蒸,得白色膏状固体1-戊基苯并咪唑1.52 g,收率81%。 9-(氯甲基)蒽的合成参考文献[25]。 9,10-二(溴甲基)蒽的合成参考文献[26]。
受体分子1 N2气保护下,在配有回流冷凝管和搅拌器的100 mL两口烧瓶中加入9-(氯甲基)蒽0.68 g(3.0 mmol)和甲苯30 mL,加热至110 ℃,缓慢滴加溶于20 mL甲苯的1-戊基苯并咪唑0.66 g(3.5 mmol),约5 h滴完,加热回流反应72 h。 反应结束后,冷却至室温,过滤,无水乙醚洗涤,真空干燥。 将所得固体0.83 g(2 mmol)溶于30 mL去离子水中,加入六氟磷酸铵0.49 g(3 mmol),室温搅拌5 h。 反应结束后,过滤,水洗3次,真空干燥,得黄色固体0.76 g,即受体分子1,收率72%。1H NMR(DMSO- d6,400 MHz), δ:0.71(t,3H, J=7.2 Hz,CH3),0.961.04(m,2H,CH2),1.091.16(m,2H,CH2),1.641.71(m,2H,CH2),4.29(t,2H, J=7.0 Hz,CH2),6.74(s,2H,CH2),7.717.75(m,2H,ArH),7.777.87(m,4H,ArH),8.12(d,1H, J=8.2 Hz,ArH),8.39(d,1H, J=8.2 Hz,ArH),8.46(d,2H, J=8.8 Hz,ArH),8.63(d,2H, J=8.8 Hz,ArH),8.95(s,1H,BimC2-H);13C NMR(100 MHz,DMSO- d6), δ:14.16,21.82,28.06,28.72,43.81,47.02,114.28,114.88,122.83,124.70,125.66,127.26,127.47,128.21,128.65,128.69,131.70,131.74,131.98,132.30,141.62;元素分析:C27H27F6N2P,实测值(计算值)/%:C 61.85(61.83),H 5.19(5.22),N 5.34(5.35);ESI-MS, m/z:[1-P
受体分子2 N2气保护下,在配有回流冷凝管和搅拌器的100 mL两口烧瓶中加入9,10-二(溴甲基)蒽0.73 g(2.0 mmol)和甲苯40 mL,加热至110 ℃,缓慢滴加溶于30 mL甲苯的1-戊基苯并咪唑0.79 g(4.2 mmol),约5 h滴完,加热回流反应72 h。 反应结束后,冷却至室温,过滤,用少量无水乙醚洗涤,真空干燥。 将所得固体0.96 g(1.3 mmol)溶于30 mL去离子水中,加入六氟磷酸铵0.42 g(2.6 mmol),室温搅拌6 h。 反应结束后,过滤,水洗3次,真空干燥,得淡黄色固体0.68 g,即受体分子2,收率60%。1H NMR(DMSO- d6,400 MHz), δ:0.72(t,6H, J=6.9 Hz,2×CH3),1.031.08(m,4H,2×CH2),1.131.16(m,4H,2×CH2),1.691.74(m,4H,2×CH2),4.18(t,4H, J=7.5 Hz,2×CH2),6.84(s,4H,2×CH2),7.737.80(m,8H,ArH),8.13(d,2H, J=7.8 Hz,ArH),8.34(d,2H, J=7.8 Hz,ArH),8.528.58(m,4H,ArH),9.14(s,2H,2×BimC2-H);13C NMR(100 MHz,DMSO- d6), δ:14.1,21.8,28.1,28.7,44.1,47.1,114.4,114.9,125.1,126.4,127.3,127.5,128.2,131.5,131.7,132.3,141.7;元素分析:C40H44F12N4P2,实测值(计算值)/%:C 55.18(55.25),H 5.09(5.11),N 6.43(6.48);ESI-MS, m/z:[2-P
在受体分子1和2(5.0 × 10-6 mol/L)的乙腈溶液中,采用累计进样法,逐次加入5.0×10-4 mol/L阴离子(F-、Cl-、Br-、I-、AcO-、HSO4-、H2P、ClO4-、NO3-)的四丁基铵盐的乙腈溶液,搅拌2 min,待平衡后利用荧光光谱仪测定其荧光发射光谱。
利用Job曲线法[27]测定受体分子与阴离子的配位比,使受体分子和阴离子的总浓度保持恒定(5×10-6 mol/L),顺序改变受体分子与阴离子的摩尔分数, x(G)=0、0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1.0,测试其荧光发射光谱。 以复合物的浓度 c(HG)对阴离子的摩尔分数 x(G)作图,曲线最大值那一点的 x(G)值即是受体分子1与阴离子的配位比。 其中, c(HG)=( I0- I)/ I0× c(H), I0代表未加阴离子的受体分子的荧光发射强度, I代表加入阴离子后的荧光发射, c(HG)是相应的受体分子的浓度。
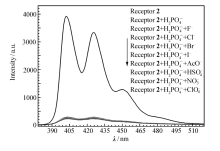
通过荧光光谱分析了受体分子1和2与各种阴离子之间的相互作用。 在乙腈溶液中,以370 nm光作为激发光时,受体分子1和2在402、428和450 nm处均有3个荧光发射峰,分别加入阴离子,使得阴离子的物质的量为受体分子的10倍。 如图1所示,H2PO4-离子加入时,受体分子1和2的荧光均发生了猝灭,但受体分子2的荧光猝灭程度更大。 其它阴离子F-、Cl-、Br-、I-、CH3COO-、HSO4-、ClO4-、NO3-的加入只引起受体分子荧光强度的微小变化,上述结果表明受体分子1和2均可以作为“turn-off”荧光传感器,用于H2PO4-的特异性识别。
为了进一步研究受体分子与H2PO4-之间的相互作用,进行了荧光滴定实验。 在受体分子1和2的乙腈溶液(浓度均为5×10-6 mol/L)中不断加入H2PO4-(1:0,0.1,0.2,0.4,0.6,0.8,1.0,2.0,3.0,……,10.0倍化学计量,2:0,0.1,0.2,0.4,0.6,0.8,1.0,2.0,3.0,……,15.0倍化学计量),如图2所示,随着H2PO4-离子浓度的增大,受体分子1和2在402,428和450 nm处的荧光强度逐渐降低,其中,受体分子1在加入1倍化学计量的H2PO4-时,其荧光强度不再有明显变化,猝灭百分数为13%,而受体分子2在加入7倍化学计量的H2PO4-时,其荧光强度不再有明显变化,猝灭百分数高达94%,说明受体分子2对H2PO4-的识别性能更好。 同时如图2中的内插图所示,在波长为365 nm紫外光照射下,受体分子1和2的乙腈溶液中加入H2PO4-后,荧光明显消失。 上述实验结果表明,受体分子1和2与H2PO4-之间发生了相互作用,推测其机理为光诱导电子转移过程(PET)[28]。 为了验证在识别H2PO4-离子时其它阴离子的干扰情况,考察了H2PO4-离子和其它阴离子的竞争性实验[29],结果如图3所示,加入相同化学计量的不同种类的阴离子后,H2PO4-依然能显著猝灭受体分子2的荧光,说明受体分子2在识别H2PO4-离子时,其它离子没有干扰。 根据荧光滴定曲线,受体分子2检测H2PO4-的线性范围为1.0×10-61.3×10-5 mol/L,最低检测限为3.8×10-6 mol/L。
利用Job曲线法可以确定受体分子与阴离子的配位比,如图4所示,受体分子1和2与H2PO4-的Job曲线均显示[HG]最大值对应的 x(G)值均为0.5,表明受体分子1和2与阴离子的结合比均为1:1。
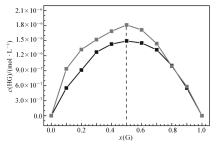 | 图4 受体分子1和2与H2PO4-作用的Job曲线(总浓度为5.0×10-6 mol/L)Fig.4 Job’s plot between receptors 1/2 and AcO- with a total concentration of 5.0×10-6 mol/L |
在超分子体系中,若主客体之间形成化学计量比为1:1的配合物,可通过以下方程非线性拟合求出相应的结合常数[30]:
I= I0+( Ilim- X0) /2 cH{ c(H)+ c(G)+
其中, I0代表未加入阴离子的受体分子的光谱强度; I代表加入阴离子后的光谱强度, c(H)和 c(G)是相应的受体分子和所加阴离子的浓度(mol/L); K为结合常数。 根据荧光光谱滴定曲线,经最小二乘法非线性拟合计算得到了受体分子1和2与阴离子的结合常数和相关系数(见表1)。 如表1所示,受体分子1和2与阴离子拟合的相关系数均大于0.99,再次表明受体分子1和2均与这些阴离子均形成了1:1型的配合物。
| 表1 受体分子1和2与阴离子的结合常数 Table 1 Binding constants of receptors 1 and 2 with various anions |
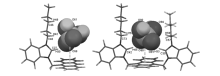
以DMSO- d6为溶剂,在受体分子1和2的溶液中分别加入1倍化学计量 H2PO4-均立刻生成白色沉淀,未能得到有效的核磁信号,因此无法通过H1 NMR研究受体分子与阴离子之间的作用机理。 为了研究受体分子与H2PO4-的具体结合模式,使用Gaussian 09软件,在PCM(MeCN)-B3LYP/6-31+G(d,P)的水平下采用DFT分别计算了受体分子1和2与H2PO4-之间的相互作用。如图5所示,受体分子1和2通过咪唑鎓中的C2-H与H2PO4-之间形成了非常强的离子型氢键(具体键长如表2所示),同时,受体分子1中的蒽环与H2PO4-之间的最近距离为0.3892 nm,受体分子2中的蒽环与与H2PO4-之间的最近距离为0.3769 nm,表明H2PO4-与受体分子1和2中的蒽环之间均存在较强的阴离子- π作用[31]。 受体分子1和2与H2PO4-结合后的最高已占轨道(HOMO)、最低未占轨道(LUMO)能级,以及HOMO-LUMO的能隙差值(HLG)见表3,H2PO4-与受体分子2的HLG小于受体分子1,表明受体分子2与H2PO4-的结合性能更好,这与荧光测试的结果一致。
| 表2 受体分子1和2与H2PO4-结合后的键长参数(nm) Table 2 Bond distances of receptors 1 and 2 with H2PO4-(nm) |
| 表3 DFT模拟计算的HOMO、LUMO、HOMO-LUMO能隙差值HLG(eV) Table 3 DFT calculated HOMO, LUMO, HOMO-LUMO gap HLG(eV) |
配制浓度为5.0×10-6 mol/L的受体分子2的乙腈溶液,并分别配制浓度为1.0×10-3、2.0×10-3和3.0 × 10-3 mol/L的四丁基磷酸二氢铵的乙腈溶液。 取2 mL受体分子2的溶液,向其中加入5 μL四丁基磷酸二氢铵溶液,使最终溶液中H2PO4-浓度为2.5×10-6、5.0×10-6和7.5×10-6 mol/L,充分混匀后测定荧光强度,结果如表4所示。 由表4可知,该法测量H2PO4-的精确度较好,回收率分别为99.4%、104.4%和100.2%,可以用来检测样品中的H2PO4-。
| 表4 基于受体分子2的乙腈溶液中H2PO4-离子检测结果 Table 4 Determination of H2PO4- in acetonitrile using the receptor 2 |
本文设计合成了基于蒽-苯并咪唑鎓的受体分子1和2,发现其在乙腈溶液中对阴离子H2PO4-均具有良好的选择性,可实现荧光识别,并具有荧光关闭(turn-off)的功效。 受体分子2在构型上与H2PO4-更匹配,对H2PO4-的识别性能更好。 该类受体分子有望成为对H2PO4-具有特异性荧光识别的探针,为生物化学和环境化学中H2PO4-的检测提供重要的方法。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|