共同通讯联系人:高博,讲师; Tel:029-62307017; E-mail:gaoboo_1989@126.com; 研究方向:离子液体的合成及应用
基于N
Co-corresponding author:GAO Bo, lecturer; Tel:029-62307017; E-mail:gaoboo_1989@126.com; Research interests:synthesis and application of ionic liquids
Based on N
离子液体(ILs)在室温或至100 ℃时呈液态,由有机阳离子和无机或有机阴离子组成[1],具有非常高的离子摩尔浓度,从而使其具有极低的蒸汽压,较高的离子电导率,较宽的液体稳定范围以及良好的溶解性能等特性[2,3,4,5,6,7,8,9]。 另外,可以通过选择不同的阴离子或改变阳离子的官能团来改善离子液体的物理化学性质[10,11,12,13]。 采用4-氨基-1,2,4-三唑作为阳离子合成的离子体,属于功能型离子液体的新体系,因其分子结构中含有大量的高能C—N和N—N键,故而称之为含能离子液体(EILs)[14]。
近年来,国内外的研究者广泛地研究了含能离子液体的熔点、密度、热稳定性、燃烧热和生成焓等物理化学性质[15,16,17,18,19,20],为离子液体结构的研究以及新型功能化离子液体的设计提供了基础[21,22,23]。 但是关于4-氨基-1,2,4-三唑类EILs溶解性质的研究仍然很少,只有少数离子液体在文献中有所报道,数据十分有限,且大多停留在定性研究离子液体在有机或无机溶剂中的溶解,并未定量地研究其溶解性,对其溶解度和溶解度的一般规律则很少关注[24,25]。 因此,EILs的溶解性质研究的不足成为阻碍其在含能材料中应用的瓶颈。
本文基于N
4-氨基-1,2,4-三唑(ATZ)、溴代正丁烷(C4H9Br,分析纯)、溴代正戊烷(C5H11Br,分析纯)、溴代正己烷(C6H13Br,分析纯)和溴代正癸烷(C10H21Br,分析纯)均购自阿尔法试剂公司;硝酸银(AgNO3)、高氯酸银(AgClO4)、乙腈(CH3CN)、乙醇(C2H5OH)、二氯甲烷(CH2Cl2)和无水甲醇(CH3OH)购自国药集团化学试剂有限公司,均为分析纯试剂,纯度大于99%;双氰胺钠盐(NaN(CN)2)、2,4,5-三硝基唑类铵盐(NH4[2,4,5-TNI])和3,5-二硝基-1,2,4-三唑钠盐(Na[3,5-DNTZ])实验室自制,纯度大于98%。
AVANCE 300型超导傅里叶数字化核磁共振谱仪(NMR,德国Bruker公司);DDS-307型电导率仪(杭州科晓化工仪器设备有限公司);FA2004N型分析天平(上海天平仪器厂);旋转蒸发仪;DZF-6020型真空干燥箱(上海精宏实验设备有限公司)。
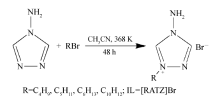
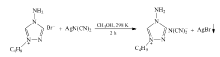
将ATZ(5 g)和C4H9Br(23 mL)和CH3CN(50 mL)置于200 mL圆底烧瓶中,在50 ℃均匀搅拌反应2 h,升温至85 ℃反应48 h直到ATZ完全反应。 在40 ℃,用旋转蒸发仪对产物减压蒸馏至无气泡冒出,在40 ℃真空干燥48 h,得到浅黄色粘稠液体1-丁基-4-氨基-1,2,4-三唑溴离子液体([BATZ]Br)。 按照Scheme 1的合成路线,合成其它1-烷基-4-氨基-1,2,4-三唑溴离子液体([RATZ]Br)。
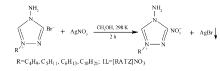
将[BATZ]Br和AgNO3按摩尔比1∶1.2加入到CH3OH中,磁力搅拌至反应物充分溶解,在25 ℃反应2 h,用砂芯漏斗过滤。 在40 ℃,使用旋转蒸发仪对该产物减压蒸馏,至无气泡冒出,在40 ℃真空干燥48 h,得到黄色粘稠状液体,即1-丁基-4-氨基-1,2,4-三唑硝酸盐含能离子液体([BATZ]NO3)。 按照Scheme 2的合成路线,合成其它1-烷基-4-氨基-1,2,4-三唑硝酸盐含能离子液体([RATZ]NO3)。
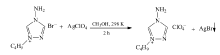
将[BATZ]Br和AgClO4按摩尔比1∶1.2加入到含有无水甲醇的圆底烧瓶中,均匀搅拌至反应物充分溶解,在25 ℃下反应2 h,用砂芯漏斗过滤。 在30 ℃,对产物进行旋转减压蒸馏至无气泡产生,在30 ℃真空干燥48 h,得到淡黄色粘稠状1-丁基-4-氨基-1,2,4-三唑高氯酸盐EILs([BATZ]ClO4),如Scheme 3所示。
[BATZ]Br和AgN(CN
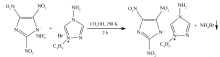
[BATZ]Br和NH4[2,4,5-TNI][27]按摩尔比1∶1.2加入到含有无水甲醇的100 mL圆底烧瓶中,磁力搅拌器均匀搅拌至反应物完全溶解,25 ℃下反应2 h,砂芯漏斗过滤。 对反应粗产物在30 ℃进行旋转蒸馏至呈黄色粘稠状液体,在30 ℃温度下真空干燥48 h,即得1-丁基-4-氨基-1,2,4-三唑·2,4,5-三硝基唑类EILs([BATZ][2,4,5-TNI]),如Scheme 5所示。
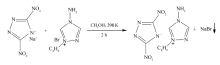
[BATZ]Br和Na[3,5-DNTZ][28]按摩尔比1∶1.2加入到含有无水甲醇的100 mL圆底烧瓶中,磁力搅拌器均匀搅拌,25 ℃下反应2 h,砂芯漏斗过滤。 对反应粗产物进行旋转蒸馏至呈黄色粘稠状液体,真空干燥48 h,温度均为30 ℃,得到1-丁基-4-氨基-1,2,4-三唑3,5-二硝基-1,2,4-三唑含能离子液体([BATZ][3,5-DNTZ]),如Scheme 6所示。
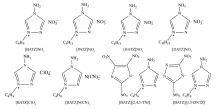
称量上述合成的[RATZ]NO3、[BATZ]ClO4、[BATZ]N(CN)2、[BATZ][2,4,5-TNI]和[BATZ][3,5-DNTZ]含能离子液体,计算产率。 将上述含能离子液体的符号、名称、简写、纯度以及产率列入表1中,结构图如Scheme 7所示。
| 表1 1-烷基-4-氨基-1,2,4-三唑类含能离子液体的符号、名称、简写、纯度以及产率 Table 1 The code, name, abbreviation, formula, purity and yield of EILs |
采用电导率仪和分析天平测定[RATZ]NO3、[BATZ]ClO4、[BATZ]N(CN)2、[BATZ][2,4,5-TNI]和[BATZ][3,5-DNTZ]含能离子液体在水、甲醇、乙醇、丙酮和乙腈中的溶解度,温度 T=293 K。 将电导率仪的电极置于装有10 g上述溶剂的烧瓶中,分别将合成的含能离子液体逐滴缓慢添加到烧瓶中,观测电导率的变化,直至电导率保持恒定,通过测定溶解在溶剂中含能离子液体的质量(g)得到其溶解度 S(g/10 g)。 溶剂依介电常数即极性从大到小排列,分别为水(78.5)、乙腈(37.5)、甲醇(32.5)、乙醇(24.5)和丙酮(20.7)。
采用核磁共振谱仪对[RATZ]NO3、[BATZ]ClO4、[BATZ]N(CN)2、[BATZ][2,4,5-TNI]和[BATZ][3,5-DNTZ]含能离子液体进行1H NMR表征,以CDCl3为锁定溶剂,化学位移以TMS为内标。 1-烷基-4-氨基-1,2,4-三唑类含能离子液体的1H NMR见表2。 由表2可知,合成的含能离子液体1H NMR谱与目标产物一致,不含杂质。
| 表2 1-烷基-4-氨基-1,2,4-三唑类含能离子液体含能离子液体的1H NMR谱 Table 2 1H-NMR data of the synthesized EILs |
2.2.1 含能离子液体与溶剂的分子间作用能
小分子化合物的溶解机理是溶剂和溶质分子之间存在着一种相互作用,它可以破坏溶质分子之间的相互作用,使溶质分子从溶剂的表面逐渐消失,然后通过扩散均匀地分散到溶剂中[25]。 溶剂和溶质分子之间的相互作用可以用范德华力和氢键相互作用能两种力的平衡来描述,直接影响上述含能离子液体的溶解性。 因此,采用MP2/6-311G++(2d,p)对EILs、溶剂以及EILs-溶剂进行结构优化,其分子间相互作用能Δ E[24]由式(1)得到:
其中,A为EILs;B为溶剂; EA-B、 EA和 EB分别为A-B、A和B的单点能, EA-B、 EA和 EB的单位分别为a.u.。 EIL-溶剂的分子间作用能(Δ E)列于表3。
| 表3 1-烷基-4-氨基-1,2,4-三唑类含能离子液体与溶剂之间的分子间相互作用能(Δ E/(kJ·mol-1)) Table 3 Interaction energies(Δ E/(kJ·mol-1)) of the EILs-solvents by MP2/6-311G++(2d,p)) |
图1为1-烷基-4-氨基-1,2,4-三唑类含能离子液体与溶剂之间的分子间作用能与不同阳离子结构和不同阴离子结构之间的关系图。图1A中,当阳离子不同时,随着烷基链的增长,[RATZ]NO3与溶剂间的作用能曲线呈升高趋势,其中[BATZ]NO3与溶剂间的Δ E绝对值最大,分子间作用能越负,离子液体与溶剂之间的作用能绝对值越大,形成的结构越稳定,因为烷基链增长导致阳离子的体积变大,使[RATZ]NO3对称性降低,较大的空间位阻阻碍了溶剂分子靠近[RATZ]NO3含能离子液体。
 | 图1 不同阳离子结构和不同阴离子结构与1-烷基-4-氨基-1,2,4-三唑类含能离子液体与溶剂之间的分子间作用能之间的关系Fig.1 Relationship of interaction energies(Δ E) and structure of EILs |
图1B中,当阴离子不同时,[BATZ][2,4,5-TNI]和[BATZ][3,5-DNTZ]含能离子液体与溶剂间作用能绝对值比[BATZ]NO3、[BATZ]ClO4和[BATZ]N(CN)2大,其分子间作用能更负,形成的结合能更大,结构更稳定,因为[2,4,5-TNI]-和[3,5-DNTZ]-阴离子含有多个—NO2,可以与溶剂形成更多的氢键,分子间作用能增大。
2.2.2 含能离子液体的偶极矩
采用MP2/6-311G++(2d,p)方法,得到[RATZ]NO3、[BATZ]ClO4、[BATZ]N(CN)2、[BATZ][2,4,5-TNI]和[BATZ][3,5-DNTZ]含能离子液体的偶极矩,如图2所示,图2为1-烷基-4-氨基-1,2,4-三唑类含能离子液体的偶极矩与其阴阳离子结构之间的关系图。图2A为[RATZ]NO3含能离子液体的偶极矩与阳离子结构之间的关系。 从图2A看出,随烷基链的增长偶极矩减小,[RATZ]NO3的极性下降,这是因为三唑环上的正电荷对N原子上取代基烷基链有 p-π超共轭诱导效应,烷基链越长可从三唑环上获得更多的正电荷,从而使三唑环上的有效正电荷减少。图2B为[BATZ]NO3、[BATZ]ClO4、[BATZ]N(CN)2、[BATZ][2,4,5-TNI]和[BATZ][3,5-DNTZ]含能离子液体的偶极矩与阴离子结构的关系。 从图2B看到,[BATZ]NO3、[BATZ]ClO4和[BATZ]N(CN)2的偶极矩随着阴离子极性的减小而减小。 阴离子极性大小顺序为N(CN
 | 图2 1-烷基-4-氨基-1,2,4-三唑类含能离子液体的偶极矩与结构之间的关系Fig.2 Relationship of the dipole moment and the structure of EILs |
对于[BATZ][2,4,5-TNI]和[BATZ][3,5-DNTZ],—NO2越多其诱导作用越强,负电中心的有效电荷越少,则偶极矩减小;咪唑环上的-N(CH) =增大了阴离子的正电性,使负电中心的有效电荷增多,极性增大,即偶极矩增大。 由于[2,4,5-TNI]-和[3,5-DNTZ]-阴离子极性较大,[BATZ][2,4,5-TNI]和[BATZ][3,5-DNTZ]的偶极矩大于[BATZ]NO3、[BATZ]ClO4和[BATZ]N(CN)2。
含能离子液体具有极佳的溶解性能,其在溶剂中溶解是由于溶剂和离子液体分子或离子之间存在相互吸引力,破坏了离子液体分子间与分子内的相互作用力,使其通过扩散作用均匀地分散到溶剂中[14],下面讨论极性、结构对含能离子液体溶解度的影响。表4为25 ℃下1-烷基-4-氨基-1,2,4-三唑类([RATZ]NO3、[BATZ]ClO4、[BATZ]N(CN)2、[BATZ][2,4,5-TNI]和[BATZ][3,5-DNTZ])含能离子液体在不同极性溶剂中的溶解度。
| 表4 1-烷基-4-氨基-1,2,4-三唑类含能离子液体298 K时的溶解度 S(g/10 g) Table 4 Solubility( S) of the EILs in different solvents at 298 K( p=0.1 MPa) |
2.3.1 含能离子液体溶解性能与溶剂极性的关系
根据表4得到溶剂分子极性对1-烷基-4-氨基-1,2,4-三唑类([RATZ]NO3、[BATZ]ClO4、[BATZ]N(CN)2、[BATZ][2,4,5-TNI]和[BATZ][3,5-DNTZ])含能离子液体的溶解性能的影响如图3所示。
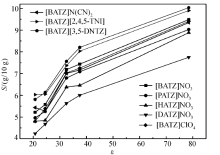 | 图3 溶剂分子极性对含能离子液体溶解度的影响Fig.3 Influence of dielectric constant( ε) of solvent on the solubility of EILs at 298.15 K( ε:water 78.5, acetonitrile 37.5, methanol 32.5, ethanol 24.5, acetone 20.7) |
从图3可看出,随着溶剂介电常数 ε的减小即极性的减弱,上述含能离子液体的溶解度呈减小趋势,不同[RATZ]NO3的偶极距随着烷基链的增长减小,其溶解度随着烷基链的增长、自身极性的减小以及溶剂极性的减小而减小。 因为水、乙腈、甲醇、乙醇为质子性溶剂能够提供质子与离子液体以氢键相缔合,溶解度大;另外,丙酮为偶极非质子性溶剂, C-N…O可以形成氢键,在上述含能离子液体的阳离子中,与氮原子直接相连的亚甲基上的氢原子可以与丙酮羰基上的氧原子形成氢键,使其在丙酮中的溶解度较大。
2.3.2 含能离子液体溶解性能与其结构的关系
根据表4得到图4,从图4中可以看出,[RATZ]NO3含能离子液体的阴离子相同时,在极性溶剂中的溶解度随着阳离子烷基链长的增加、分子间相互作用能的减小而减小。 因为阳离子中的烷基链是分子中的亲水性部分,有能力极化至形成氢键,烷基链越长亲水性越差,极性越弱,在非极性溶剂中易于溶解;且烷基链增长导致阳离子的体积变大,分子间作用能减小,较大的空间位阻阻碍了溶剂分子靠近该含能离子液体,溶解性能变差。
阳离子相同时,含能离子液体在溶剂中的溶解度大小顺序为[BATZ][3,5-DNTZ]>[BATZ][2,4,5-TNI]>[BATZ]NO3>[BATZ]ClO4>[BATZ]N(CN)2,这是因为阴离子对离子液体溶解性的影响主要与阴离子形成氢键的能力有关,易形成氢键的溶解度大;此外,形成氢键数量越多,含能离子液体与溶剂之间的分子间作用能越大(见表3)。
综上所述,[RATZ]NO3、[BATZ]ClO4、[BATZ]N(CN)2、[BATZ][2,4,5-TNI]和[BATZ] [3,5-DNTZ]含能离子液体本身就是一种强极性溶剂,遵循相似相溶原理,故其在极性溶剂中溶解性较好。
本文合成了系列1-烷基-4-氨基-1,2,4-三唑类([RATZ]NO3、[BATZ]ClO4、[BATZ]N(CN)2、[BATZ][2,4,5-TNI]和[BATZ][3,5-DNTZ])含能离子液体。 对上述含能离子液体溶解性能的研究表明:含能离子液体在不同溶剂中的溶解度随着溶剂介电常数 ε即极性的减小而降低,上述含能离子液体的溶解度呈减小趋势,不同[RATZ]NO3的偶极距随着烷基链的增长减小,其溶解度随着烷基链的增长、自身极性的减小以及溶剂极性的减小而减小;阴离子相同时,[RATZ]NO3含能离子液体在极性溶剂中的溶解度随着阳离子烷基链长的增加而减小;阳离子相同时,在溶剂中的溶解度大小顺序为[BATZ][3,5-DNTZ]>[BATZ][2,4,5-TNI]>[BATZ]N(CN)2>[BATZ]NO3>[BATZ]ClO4,与阴离子形成氢键的能力有关,易形成氢键的溶解度大。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|