二维(2D)层状石墨型氮化碳纳米片(CNNS)由于具有各向异性的2D几何形态和芳香族 p-π共轭骨架,高度开放的平面结构、超高的比表面积、增强的电子迁移速率和与层厚度相关可调的半导体带隙等特征,是目前2D层状材料的研究热点之一。 本文综述了近年来氮化碳纳米片的各种制备方法、功能化改性和应用,涉及环保、能源转换及生物传感等领域。 最后指出进一步探索制备高质量氮化碳纳米片的新方法以及拓展其在光催化领域的应用是未来研究的重点。
Two-dimensional(2D) layered graphitic carbon nitride nanosheets(CNNS) have an anisotropic two-dimensional geometry and aromatic p-π conjugated backbone, a highly open planar structure and high specific surface area, and enhanced charge-carriers transfer rate and adjustable band gap related to the layer thickness, and become one of the top two-dimensional layered materials for research. This article reviews various preparation and modification methods and applications of carbon nitride nanosheets in environmental protection, energy conversion, and biosensing, etc., in recent years. Finally, it can be concluded that exploring the new preparation methods of carbon nitride nanosheets with high quality and finding more applications of the photocatalysis are the focus of the future research.
二维(2D)层状材料[1],特别是纳米片材料,具有层间限域效应、量子尺寸效应等而显示出独特的物理化学性能,在生物学、医学、物理学和化学领域的应用展现了巨大的机会和前景[2,3,4,5] 。 石墨烯,作为一种典型的2D层状材料[6,7],由单层碳原子以 sp2杂化轨道组成六边形呈蜂巢形晶格排列,显示出许多优异的特性,例如优异的载流子迁移率,机械强度和高的热/化学稳定性,这使得石墨烯在电子器件、生物工程和能量储存领域有着广泛应用[8,9]。 除了零带隙石墨烯和杂原子(例如B、N、P等)掺杂的石墨烯,其它2D纳米片的制备也引起了研究者极大的兴趣,特别是具有半导体特性的纳米片[10,11,12]。 纳米片材料具有可以通过调节其厚度来调节能带结构的特征,这进一步扩展了2D纳米片材料在电子和光电子领域的应用。 迄今为止,科学家们已经制备出多种2D纳米片材料,诸如:石墨烯或氧化石墨烯(GO)、过渡金属氧化物、金属硫属元素化物、氮化物和过渡金属磷酸盐等,与其块状材料相比,在储能、传感器、电子器件和催化等领域显示出巨大优势[13,14,15]。
普通石墨型氮化碳( g-C3N4)又称为体相氮化碳(bulk CN),作为一种新型无金属层状催化剂受到了广泛关注。 由于bulk CN具有比表面积不高、光生电子-空穴对复合快、对可见光响应范围窄和量子效率低等缺点,导致其光催化效率不高。 2D石墨型氮化碳纳米片(CNNS)因其具有200~300 m2/g的较高比表面积、光生载流子迁移速率快、活性位点多等优点,成为了近期的研究热点[16,17,18]。
氮化碳具有与石墨烯类似的层状结构,即2D平面内形成强的C—N共价键,层间以范德华吸引力相连[19](图1a);而将体相氮化碳进行层剥离被认为是获得氮化碳纳米片的可行方法[20](图1b)。 与零能带隙的石墨烯或杂原子掺杂石墨烯不同,剥离得到的氮化碳纳米片保留了原有氮化碳的芳香杂环结构,使其具有比体相氮化碳更多的优点[21,22]。 首先,高度开放的2D平面结构以及较大的比表面积有利于对光和反应物分子的捕获和收集,使得其表面更易与反应物分子反应;其次,超薄的层状结构显著缩短了电子从体相转移到表面的距离,促进平面内的电子传输并能减少电荷复合产生的能量损耗[23,24,25]。 本文综述了近期氮化碳纳米片的制备方法以及有望用于如能源再生和环境治理(光催化剂,析氧反应,氧气还原反应)、生物成像、医药、电化学发光等领域的功能化研究进展,并对其在光催化剂研究领域的进展做了重点阐述和展望。
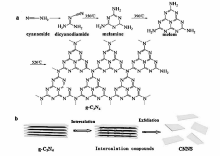 | 图1 g-C3N4结构示意图(a)[19]和 g-C3N4剥离示意图(b)[20]Fig.1 Scheme of g-C3N4 structure(a)[19] and scheme of g-C3N4 exfoliation(b)[20] |
目前各种氮化碳纳米片的制备方法可以分为两大类:一是剥离法,将体相氮化碳通过物理或化学方法剥离成分散的纳米片;二是模板法,采用合适的片状模板合成氮化碳纳米片。
基于氮化碳的类石墨层状结构,常见的有3种方法可以剥离氮化碳,使之成为层数较少的氮化碳纳米片,主要包括超声辅助液相剥离、热氧化刻蚀剥离和化学剥离法。
1.1.1 超声辅助液相剥离
受氧化石墨烯超声制备方法的启发,人们发现CNNS也可以用超声剥离加液相分散的超声辅助液相剥离法制备。 Zhang等[26]将bulk CN分散在水里,经过16 h的超声剥离将块体氮化碳剥离成纳米片。 Schwinghammer等[27]用熔盐法制备出聚三嗪酰亚胺(PTI/Li+Cl-),与普通的共价键型的 g-C3N4相比,PTI/Li+Cl-是结晶良好的盐类化合物,呈六元环状。 层内以三嗪环相连,层间为弱的范德华作用力,层间间隙中存在Li+和Cl-。 通过水溶液剥离,可以得到2~4个PTI层厚的纳米片。剥离后的纳米片结构未发生改变,其增大的比表面积和量子限域效应导致光催化分解水制氢的速率达到未剥离的PTI/Li+Cl-的15倍。
Yang等[28]用异丙醇(IPA)作溶剂成功将体相氮化碳剥离成厚度约为2 nm,横向尺寸达到微米级别的CNNS。 由于未经过任何高温处理或氧化过程,得到的CNNS依然保持有原始晶体的结构和化学计量比,是一种比较理想的剥离方法。 但缺点是耗费时间,纳米片大小和厚度难以控制。
在液相剥离过程中人们发现,一些含水的混合溶液,包括乙醇水溶液、异丙醇水溶液和四氢呋喃水溶液,可以进一步提高液相剥离效果,制备出厚度仅为0.35 nm的CNNS,并且能够在溶液中实现稳定的单层分散[29]。 此外由于氮化碳具有七嗪环结构,可用质子酸如H2SO4、HCl等质子化氮化碳,使氨基上的N原子与H+结合,可以扩大层间距。 通过质子化处理可明显缩短超声处理时间,同时还会显著增加CNNS的产量和质量。 结果显示,用H2SO4处理过的纳米片厚度为0.4 nm,宽度则为微米级别[30]。 另外,Yin等[31]使用离子半径非常小的锂离子插层氮化碳进行剥离可以制备出几个原子层厚度的CNNS(图2),经锂化剥离后的CNNS表现出良好的析氢性能,约为8 μmol/h,达到bulk CN的两倍。
 | 图2 锂插层剥离 g-C3N4示意图[31]Fig.2 Schematic diagram of the lithiation and exfoliation of g-C3 |
1.1.2 化学氧化剥离
1)研究表明空气的氧化作用削弱氮化碳层间的范德华力。 Niu等[32]通过在空气中对体相氮化碳固体进行直接热氧化蚀刻制备出了CNNS,其片层结构如图3所示,可以认为是空气插层后通过加热膨胀削弱层间范德华力从减少层厚度。 层厚度是可以通过逐层热蚀刻工艺减小到期望的层数,如在500 ℃下将空气中的CN固体直接加热2 h可制备厚度约为2 nm的CNNS(约6、7层的CN)。 这是一种快速、低成本和环保的方法,适用范围广泛。
Dong等[33]用热聚合的方法煅烧硫脲制备 g-C3N4,再分别在450、500和550℃下煅烧bulk CN,制备出不同比表面积的CNNS,bulk CN比表面积仅有 26 m2/g,550 ℃下煅烧得到的纳米片达到151 m2/g的比表面积,并且随着温度和处理时间的增长,得到的纳米片厚度不断减小,比表面积继续增大。
到目前为止,热氧化剥离方法合成的CNNS已被广泛地用作可持续转化太阳能的光催化剂。 然而,在热剥离过程中会产生大量的界面缺陷,且产率也很低(<10%),所以难以大规模的工业化制备,目前仅能在实验室使用。
2)氮化碳在碱溶液中进行剥离时,有两种可能发生的反应:一是OH-和—NH2在CN层间形成氢键;二是OH-与—NH2末端连接的杂环碳原子之间发生亲电取代,导致部分—NH2基团被OH-取代。 CN表面会被强碱所侵蚀,同时也会插层到CN的层间,使CN表面带负电。 层间的弱范德华力被破坏,导致片层分离,形成超薄氮化碳纳米片。 在碱剥离中碱的强度是影响 g-C3N4剥离效果的关键因素。 强碱更利于体相氮化碳剥离成超薄纳米片。 基于此原理,Li等[34]用KOH溶液在80 ℃反应24 h,形成透明的纳米片胶体溶液,得到厚约0.4 nm、横向尺寸为50~100 nm的纳米片。 Zhang等[35]将bulk CN与浓氨水混合均匀后,置于反应釜中在180 ℃下反应12 h,所得产物水洗后再在水中超声6 h,得到了尺寸小于30 nm的纳米片。
3)酸剥离主要利用氧化性酸的强氧化能力,通过削弱 g-C3N4层间弱的范德华力,使层与层分离成超薄纳米片。 Chen等[36]将bulk CN研磨成粉末后与HNO3充分混合,回流24 h,产物干燥后得到200 nm尺寸大小的 g-C3N4纳米片。 发现其具有良好的荧光性质,在365 nm 紫外光的激发下发射出强烈的波长为435 nm的蓝色荧光。 由于浓硫酸具有很强的氧化能力和放热性,也可以削弱 g-C3N4层之间的相互作用力,可将体相 g-C3N4剥离成少层的CNNS。 Du等[37]用浓硫酸高温处理氮化碳,经水稀释后,低温结晶过滤洗涤干燥后得到50~200 nm尺寸的白色 g-C3N4纳米片。 他们提出了酸剥离的3个必备条件:强酸、高温和无水环境。 强酸提供了强氧化能力、剥离和酸化的条件,高温可以破坏层间的范德华力,而无水环境能减少氮化碳在强酸型条件下的水解。 Cheng等[38]将块状 g-C3N4加入硫酸中超声辅助剥离,超声结束后 g-C3N4立刻凝聚,通过蒸馏水洗涤后,得到 g-C3N4纳米片。 结果发现 g-C3N4在酸性介质中带有正电荷,在碱性介质中带负电荷,显示出两性性质。 利用这种方法可以通过改变溶液的pH值,合成具有不同电性的 g-C3N4结构。
通过化学剥离法虽然能够大量制备CNNS,但浓酸浓碱的使用和高温条件的操作是苛刻和危险的,并且制备出的纳米片大小无法控制,层数较多,耗时较长,因此化学剥离法还需进一步改进。
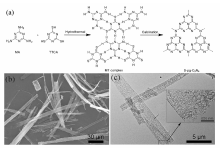
模板法是一种通用的纳米结构制造方法,可用于多种纳米结构氮化碳的构筑,主要包括硬模板法和软模板法。 一个典型的硬模板制备CNNS工艺如图4所示[39],首先通过氧化石墨烯(GO)为模板得到硬模板二氧化硅纳米片,进一步采用乙二胺和四氯化碳的聚合作用合成了CNNS。 Liu等[40]发现,通过调节氰胺在硅藻基质上的组成成分比例和加热温度实现氰胺的可控缩聚可获得CNNS。 Fan等[41]以Triton X-100为预模板剂对三聚氰胺进行结构修饰,之后洗去模板剂,通过煅烧得到多孔氮化碳。 其优点在于Triton X-100本身不参与 g-C3N4的聚合过程,避免了模板剂的过早分解导致结构破坏。
最近,Liu等[42]以Mg-Al水滑石(LDH)为模板,利用水滑石层间的量子限域作用制备CNNS:将制备好的Mg-Al水滑石浸泡在尿素溶液中,使尿素分子插层到水滑石的层间,经微波处理后得到了CN/LDH的复合材料(图5)。 这种复合材料有着高达95.9%的固态量子产率,是迄今为止固态量子产率中最高的。 而且CN/LDH复合材料的化学、热稳定性也很好。
独特的2D纳米片形态,以及内在的共轭聚合物的结构,使CNNS具有广泛的应用前景。 例如,CNNS可用作无金属光催化剂在太阳能辐照条件下来催化相关化学品的获得,如光催化分解水,二氧化碳光还原等。
Lin等[43]用乙二醇作溶剂,CNNS、十六烷基三甲基溴化铵和PVP为原料,通过溶剂热的方法制备出鱼鳞状氮化碳纳米片(FSGN),具体步骤如图6所示。 其中样品FSGN拥有较高的比表面积,表现出优异的析氢活性和出色的稳定性。 通过粉末X射线衍射(XRD)可以看出,鱼鳞状结构的制备并未破坏CN本身的结构,表明其结晶程度较好。 测试表明,FSGN的荧光寿命比CNNS的要长很多,说明结构诱导的选择性电子迁移有利于光生电荷的分离和迁移,导致光生载流子的寿命大幅提高,从而提高了其光催化性能。
Wang等[44]用三聚氰胺做原料通过预聚合-再聚合两步法制备出多孔氮化碳纳米片,并且比较了块状氮化碳和多孔氮化碳纳米片的荧光寿命,发现多孔氮化碳纳米片的光生电子空穴的分离要比块状氮化碳好。 从催化剂的比表面积来看,多孔氮化碳纳米片的比表面积从原来的5.8 m2/g增加到了71.8 m2/g,由于多孔结构的形成导致比表面积的增加,从而显示出了优异的光催化性能。 Fan等[45]在多孔氮化碳纳米片的基础上负载CdS量子点,形成稳定的异质结结构。 他们认为,多孔结构有助于CdS量子点的分散、抑制其团聚而且对CdS又有固定作用。 同时CdS量子点能够扩大光吸收范围,提高其光催化活性。
Fan等[46]使三聚硫氰酸和三聚氰胺在水中形成三聚氰胺-三聚硫氰酸复合物(MT),通过煅烧这种前体来制备S掺杂的氮化碳纳米带。 三聚硫氰酸既可以被认为是一种模板,也可以看作是硫源,三聚硫氰酸在高温热解产生气体形成多孔结构,少量S元素能够进入 g-C3N4的骨架中,最终形成S掺杂的多孔氮化碳纳米带(S- pg-C3N4),如图7所示。
Yan等[47]采用水热法制备了TiO2/C3N4异质结2D催化体系,TiO2纳米颗粒均匀分散在C3N4 纳米片表面上且紧密接触,显著提高了光生电子空穴的分离效率;将形成的TiO2/C3N4异质结作为Z型光催化体系, β-Ni(OH)2/WO3作为产氧催化剂,很大程度上提高了水的分解效率,在405 nm的单色可见光照射下,量子效率为4.01%。 Ye等[48]通过原位合成法将二维C3N4纳米片负载到一维的CoTiO3微米棒表面上,在420 nm可见光下其量子效率为3.23%。 Katsumata等[49]用煅烧法将CNNS与WO3 颗粒复合构建二维Z型光催化体系,在不添加任何牺牲剂条件下产氢率达到了110 μmol/(h·g)。
通过上述方法制备的CNNS除形貌不可控以外,还存在由于光生电子和空穴复合较快导致量子产率低的问题,另外剥离形成的CNNS仅对420 nm以内的可见光有吸收,对可见光的利用率不足也是其亟待解决的问题。 通过元素掺杂可以有效调节CNNS的带隙结构,拓宽其可见光的吸收范围,提高光催化效率以及产生更多活性位点。
Deng等[50]用三聚氰胺和氨基乙基膦酸为原料,经过两步煅烧制备出磷掺杂的CNNS,磷掺杂可以提高可见光的利用率,并且提高光生电子和空穴的分离效率,使得磷掺杂的CNNS对Cr(Ⅵ)重金属离子和RhB染料有着良好的降解性能。 Pan等[51]通过静电作用使CoP和Pt纳米粒子沉积在CNNS上,发现经过CoP和Pt两种助催化剂的修饰后,CNNS可以实现对水的光催化全分解,通过两种助剂的负载,提高了光生电子和空穴的分离度,同时两个助剂之间的协同作用也会提高光催化性能。
Ran等[52]通过P元素掺杂和热剥离技术成功制备了多孔P掺杂的CNNS,即PCN-S(图8),在PCN-S的导带下方出现了空的能隙间隔,可以容纳从价带激发上来的光生电子,大大促进了 g-C3N4对于能量低于带隙值的光子的吸收。 P掺杂使得体相氮化碳的带隙从2.78 eV降低到2.68 eV,并且扩大了对可见光的响应范围,使其在光催化制氢过程中能够利用波长为557 nm的可见光。 P掺杂 g-C3N4纳米薄片的产氢速率(1596 μmol/(h·g))是体相 g-C3N4产氢速率(108 μmol/(h·g))的14.8倍。
 | 图8 PCN-S的TEM图和AFM图(a)及PCN-S的N2吸脱附曲线和孔径分布图(b)[52]Fig.8 TEM image of PCN-S with the inset showing the high magnification TEM image, the AFM image and the corresponding height profile of PCN-S(a) and N2 sorption isotherms of CN-B, CN-S, PCN-B and PCN-S with the inset displaying the corresponding pore size distribution curves(b)[52] |
在可见光条件下分解水产氢,实现能源的再生利用是解决能源紧缺,环境污染的理想方法。 氮化碳由于具有合适的价能结构,可被用作光催化分解水的催化剂。 2009年,Wang等[16]首次验证了氮化碳可以作为一种非金属光催化剂在可见光下分解水。 Yang等[53]用简单的超声剥离方法来制备出CNNS。 剥离后的CNNS由于能够暴露更多的活性位点,可以提升其光催化活性。 CNNS在420 nm的可见光波长下的平均制氢速率为93 μmol/h,量子产率为3.75%。 Niu等[32]用热剥离的方法制备出约2 nm厚的CNNS,在>400 nm可见光下的析氢速率约为30 μmol/h ,远大于体相氮化碳的析氢速率。
Zhao等[54]用热剥离和超声联用的方法制备出单层 g-C3N4纳米片。 单层的CNNS由于其厚度大大降低,使光生电子到达其表面的能量显著降低,活性位点增多,既提高到了催化效率,也增加了材料的稳定性,CNNS在10次光降解循环后依然无明显的活性损失。 Shao等[55]制备出三元CN/RGO/ZnS体系,发现CN/RGO/ZnS复合材料在60 min内可以完全降解RhB。 其中RGO作为载体,有着优异的光生载流子迁移速率,CN和ZnS形成TypeⅡ异质结负载在RGO上。 经过光照,光生电子从CN的导带转移到ZnS的导带,再转移到RGO上产生·O2-;空穴从ZnS转移到CN的价带上,产生空穴(h+)来降解RhB。
g-C3N4纳米片因其独特的 π共轭有机骨架结构和多样的2D片层结构制备方法以及优异的光催化活性而引起了科学家们的浓厚兴趣。 迄今为止,制备 g-C3N4纳米片有热氧化刻蚀法、化学剥离法、超声辅助液相剥离法和模板法等多种方法。 由于2D纳米片结构所特有的性质和氮化碳本身芳香杂环所特有的π共轭体系, g-C3N4纳米片在光催化剂、析氢和析氧反应、储能领域、生物成像、ECL检测等领域被广泛应用。 为了进一步利用 g-C3N4纳米片,已经开发了一些旨在改进材料功能的有效方法来对 g-C3N4纳米片进行改性,即形成异质结、掺杂、负载、敏化和共聚等方法。 这些方法明显提高了 g-C3N4纳米片的相应性能,突出了纳米片的优势。
目前,尽管在 g-C3N4纳米片的合成和功能化改性方面取得了长足进展,但还存在难以可控合成出单层或少层和缺陷较少、结晶度高的 g-C3N4纳米片;其次是纳米片固有的团聚会严重劣化 g-C3N4纳米片的催化性能。 综上所述,我们认为今后 g-C3N4纳米片的研究方向有:1)继续探索高质量 g-C3N4纳米片的合成方法,特别是能有效控制2D氮化碳材料的层数,进而调控半导体的能带结构,更好地用于氮化碳基功能材料的设计;2)通过形貌控制及掺杂等一系列改性手段提升其催化性能;3)与其它材料复合形成多元Z型光催化体系。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|
| [49] |
|
| [50] |
|
| [51] |
|
| [52] |
|
| [53] |
|
| [54] |
|
| [55] |
|