为得到分散性和稳定性较好的聚多巴胺纳米粒子,利用“沉淀-再分散法”高效制备了聚多巴胺纳米粒子水分散液。 首先利用溶液氧化法制备了分散在水/乙醇中的聚多巴胺纳米粒子,然后向分散液中加入丙酮使聚多巴胺纳米粒子絮凝。 收集沉降物,用丙酮冲洗并干燥后,加水重新分散得到纯化的聚多巴胺纳米粒子水分散液。 丙酮沉淀法得到的聚多巴胺纳米粒子形貌规整,分散性好,粒径分布在250 nm左右,在水中具有良好的储存稳定性和光热性能,与传统的超速离心提纯法相比,产率可提高57.4%。 此方法为其之后在药物载体及光热治疗等方面的应用研究提供了便利。
In order to obtain dispersive and stable polydopamine nanoparticles, an aqueous dispersion of polydopamine nanoparticles was efficiently prepared using the “precipitation-redispersion” method. First, polydopamine nanoparticles dispersed in water/ethanol were prepared by a solution oxidation method, and then acetone was added to the dispersion to flocculate the polydopamine nanoparticles. The precipitate was collected, rinsed with acetone and dried, and then redispersed in water to obtain a purified aqueous dispersion of polydopamine nanoparticles. The polydopamine nanoparticles obtained by the acetone precipitation method are regular in shape with good dispersibility. The particle size distribution is about 250 nm, and has good storage stability and photothermal properties in water. Compared with conventional ultracentrifugation purification method, the yield increases by 57.4%. This method is essential for further applications in drug delivery and photothermal therapy.
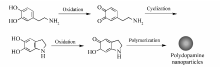
儿茶酚类化合物广泛存在于自然界中,其结构中的儿茶酚基团具有多种功能,如较强的氧化还原性、pH响应性和显著的金属离子螯合性[1]。 在种类繁多的儿茶酚类化合物中,最具有代表性的便是多巴胺(4-(2-乙胺基)苯-1,2-二酚)。 多巴胺是一种生物神经递质,在溶解氧的水溶液中,多巴胺的邻苯二酚基团很容易发生氧化,生成具有邻苯二醌结构的多巴胺醌化合物。 多巴胺和多巴胺醌之间发生反歧化反应,产生半醌自由基,然后偶合成交联键,并形成致密的交联网络结构的交联复合层[2,3,4]。 当基材存在时,多巴胺便会自聚形成强力附着于材料表面的聚多巴胺复合薄层[5,6,7,8]。 多巴胺不仅可以在固体材料表面形成牢固黏附的涂层,还可通过自身组装形成纳米粒子[9]。 聚多巴胺具有良好的粘附性、水分散性、生物相容性和稳定性[10,11],在紫外线防护、抗菌、温度调节、自由基消除等领域被认为有潜在的应用[12,13,14,15]。
近年来,随着纳米科技的发展,聚多巴胺纳米粒子已经迅速地被纳入化学、生物、医学和智能材料等研究领域,在药物运输、光热治疗、生物分子固定、骨和组织工程应用、分子印刷技术、细胞粘附和图案化和抗菌应用等领域展现了广泛的应用前景[16,17,18,19,20]。 聚多巴胺纳米粒子多采用溶液氧化法制备[20],得到的是含有聚多巴胺纳米粒子的混合液,需进一步进行分离提纯。 目前,报道的聚多巴胺纳米粒子的提纯方法均为超速离心法。 但是,超速离心法对离心设备要求很高,且效率差、产率低,只适用于微量实验研究。 此外,超速离心法可能会引起聚多巴胺纳米粒子的不可逆聚集,导致纳米粒子的储存稳定性较差。 因此,开发一种更简单、高效的聚多巴胺纳米粒子提纯方法十分必要。
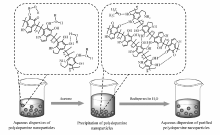
本文利用沉淀法对聚多巴胺纳米粒子进行高效提纯。 首先,利用溶液氧化法制备了分散在水/乙醇中的聚多巴胺纳米粒子(Scheme 1),然后向分散液中逐滴加入丙酮使聚多巴胺纳米粒子絮凝。收集沉降物,用丙酮冲洗并干燥后,加水重新分散得到纯化的聚多巴胺纳米粒子水分散液(Scheme 2)。 对聚多巴胺纳米粒子的结构、形貌和尺寸等进行了表征,对丙酮沉淀提纯法的效果进行了研究。
盐酸多巴胺(≥98%)购自阿拉丁试剂(上海)有限公司;氨水、乙醇、丙酮、盐酸均购自国药基团化学试剂有限公司,均为分析纯试剂。
UV1902-Ⅱ型紫外-可见分光光度仪(UV-Vis,北京瑞利分析仪器公司);Sorvall ST 16R型超速离心机(上海赛默飞世尔科技(中国)公司);SU8220型场发射扫描电子显微镜(FESEN,日本日立株式会社);JEM-2100plus型透射电子显微镜(TEM,日本电子株式会社);ALV/DLS/SLS-5022F型动态光散射仪(DLS,德国HOSIC LIMITED公司);MDL-Ⅲ-808-2W型激光器(长春新产业光电技术有限公司)。
采用溶液氧化法制备聚多巴胺纳米粒子[21]。 在250 mL圆底烧瓶中加入2 mL氨水(质量分数为28%~30%)、40 mL无水乙醇和90 mL超纯水,常温搅拌30 min。 将盐酸多巴胺溶液(质量浓度0.05 g/mL)溶液快速加入到上述溶液中,敞口反应24 h制得聚多巴胺纳米粒子分散液。
取2 mL聚多巴胺纳米粒子分散液,在快速搅拌状态下,将丙酮(2、4、8或16 mL)缓慢滴入,滴加完毕后静置沉降。 沉降10 min后,低速离心(500 r/min,5 min)收集沉淀物,移除上清液,沉淀物用丙酮洗涤3次并自然干燥后,重新分散于2 mL超纯水中保存。
设置对照组实验,采用传统的超速离心法提纯[21]。 取2 mL聚多巴胺纳米粒子分散液,在15000 r/min的转速下离心20 min,移除上清液,将沉淀物重新分散在2 mL超纯水中保存。
取聚多巴胺纳米粒子水分散液(质量浓度为0.3 g/L)和去离子水各1.5 mL,激光照射6 min。 在激光照射的过程中,每隔1 min用温度探头测定溶液温度。
沉淀法是常用的纳米粒子提纯方法之一,是通过向纳米粒子分散液中加入极性相反的溶剂,利用溶液极性的改变使纳米粒子絮凝并沉淀,从而达到提纯的目的。 通过溶液氧化法制备的聚多巴胺纳米粒子分散液,其分散介质为水和乙醇,聚多巴胺纳米粒子主要通过与水分子的氢键作用而稳定分散在溶液中。 经过筛选,本文采用丙酮作为反溶剂,丙酮可以与水互溶,极性适中,通过调节加入量可以有效调控溶液的极性,从而达到最佳的沉淀效果。图1为向2 mL聚多巴胺纳米粒子分散液中分别加入2、4、8和16 mL丙酮后的沉淀效果照片。 可以看到,当 V(分散液): V(丙酮)=1:1时(图1A),溶液并未发生肉眼可辨识的变化,静置24 h之后仍未观察到明显的沉淀效果。 而当 V(分散液): V(丙酮)=1:2时(图1B),聚多巴胺纳米粒子发生快速且明显的絮凝,静置24 h之后基本实现完全沉降。 进一步提高丙酮的加入量至 V(分散液): V(丙酮)=1:4(图1C)和1:8(图1D),沉淀效果更加明显,1 min后就可以看到清晰的沉降分层,且上清液基本澄清透明,这说明丙酮沉淀法可以实现聚多巴胺纳米粒子的高效沉淀。 我们推测丙酮的加入极大抑制了聚多巴胺纳米粒子与水分子的氢键作用,而转变为聚多巴胺纳米粒子与丙酮分子、聚多巴胺纳米粒子之间的氢键作用,从而引起了聚多巴胺纳米粒子之间的絮凝及沉淀。 同时,从图1中可以看出,聚多巴胺纳米粒子完全沉降后,上清液仍呈现浅棕色,说明丙酮的加入不会将溶液中的副产物一起沉淀下来,从而实现聚多巴胺纳米粒子的分离与提纯。
 | 图1 V(分散液): V(丙酮)=1:1(A)、1:2(B)、1:4(C)和1:8(D)的聚多巴胺纳米粒子沉淀效果图Fig.1 Images of precipitation effect of polydopamine nanoparticles V(dispersion liquid): V(acetone)=1:1(A), 1:2(B), 1:4(C)and 1:8(D) |
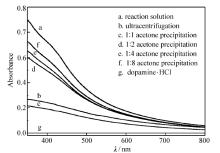
进一步利用紫外-可见吸收光谱对丙酮加入量与沉淀效率的关系进行了定量分析。 为了提高操作效率,缩短提纯的时间,采用了低速离心的方法来辅助收集沉淀物。 另外,为了完全除去副产物,继续用丙酮充分洗涤沉淀物,然后自然干燥挥发丙酮,最终将沉淀物重新分散在超纯水中,得到充分提纯的聚多巴胺纳米粒子水分散液。图2是不同丙酮加入量沉淀提纯的聚多巴胺纳米粒子水分散液的紫外-可见吸收光谱,提纯前和超速离心法提纯的聚多巴胺纳米粒子水分散液用作对比组。 通过吸收峰强度的对比可以看出,增加丙酮加入量可以提高聚多巴胺纳米粒子的提纯效率,且 V(分散液): V(丙酮)=1:2时,丙酮沉淀法的提纯效率明显高于超速离心法。 由于只有聚多巴胺纳米粒子在可见光区有吸收,所以可以利用提纯前后聚多巴胺纳米粒子分散液在可见光区吸收强度的比值计算其产率。 考虑到聚多巴胺纳米粒子分散液在400 nm处吸收强度适中,所以采用各个样品在400 nm处的吸收强度来计算产率,超速离心法的产率为33.4%, V(分散液): V(丙酮)为1:1、1:2、1:4和1:8时的产率分别为26.3%、68.3%、73.0%、81.2%,采用丙酮沉淀法的产率最高可以达到81.2%。
纳米材料的尺寸效应直接影响其性能及后续应用,所以在提纯过程中要避免纳米材料发生不可逆聚集,使其尺寸在提纯前后保持一致。 因此,对丙酮沉淀法提纯得到的聚多巴胺纳米粒子的形貌及粒径进行了表征。 首先,利用SEM和TEM对丙酮沉淀法和超速离心法提纯得到的聚多巴胺纳米粒子的形貌特征进行了观察,其结果见图3。 可以看到,两种提纯方法均得到形貌规整的聚多巴胺纳米粒子,但其粒径均一性和分散状态有所差别。 丙酮沉淀法提纯的聚多巴胺纳米粒子(图3A和3C)具有较好的粒子分散性,未观察到团聚现象,对图3A中聚多巴胺纳米粒子的大小进行统计分析,其粒径为(231.5±17.4) nm。 而用超速离心方法提纯得到的聚多巴胺纳米粒子(图3B和3D)明显团聚在一起,形成致密堆积状态,对图3B中未团聚的聚多巴胺纳米粒子的大小进行统计分析,其粒径为(224.3±20.9) nm。 造成这一现象的原因可能是丙酮沉淀法条件温和,通过削弱聚多巴胺纳米粒子与水分子的氢键作用而形成较松散的絮凝物,所以可较容易地重新分散在水溶液中。 而超速离心方法依赖于较强离心力,可能会使聚多巴胺纳米粒子在离心过程中形成较紧密的沉淀物,重新分散在水中时稳定性较差,造成SEM和TEM样品制备时容易再次发生团聚,且粒径受到离心力影响,相比较丙酮离心法得到的粒子偏小。
为了验证这种推测,进一步利用动态光散射对两种提纯方法得到的聚多巴胺纳米粒子分散液进行表征,结果如图4所示。 丙酮沉淀法提纯得到的聚多巴胺纳米粒子的平均流体力学半径均为~125 nm,且分布较窄。但是超速离心法提纯得到的聚多巴胺纳米粒子粒径明显分布较宽,粒径均一性较差,很可能是部分聚多巴胺纳米粒子发生了聚集,这与SEM和TEM观测的结果相符。
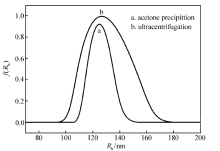 | 图4 聚多巴胺纳米粒子的DLS粒径分布图Fig.4 Average size distributions of polydopamine nanoparticles estimated by dynamic light scattering |
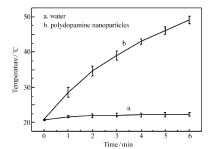
聚多巴胺纳米粒子在近红外光区有较强的吸收,且具有良好的光热转化效率和光稳定性,作为一种新颖的光热治疗(PTT)试剂,在肿瘤的光热治疗领域有较好的应用前景[17,18,21,22]。 为了探究丙酮沉淀法提纯得到的纳米粒子的光热效应,对提纯后的聚多巴胺纳米粒子水溶液进行激光照射,其光热性能如图5所示。 由图5可知,制备的聚多巴胺纳米粒子分散液在激光照射6 min后,其温度升高了28.2 ℃,而作为对比的去离子水在激光的照射下其温度并未发生明显的变化,可见采用丙酮沉淀方法提纯后的聚多巴胺纳米粒子仍可保持良好的光热效应。
利用丙酮沉淀法实现了聚多巴胺纳米粒子的高效提纯。与传统的超速离心提纯法相比,丙酮沉淀提纯法操作简单、效率更高,且得到的聚多巴胺纳米粒子的稳定性更好,且粒子偏差较小,同时保持较好的光热性能。丙酮沉淀法可以用于大批量聚多巴胺纳米粒子的高效制备,制备得到的聚多巴胺纳米粒子在药物载体及光热治疗等方面的应用研究正在进行中。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|