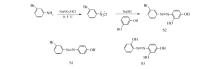
设计合成了3个含酚羟基数量不同的偶氮苯化合物S1、S2和S3作为传感分子,研究S1、S2和S3对阴离子的比色识别,并探讨传感分子的结构与识别阴离子能力之间的联系。 结果表明:传感分子S1、S2和S3对F-、H2P
Three colorimetric sensors S1, S2 and S3 based on azobenzene containing different numbers of active phenolic hydroxyl groups have been designed and synthesized. The sensors in CH3CN exhibit high sensitivity toward F-, H2P
阴离子在许多生物过程中起着重要作用,例如传递基因信息的DNA与腺苷三磷酸(ATP,Adenosine Triphosphate)、具有催化作用的酶与底物或辅酶之间的相互作用都涉及到阴离子的聚集和识别过程[1,2,3,4,5,6,7]。 一些阴离子的大量存在会对环境造成污染,例如磷酸盐肥料的过度使用会引起水质的富氧化污染,以及由硝酸盐代谢而引起的致癌作用。 又如醋酸根阴离子在血液中起调节pH值、稳定酸度的作用,其在人体内含量过高,超过人体自身代谢能力,在临床上常发生恶心、疲倦和肌肉痛性痉挛等不良反应。 氟与牙齿、骨骼组织的代谢密切相关,可以避免龋齿的发生,但过量的氟会造成氟中毒[8,9,10,11,12,13,14]。 由于阴离子在环境、医学和生命科学中发挥非常重要的作用,因此,设计和合成选择性的阴离子化学传感器对阴离子的检测、富集和治理具有重要的意义和广泛的应用前景[15,16,17]。
阴离子化学传感器的传感分子与阴离子间的识别主要通过疏水作用、氢键作用、偶极作用及配位作用等,其中氢键的作用尤为重要,如脲、硫脲、胺、酰胺、胍、吡咯和偶氮等化合物通过氢键与阴离子形成结合物而达到识别[18,19,20,21,22],比色化学传感器是以紫外可见吸收光谱的变化为输出信号,往往可以借助颜色的变化直接用裸眼观察就可以达到识别目的,比色识别因直观、检测操作简便快捷,无需借助复杂昂贵的化学测试仪器而备受青睐[23,24,25,26,27,28,29,30,31,32,33,34,35,36,37,38,39,40]。
偶氮苯基态时可发生分子内电荷转移(ICT),这类分子具有较大的偶极矩,利用其对介质环境的敏感性可望发展一类高效的阴离子显色体系,其次,偶氮类化学传感分子合成条件温和,产率高,成为近年来化学传感器研究的热点之一[41,42,43,44,45],然而在前人工作中,研究化学传感分子结构与识别阴离子能力之间的联系鲜有报道[46],因此,本论文利用廉价易得的原料,通过简单的重氮偶合反应,合成了3个结构简单、含羟基数量不同的偶氮苯酚分子作为传感分子,探讨传感分子结构对阴离子识别能力影响,旨在为传感分子结构的设计提供一定理论指导。
Bruker-AR400型超导核磁共振仪(NMR,瑞士Bruker公司),CDCl3作溶剂,TMS为内标;Perkin Elmer 2400-Ⅱ型元素分析仪(美国珀金埃尔默公司);Thermo LCQ DECA XP MAX型质谱仪(MS,美国热电公司);Nicolet 6700型傅里叶变换红外光谱仪(FT-IR,美国热电公司);WR S-2A型微机熔点仪(上海精密科学仪器公司);UV-3600型紫外-可见-近红外分光光度计(UV-Vis-NIR,日本岛津公司)。 间苯二酚、邻氨基苯酚、苯酚(分析纯,国药集团试剂公司),3-溴苯胺、四丁基铵盐阴离子试剂(分析纯,阿拉丁试剂),乙腈、甲醇(色谱纯,阿拉丁试剂),其它试剂均为市售分析纯。
3'-溴-2,4-二羟基偶氮苯(S2)合成 100 mL烧杯中加入3-溴苯胺(6 mmol)和8 mL 20% HCl,在冰浴条件下向上述悬浊液中缓慢滴加NaNO2(6.6 mmol)水溶液,混合溶液由浑浊逐渐变澄清。 重氮反应结束后,加入适量尿素将过量亚硝酸消耗掉,再用醋酸钠固体调节体系pH=5,得澄清液置于冰水中备用。 间苯二酚(6 mmol)用pH≈11 NaOH水溶液溶解,接着缓慢滴加到重氮盐溶液中,控制体系pH值810,TLC跟踪反应至原料点消失后终止反应,抽滤得固体粗产物,粗产物柱层析得到目标化合物S2。 橙红色固体,产率72.1%;mp 156.6157.1 ℃;1H NMR(DMSO- d6,400 MHz), δ:6.38(s,1H,Ar—H),6.476.50(m,1H,Ar—H),7.477.51(t, J=8.8 Hz,1H,Ar—H),7.62(d, J=8.8 Hz,1H,Ar—H),7.67(d, J=8.8 Hz,1H,Ar—H),7.87(d, J=8.8 Hz,1H,Ar—H),8.09(s,1H,Ar—H),10.64(s,1H,OH),11.82(s,1H,OH);13C NMR(DMSO,100 MHz), δ:103.4,109.7,122.9,123.0,123.3,128.1,131.7,132.7,132.9,152.7,157.6,164.1;IR(KBr), σ/cm-1:3195(m),3056(w),1620(s),1584(m),1507(s),1480(s),1429(m),1238(s),1121(s);ESI-MS m/z:292.82([M+H]+);计算值(C12H9BrN2O2)/%:C 49.17,H 3.09,N 9.56;实测值/%:C 49.00,H 3.10,N 9.32。 合成路线见图1。
偶氮苯酚传感分子S1与S3按照文献[47,48]方法制备,S1收率75.8%,158.3159.9 ℃,文献值[47]55.3%,mp 158.0159.5 ℃。 S3收率85.2%,mp 203.7204.5 ℃,文献值[48]80.2%,mp 204.5204.9 ℃。
为研究传感分子S1、S2和S3对不同阴离子的响应情况,将传感分子S1、S2和S3配制成2.0×10-5 mol/L的CH3CN溶液,分别滴加5倍物质的量浓度为2×10-2 mol/L F-、Cl-、Br-、I-、HS
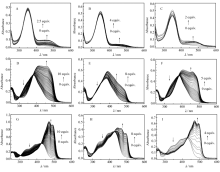
图3A是在S1-CH3CN溶液中逐渐加入F-引起S1的紫外可见吸收光谱的变化图。 未加入F-前,S1在波长为349 nm出现强吸收峰,加入F-后,400550 nm处出现新的吸收峰,随着加入F-浓度的增大,400550 nm吸收峰逐渐增高,溶液颜色明显加深,这是因为S1酚羟基与F-形成了氢键,该过程属于ICT 过程。 当加入H2P
当往传感分子与阴离子配合的CH3CN溶液中不断滴加少量质子溶剂甲醇,随着甲醇加入量增多,配合物吸收峰(400550 nm处)逐渐减弱(图4),溶液颜色逐渐变回传感分子溶液的颜色,表明了配合物的解离,这是甲醇与传感分子竞争结合阴离子所导致的,此现象说明传感分子与阴离子形成的配合物是通过氢键作用维系着的。
 | 图4 S3(2×10-5 mol/L)与4倍物质的量F-在CH3CN溶液中的CH3OH滴定紫外曲线图2.3 结合比测定Fig.4 UV-Vis spectra of S3(2×10-5 mol/L) and 4 times the amount of F- in CH3CN upon titration with increasing amount of CH3OH |
紫外可见滴定的吸收光谱中出现数目不等的等吸收点,表明传感分子和阴离子之间生成了具有确定化学计量比的配合物。 采用等摩尔连续变化法,控制受体和阴离子的总浓度为100 μmol/L,测定其紫外可见吸收光谱,绘制Job's曲线。图5是S2与F-的Job's曲线图,紫外可见最大吸收值在最大摩尔分数比对应的值为0.5处,表明S2与F-形成化学计量比为1:1的配合物。 S1、S2和S3与F-形成的配合物化学计量比分别为1:1、1:1和1:2,S1、S2和S3与AcO-形成的配合物化学计量比分别为2:1、1:1和2:3,S1、S2和S3与H2P
-'>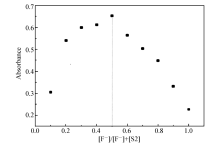 | 图5 传感分子S2与F-的Job's曲线2.4 结合常数测定Fig.5 Job's plot for the evolution of binding stoichiometry between S2 and F- |
传感分子与阴离子结合程度决定着传感分子对阴离子的识别能力强弱,为了进一步研究传感分子S1、S2和S3与F-、H2P
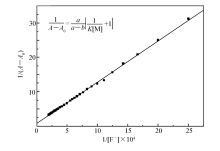 | 图6 CH3CN中S2与F-作用469 nm处吸收值变化Benesi-Hilderbrand图Fig.6 Benesi-Hilderbrand plot of S2 binding with F- associated with absorbance change at 469 nm in CH3CN |
由表1各配合物的结合常数可得出以下规律及其结论:
| 表1 S1、S2和S3与F-、H2P |
1)同一传感分子与不同阴离子的结合能力表现为:S1与不同阴离子结合能力顺序为F-≫H2P
2)相同阴离子与不同传感分子结合能力差异表现为:当阴离子为F-时,S1、S2和S3与它的结合常数为同一数量级,传感分子对F-识别能力顺序是S3>S2>S1。 当阴离子为H2P
总之,传感分子S1、S2和S3对阴离子F-、H2P
CH3CN溶液中S1、S2和S3的F-、H2P
| 表2 CH3CN溶液中S1、S2和S3对F-、H2P |
为研究传感器传感分子与阴离子的作用机理,通过核磁滴定考察了传感分子在DMSO- d6溶液中与阴离子作用后发生氢谱信号的变化。 以F-滴定传感分子S3与为例,当滴加少量的F-时,F-与传感分子S3通过氢键结合,Ha、Hb和Hc3个氢的化学位移峰强度减弱。 随着滴入F-的量增加,传感分子S3的Ha、Hb和Hc发生了去质子化,导致Ha、Hb和Hc3个峰消失,继续滴加F-至4.0倍物质的量时,在 δ 16.3处出现S3分子去质子化产生了H
 | 图7 S3(2×10-2 mol/L) DMSO- d6溶液中滴加不同量F-的1H NMR图Fig.7 1H NMR spectra of sensing molecule S3 in DMSO- d6(2×10-2 mol/L) upon addition of different amounts of F- |
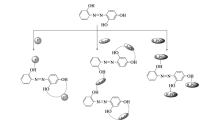
核磁滴定实验表明,在F-浓度较低时,S3与F-通过氢键作用相结合,高浓度时,由于氟离子的电负性较大,则发生质子化过程。 当向传感分子S3溶液滴加入低浓度F-时,F-先与S3的酚羟基通过氢键作用相结合,一分子F-与同一苯环上互为间位两个O—H氢键作用形成六元环,另一分子F-与另一苯环上O—H形成氢键,形成摩尔比1:2的配合物,随着F-量的增加,S3上3个活泼氢发生去质子,并有H
设计合成了3个结构简单、含羟基数量不同的偶氮苯化合物S1、S2和S3,以它们作为传感分子对F-、Cl-、Br-、I-、HS
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|
| [49] |
|
| [50] |
|
| [51] |
|