共同通讯联系人:王新海,教授; Tel:0371-23259385; Fax:0371-23881589; E-mail:xinhaiwang@126.com; 研究方向:水污染控制
纤维素作为可再生资源,其催化水解得到的平台化合物对缓解能源压力具有重要的意义。 本文以生物质竹子为原料选择700 ℃预碳化、150 ℃磺化得到的固体炭磺酸为基体,负载1-丁基-3-甲基咪唑氯后得到离子液体功能化固体炭磺酸催化剂。 结果表明,催化剂最优条件下水解纤维素得到的总还原糖产率相对于固体炭磺酸提升了15.2%,循环使用后,依然表现出良好的催化性能。
Co-corresponding author:WANGXinhai, professor; Tel:0371-23259385; Fax:0371-23881589; E-mail:xinhaiwang@126.com; Research interests:water pollution control
Cellulose is a renewable resource. Compounds obtained by the hydrolysis of cellulose are of great significance to ease the energy pressure. Herein, the hydrolysis of cellulose catalyzed by solid carbon sulfonic acid supported 1-butyl-3-methylimidazolium chloride is reported. The solid carbon sulfonic acid obtained from bamboo biomass by pre-carbonization at 700 ℃ and sulfonation at 150 ℃ was used as the matrix. Ionic liquid functionalized solid carbon sulfonic acid catalyst was obtained by loading 1-butyl-3-methylimidazolium chloride. The results show that the total reducing sugar yield under optimal conditions is increased by 15.2% relative to the total reducing sugar yield by exploiting solid carbon sulfonic acid. The catalyst still exhibits good performance after recycling.
随着化石能源日益枯竭以及环境问题的突出,利用生物质资源替代不可再生能源变得尤为重要[1,2,3]。 纤维素作为自然界中最丰富的可再生资源之一,占生物质的35%~50%,是植物纤维的主要成分。 而纤维素水解所得到的葡萄糖及其它产物,则可以作为平台化合物转化为重要的化工原料和燃料。 因此,纤维素的转化和利用得到了广泛的关注[4,5,6]。
纤维素是由 D-吡喃葡萄糖分子通过 β-1,4糖苷键聚合形成的链状高分子化合物,如何将其降解成单糖或者低聚物是纤维素利用的关键。 目前,水解纤维素的方法主要有纤维素酶解法和传统酸水解法,但催化过程中均存在或多或少的不足[7]。 如纤维素酶水解效率较低、成本高;传统酸水解法对反应器腐蚀严重,产物与催化剂分离困难,催化剂回收再利用工艺复杂等问题。 离子液体的应用,为纤维素水解提供了新的可行性途径,研究表明离子液体能够与纤维素上的羟基形成氢键破坏其分子内和分子间氢键达到溶解纤维素的目的[8,9],功能化的离子液体还可以在特定条件下水解纤维素并表现出良好的催化性能,不同的产物均可以达到理想的收率[10,11,12,13]。 然而,以离子液体作为催化剂,不但成本高,且粘度大、难分离,在实际的工业应用上受到严重的制约。 Hara等[14]首次报道了利用固体酸催化剂将微晶纤维素(MCC)降解为可溶性糖,随后竹子[15]、玉米秸秆[16]、柳枝[17]等生物质被尝试用作制备催化剂的原料,经炭化、磺化后制得表面含有—SO3H、—COOH和—OH官能团的固体炭磺酸[18]。 在水解过程中,—COOH和—OH作为催化剂的结合域[19],—SO3H作为催化剂的催化域,共同作用有效地促进纤维素分子中 β-1,4糖苷键断裂,将纤维素降解为葡萄糖单糖以及可溶性低聚物[20]。 但是,固体炭磺酸表面较低的—COOH和—OH含量,降低了其与纤维素的结合能力,限制了纤维素的转化。 如何提高固体炭磺酸催化剂与纤维素的结合能力,是促进纤维素水解的关键。
本文以竹子为原料,经不同温度预炭化、磺化得到不同的固体炭磺酸,通过优化水解条件实验选取出最优前驱体,负载1-丁基-3-甲基咪唑氯([BMIM]Cl)后得到离子液体(IL)功能化的固体炭磺酸催化剂。 考察了反应时间、反应温度等因素对催化剂活性的影响。
实验所用竹子为多年生毛竹取自于开封竹器加工厂废弃材料,粉碎过筛(900 μm)后充分干燥。 微晶纤维素(MCC,平均粒径50 μm)购买于美国SIGMA公司,[BMIM]Cl(99%)购于河南利华制药有限公司。 葡萄糖,98%浓硫酸,氯化钡,3,5-二硝基水杨酸,酒石酸钾钠,苯酚,无水亚硫酸钠,氢氧化钠等试剂均为市售分析纯;若无特殊说明,实验用水均为蒸馏水。
Nova NanoSEM 450型场发射扫描电子显微镜(SEM,美国FEI公司);JSM-7610F型场发射扫描电子显微镜(日本电子株式会社);Vertex70型傅里叶变换红外光谱仪(FT-IR,德国布鲁克光谱仪器公司);Bruker D8 Advance型X射线衍射(XRD,德国Bruker公司);Vario EL cube型元素分析仪(德国Elementar元素分析系统公司);UV-1750型紫外-可见分光光度计(UV-Vis,日本岛津);Agilent1260型高效液相色谱仪(HPLC,安捷伦科技(中国)股份有限公司);差示热重分析仪(DTG,瑞士METTLER TOLEDO公司)。
取竹粉30 g放入管式炉中,在N2气保护下以5 ℃/min分别升温至300、400、500和700 ℃,保持2 h,自然冷却到室温,然后用大量水冲洗去除灰分,干燥后所得竹炭命名为BB n(n=3、4、5和7分别代表相应的处理温度)。
将4 g BB n和50 mL浓硫酸加入到100 mL三口烧瓶,N2气保护下于油浴锅中150 ℃加热搅拌13 h,反应结束后自然冷却至室温。 用大量去离子水(>80 ℃)过滤冲洗所得固体,直至滤出液为中性,并用饱和BaCl2检测滤液中无沉淀产生。 80 ℃干燥12 h,得固体炭磺酸BB n-S。
取0.5 g BB n-S和50 mL 100 mmol/L的[BMIM]Cl溶液加入100 mL的锥形瓶内,将锥形瓶放入恒温振荡箱,在25 ℃下以200 r/min的转速震荡48 h后,采用高速离心机使固液分离。 将负载离子液体的炭磺酸在80 ℃下干燥12 h得到本实验催化剂,命名为BB n-S-IL。
催化剂表面—SO3H的量采用酸碱中和滴定法测定[21]。 称取催化剂0.1 g和20 mL饱和氯化钠溶液于锥形瓶中,25 ℃超声1 h,使催化剂中的H+于Na+发生质子交换。 超声结束后将混合液固液分离,滤液以酚酞为指示剂,用0.01 mol/L的NaOH溶液滴定,滴定实验平行3次取平均值。
催化剂负载[BMIM]Cl的量采用紫外分光光度法测量,在211 nm处测[BMIM]Cl的吸光度,利用标准曲线法计算催化剂的[BMIM]Cl负载量;多次循环后催化剂[BMIM]Cl的负载量采用高效液相色谱法测量(流动相为水:甲醇(体积比95:5),波长设置为211 nm,流速为0.5 mL/min,Zorbax SB-C18柱子)利用标准曲线法计算循环后催化剂的[BMIM]Cl负载量。
50 mg MCC和50 mg催化剂加入25 mL聚四氟乙烯反应釜中,加入5 mL水搅拌均匀,之后将反应釜置于真空干燥箱内,在不同时间和温度的水解反应完成后,自然冷却至室温,最后离心分离(5000 r/min,5 min),取上清液进行产物分析。 水解产物中总还原糖(Total Reducing Sugar,TRS)含量用3,5-二硝基水杨酸(DNS)法测定[22,23],底物用水多次洗涤分离后干燥,称量得到反应底物质量,与原反应中催化剂和MCC的质量对比,投加相差质量的MCC进行催化剂的重复性实验。
DNS试剂制备 18.2 g酒石酸钾钠溶于50 mL热水中,加入0.639 g的3,5-二硝基水杨酸和2.097 g氢氧化钠,再加入0.5 g苯酚和0.5 g无水亚硫酸钠,加热搅拌使其完全溶解,冷却后定容至100 mL,转移至棕色试剂瓶中,阴暗处放置7 d后使用。 TRS得率( Y)可由式(1)计算得出。
式中, mTRS为DNS法测得的总还原糖质量(mg), mt为纤维素总质量(mg)。
不同温度的生物质经炭化后,表面出现微米大小的贯通状孔洞,而且温度愈高,竹子炭化程度愈高,孔道愈明显。 磺化后的形貌与磺化之前的生物质炭相比孔道结构以及形貌未发生明显变化(见辅助材料图S1)。 辅助材料图S2A为BB n-S的红外光谱图,1650 cm-1处为—COOH基团上C=O键的伸缩振动吸收峰,1160和1036 cm-1为—SO3H基团上O=S=O键的对称和反对称伸缩振动。 这说明—SO3H成功地接枝在生物质炭上,BB n-S已经成功合成。
图1A、1B和1C分别为700 ℃炭化的生物质炭以及其磺化后和磺化并负载离子液体的SEM照片。 从图中可以看出,700 ℃炭化的生物质具有较大的孔道结构,磺化以及负载离子液体后并没有使孔道崩塌改变生物质炭形貌;图1D为700 ℃炭化时BB7、BB7-S和BB7-S-IL的X射线衍图谱,3种物质均存在2 θ=24°的较强峰以及2 θ为43°的较弱峰,分别为碳的002面和004面的衍射峰,说明固体材料为芳香结构的无定形炭材料,进一步证明负载离子液体未改生物质炭的形貌结构。 N、S、Cl元素均匀存在BB7-S-IL的表面(见辅助材料图S2B),而且通过表1的元素分析可以看到,BB7-S和BB7-S-IL中S元素的质量分数相对于BB7明显增加,BB7-S-IL的N元素含量也远远高于BB7和BB7-S,因此证实了BB7引入了—SO3H官能团并成功负载了[BMIM]Cl。
| 表1 催化剂中的元素分析 Table 1 Elemental analysis for the catalyst |
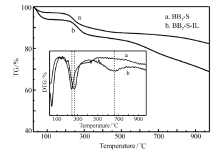
图2为700 ℃炭化制备的固体磺酸和催化剂的热重分析曲线。 从TG图中可以明显观察到BB7-S和BB7-S-IL均有3个主要的失重峰,第1个失重峰出现在90~120℃范围内,归属于材料中存在的水分蒸发和吸附气体的析出,第2个失重峰出现在230~260 ℃,第3个失重峰出现在700 ℃之后,与固体炭磺酸相比,BB7-S-IL的失重峰相对滞后,而且DTG图中催化剂BB7-S-IL的最大失重速率出现时的温度也滞后于固体炭磺酸。 综上所述,两种物质在200 ℃前均有较好的热稳定性,而且在300 ℃前BB7-S-IL的热稳定性优于BB7-S。
2.2.1 催化剂的选择
如图3A所示考察了相同时间内BB n-S在不同温度下对TRS产率的影响。 在60 ℃时几乎检测不到TRS,这可能是较低的温度和压力未能有效降低催化剂的活化能,致使催化剂难以破坏纤维素的 β-1,4糖苷键,未能有效水解纤维素。 当升温至150 ℃时,反应体系中的催化剂活化能的降低能够有效地作用于更加分散的MCC,使得TRS的产率呈现出明显的上升趋势。 继续升温至180 ℃,TRS得率上升趋于平缓,这可能是由于还原糖在较高温度下不稳定,易于转化为其他副产物。 考虑到能源消耗以及其可能的经济效益,选择150 ℃为最佳温度。在150 ℃下考察了BB n-S在不同时间对TRS产率的影响,如图3B所示,不同炭化温度得到的催化剂催化纤维素获得的TRS产率存在差异。 在20 h之前,BB3-S水解产率较高,可能原因是300 ℃炭化所得的固体磺酸中—SO3H官能团含量较高(见辅助材料表S1),20 h之后BB7-S表现出较好的水解纤维素的能力,得益于其较高的炭化温度造成的大孔道结构更利于纤维素进入孔道结构中与催化剂更有效的接触。 反应时间从10 h增加至24 h过程中,还原糖的产率随反应时间延长而增加;继续增加反应时间至48 h,TRS产率基本趋于平稳,出现增长的“平台期”,而且不同催化剂表现出相同的规律。 综上,BB7-S为最佳的水解纤维素的催化剂,因此选择BB7-S作为负载[BMIM]Cl的优良前体。 而且通过比较BB7与BB7-S在150 ℃条件下反应24 h得到的TRS产率(见辅助材料图S3)证明—HSO3对于纤维素水解中起着至关重要的作用。
 | 图3 BB n-S在不同温度(A)和时间(B)催化纤维素水解产物中的总还原糖(TRS)产率Fig.3 Total reduced sugar(TRS) yields of hydrolysis products of cellulose catalyzed by BB n-S at different temperature(A) and time(B) |
2.2.2 BB7-S-IL反应条件优化
BB7-S-IL的TRS产率在不同温度下反应24 h,TRS产率变化如图4A所示,升高温度有利于降低BB7-S-IL催化剂的活化能,120 ℃至150 ℃增长迅速,继续升温TRS产率上升趋于平缓。 考虑到高温不利于TRS的稳定,且继续升温不符合实际应用中纤维素转化的经济效益,因此将150 ℃设定为最佳反应温度。 而且负载[BMIM]Cl后TRS产率有所提升。
150 ℃下不同反应时间对TRS产率的影响如图4B所示。 在28 h之前,随反应时间的增长,两种催化剂BB7-S和BB7-S-IL的TRS产率均呈现明显的上升趋势;28 h之后两种催化剂的TRS产率无明显上升。 考虑到工业应用前景,时间愈长成本愈高,因此选择28 h为最佳催化反应时间。 在反应的各个阶段BB7-S-IL的TRS产率一直优于BB7-S,得益于负载的[BMIM]Cl能够与纤维素之间形成氢键,使得纤维素长链更易于接近催化点位,并与固体炭磺酸协同促进纤维素的水解,从而获得更高的TRS产率。 相对于BB7-S,BB7-S-IL在最佳反应时间下的TRS产率提升了15.2%。
2.2.3 BB7-S-IL的循环稳定性
本文在反应温度为150 ℃,反应时间28 h,考察了BB7-S-IL循环利用性能。 结果如图5A所示,首次循环后BB7-S-IL的TRS的得率为21.42%,与新鲜催化剂相比有所下降。 循环至第3次时,TRS得率继续下降至18.12%,循环使用至第4次TRS产率明显下降,通过检测反应前后BB7-S-IL负载的—HSO3和[BMIM]Cl的含量(图5B)发现,随着循环次数增多催化剂负载—HSO3和[BMIM]Cl的量均呈现下降的趋势。 综上所述,—HSO3和[BMIM]Cl均对催化剂的活性降低有一定的影响。 多次循环后催化剂仍表现出一定的催化活性并易与产物分离。
本文以生物质为原料合成了一系列的生物质炭磺酸催化剂,通过对比催化实验我们选取700 ℃得到的固体炭磺酸BB7-S为前驱体,通过常温下的恒温震荡负载[BMIM]Cl离子液体(IL)合成了BB7-S-IL,有效提高了总还原糖(TRS)的产率。 在150 ℃、28 h的最佳条件下负载的[BMIM]Cl与固体炭磺酸协同作用相对于单独的固体炭磺酸提升了15.2%的TRS产率。 所用的催化剂合成制备简单,与单纯用离子液体或固体炭磺酸催化剂相比,不但可大幅度降低离子液体的用量,提高水解效率,更为农林生物质资源的进一步开发利用提供了一条新的途径。
辅助材料(Supporting Information)[样品SEM照片、部分样品元素分布、FT-IR谱图、产率和—SO3H含量数据]可以免费从本刊网站(http://yyhx.ciac.jl.cn/)下载。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|