采用简便的抽滤装置制备了三明治结构的不同粒径大小的二氧化锡(SnO2)/石墨烯柔性薄膜电极,通过X射线衍射(XRD)、扫描电子显微镜(SEM)、透射电子显微镜(TEM)、原子力显微镜(AFM)、比表面积(BET)和电化学等测试技术手段对样品结构、形貌和电化学性能进行表征,研究了二氧化锡颗粒大小对复合电极电化学性能的影响。 结果表明,当SnO2纳米颗粒的粒径为6 nm时柔性复合电极表现出最优的电化学性能,在100 mA/g的电流密度下经过100次循环后,可逆比容量保持在555 mA·h/g,远高于纯SnO2和粒径过大或过小的SnO2/石墨烯复合电极。
Flexible free-standing tin oxide(SnO2) nanoparticles with different particle size/graphene sandwich paper electrodes were fabricated via a simple filtration method. The influence of SnO2 particle size on electrochemical performances was investigated by X-ray diffraction(XRD), scanning electron microscopy(SEM), transmission electronic microscopy(TEM), Brunauer, atomic force microscope(AFM), Emmett and Teller analysis(BET) and electrochemical measurements. The results show that the best electrochemical performance can be obtained when the particle size of nanoparticle is at 6 nm. When applied as an anode for lithium ion battery, an excellent cycling stability with a reversible capacity of 555 mA·h/g after 100 cycles at 100 mA/g is delivered, which is far superior to those of pristine SnO2 and the corresponding composites composed of larger or smaller particles than optimum.
随着科学技术的进步和人们生活水平的提高,电子产品朝着小型化、轻便和多样性方向发展。 其中,柔性的便携式和可穿戴电子产品,包括可卷屏手机和柔性智能手表等,成为研究热点之一。 为了满足柔性电子技术发展的需求,发展高能量密度的柔性锂离子电池是关键[1,2]。 由于二氧化锡(SnO2)具有价格低、安全性好、放电电势低和高的理论容量等优点,因此被认为是非常有希望的锂离子电池负极材料之一[3]。 但是在嵌-脱锂的反应过程中,SnO2体积发生巨大膨胀(高达300%),导致电极在反复充放电过程容易粉化和脱落,充放电循环性能差,限制了其应用[4]。
为了改善上述问题,人们通常采用减小颗粒尺寸的方法, 如将材料纳米化,以减少嵌锂与脱锂过程中的绝对体积膨胀,提高材料的可逆容量和改善材料的循环性能。 如Kim等[5]用三亚乙基二胺作为封端剂,采用水热法在不同温度下制备了结晶性非常好的粒径在3~8 nm的SnO2,电化学测试结果表明,在结晶性基本相同的情况下减小颗粒尺寸,其比容量和循环稳定性均有明显改善。可逆容量增高的原因是:随着颗粒尺寸的减小,锂离子插入的数目增多,锂离子的传输距离减小,电导率增加,从而提高了初始比容量和可逆比容量。
虽然通过减小SnO2尺寸可以在一定程度上改善其循环性能,但在循环过程中电极材料仍然容易团聚,发生粉化脱落,致使容量快速衰减,最后导致电极失效。 另一种有效的途径是通过在SnO2表面包覆其它物质以缓解充放电过程中产生的体积膨胀,碳材料是最常见的包覆材料,它既可以起到上述效果,还可以改善复合材料的电导率,进一步提高电化学性能,但常规碳材料的效果往往不够理想[6,7]。 石墨烯是一种新型二维碳材料,其电子导电率髙、且具有高柔韧性和高机械强度,易加工成薄膜,作为活性物质的基体可用于制备柔性电极材料[8,9]。 大量研究表明[10,11,12,13,14],SnO2与石墨烯复合可以大大改善其电化学性能,容量和循环稳定性方面均有显著提高,但是将SnO2分散于石墨烯片层间制备三明治结构石墨烯基柔性薄膜电极的报道很少。 Liang等[15]首次将石墨烯与60 nm的SnO2混合液体抽滤成石墨烯纸,可直接用作锂离子电池电极,即省却涂膜过程中使用导电乙炔黑和粘结剂,简化了涂膜工艺,又在一定程度上抑制了SnO2的体积膨胀和脱落问题,改善了SnO2的循环性能。但是由于使用的SnO2粒径较大,循环性能并不理想,在100 mA/g电流密度下循环50周,比容量仅剩438.5 mA·h/g。
虽然研究证明减小颗粒尺寸可以提高可逆容量和循环性能,但是如何选择合适粒径的小尺寸SnO2纳米颗粒与石墨烯纸复合制备柔性电极的研究还鲜有报道。 其中,Wang等[16]通过在石墨烯表面原位合成SnO2纳米颗粒,同时对石墨烯进行氮掺杂,制备了氮掺杂石墨烯/SnO2复合纸电极,其中SnO2的粒径为3.7 nm,在小电流密度(50 mA/g)下的循环稳定性有显著提高,但其并未报道粒径对复合纸电极电化学性能的影响。本文以石墨烯作为柔性基体,使用不同粒径SnO2作为活性材料,采用简便的抽滤、水热还原法制备柔性锂离子电池负极材料,并系统研究了SnO2粒径对复合电极材料形貌、结构以及储锂性能的影响。
四氯化锡(≥99.5%)购自成都市科龙化工试剂厂;氧化石墨烯(≥99.0%)购自常州第六元素材料科技股份有限公司;Ar气(≥99.999%)、无水乙醇(分析纯)购自成都市科龙化工试剂厂;实验用水为18.25 MΩ/cm的超纯水;六氟磷酸锂(LiPF6,≥97.0%)购自东莞市杉杉电池材料有限公司;60 nm SnO2(≥99.9%)购自阿拉丁试剂。
Smart Lab III型X射线衍射仪(XRD,日本Rigaku公司),Cu Kα辐射源,其波长 λ为0.15418 nm,扫描速度为10°/min,扫描范围5°~80°;Land-CT2001A型电池测试系统(武汉市蓝电电子股份有限公司);VMP3型电化学工作站(法国BIO-Logic公司);LS800S型手套箱(成都德力斯实业有限公司);FEI Inspect F型场发射扫描电子显微镜(SEM,美国Thermo Fisher Scientific公司);Tecnai G2 F20 S-TWIN型场发射透射电子显微镜(TEM,美国Philips-FEI公司)及能量色散谱仪(EDS,美国Philips-FEI公司);Nanoscope Ⅲa型原子力显微镜(AFM,美国Veeco公司)。
1.2.1 纳米SnO2的制备
3 nm SnO2制备[17] 首先将0.5 g SnCl4·5H2O溶于200 mL超纯水中,再加入5 mL双氧水(H2O2),搅拌均匀;然后用0.05 mol/L KOH溶液将溶液的pH值调至6,搅拌2 h,再冷冻干燥,380 ℃热处理3 h得到白色固体粉末。
6 nm SnO2制备[18] 将0.01 mol SnCl4·5H2O均匀分散于装有10 mL乙二醇的25 mL称量瓶中,然后置于含有10 mL氨水的100 mL聚四氟乙烯内衬中。 然后用不锈钢套将内衬密封,并置于已经设置好180 ℃的烘箱中,反应12 h。 待温度降为室温后,将复合产物离心脱水,并用水和乙醇洗3次,然后于40 ℃真空干燥。
1.2.2 SnO2/石墨烯薄膜的制备
氧化石墨烯(GO)溶液的制备 将GO粉末超声分散于超纯水中(频率40 kHz,功率 300 W),超声1 h。 然后将得到的溶液进行高速离心(10000 r/min)5 min,除去没有分散的杂质,得到黄褐色均匀的GO溶液待用,质量浓度为1 g/L。
SnO2/石墨烯薄膜的制备 首先将3 mg SnO2粉末分散于3 mL上述GO溶液中,超声1 h;然后将得到的混合液经过真空抽滤装置抽滤成SnO2/氧化石墨烯薄膜(GOSP),滤膜直径为50 mm,孔径0.2 μm。 待干燥后,将GOSP膜从滤膜剥离,然后220 ℃水热还原得到样品,标为GSP。 为了区别不同粒径纳米SnO2颗粒与石墨烯纸复合样品,定义其复合物名称为GSP- n, n代表SnO2颗粒的粒径,例如GSP-3表示3 nm的SnO2与石墨烯纸复合物。
按 m(SnO2粉末)∶ m(导电炭黑)∶ m(聚偏氟乙烯(PVDF))=8∶1∶1于玛瑙研钵中将混合物研磨混合均匀后,加入 N-甲基吡咯烷酮(NMP)研磨均匀,制得电极浆料,将其涂覆到铜箔上,在真空干燥箱中100 ℃干燥12 h。 使用专用模具冲切电极片,然后转移到充满Ar气的手套箱中,以金属锂片作为对电极、隔膜,六氟磷酸锂溶于 V(碳酸乙烯酯)∶ V(碳酸二甲酯)=1∶1混合溶剂配成的1 mol/L溶液为电解液,在手套箱中组装成CR2032型纽扣半电池。 釆用电池测试系统进行容量及循环性能的测试,工作电压范围0.01~3 V( vs.Li+/Li)。 循环伏安(CV)曲线和交流阻抗谱(EIS)测试在电化学工作站上进行:CV测试扫描电势范围0.01~3 V( vs.Li+/Li),扫描速率为0.1 mV/s。
图1为不同粒径大小纳米SnO2颗粒的XRD图谱。 由图1可见,商品化的60 nm SnO2的特征衍射峰非常尖锐,与四方金红石结构的SnO2标准谱图峰位一致(JCPDS标准卡片No.41-1445,空间群: P42 /mnm, a= b=0.47286 nm, c=0.31802 nm),其中2 θ=26.6°、33.9°、37.9°和51.8°的峰分别对应SnO2的(110)、(101)、(200)和(211)晶面。 而合成的另外两种SnO2与60 nm的SnO2特征衍射峰位置基本相同,表明它们晶体结构相同,但由于尺寸效应峰形明显变宽、峰强变弱。 通过Lorentz函数对26.6°的衍射峰进行拟合,得到衍射峰的半高宽,并根据谢乐公式分别计算出复合物中SnO2晶粒的平均尺寸约为3和6 nm。 通过BET对3种不同粒径的SnO2进行比表面积测试,购买的60 nm SnO2和合成的6 nm、3 nm SnO2的比表面积分别为7.1、166.5 和237 m2/g。
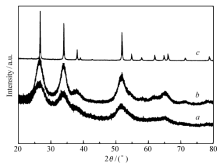 | 图1 不同粒径大小纳米SnO2颗粒的X射线衍射图谱Fig.1 X-ray diffraction patterns of purchased and synthesized SnO2 nanoparticles with different particle size a.3 nm; b.6 nm; c.60 nm |
 | 图2 合成的不同粒径纳米SnO2颗粒TEM照片( A, C)和高分辨TEM照片( B, D)Fig.2 TEM( A, C) and HRTEM( B, D) images of SnO2 nanoparticles with different particle size of 3 nm( A, B) and 6 nm( C, D) |
图2为合成的3和6 nm SnO2纳米颗粒的TEM照片。 从图2 A中可以看出,大部分3 nm SnO2以团聚的形式存在;而图2 C则显示6 nm SnO2分布更加均匀,只有局部出现轻微的团聚。 在高倍TEM照片(图2 B,2 D)中,可以清晰的看见SnO2的晶格条纹,表现出了较好的结晶性。
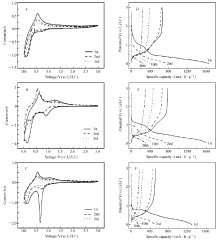
图3 A、3 C为不同粒径纳米SnO2的前3周循环CV曲线,电势扫描速率0.1 mV/s,电势扫描区间0.01~3 V。 一般认为,SnO2与锂反应按照合金型储锂机制,反应方程式如下[19]:
SnO2+4Li++4e-→Sn+2 Li2O (1)
Sn+ xLi++ xe-⇌ Li+ x Sn(O≤ x≤4.4) (2)
其中反应式(1)表示SnO2还原成金属Sn的不可逆反应[20],这种不可逆化学转变造成了大量初始容量损失。 反应式(2)表示Sn与Li之间可逆的合金化/去合金化过程,此过程贡献了电池的主要容量。 SnO2由于理论上1个Sn原子可对应存储4.4个Li原子,充放电过程中产生巨大的体积变化(300%)[4,21],在电极材料内部产生巨大内应力,从而引起电极粉化和脱落,导致容量迅速衰减。 如图3所示,对于60 nm SnO2(图3 C),首周还原曲线在0.75 V左右出现了一个强还原峰,但这个峰峰强从第2周明显减弱,对应SnO2表面固体电解质界面膜(SEI)的形成以及SnO2与Li+发生不可逆氧化还原反应生成Li2O和金属Sn的过程(反应式(1))[22]。 这两个反应电势接近,在CV曲线上重叠显示一个还原峰,它们也是SnO2首周库仑效率低的主要原因。 还原曲线上0.5~0.01 V电势区间出现的宽的还原峰,对应于生成Li xSn合金反应(反应式(2))。 当扫描转向时,在0.5 V左右的氧化峰对应Li xSn去合金化,而1.25 V左右的弱氧化峰为Li2O参与的部分氧化反应[23]。 当SnO2粒径减小时,不可逆反应对应的还原峰强度明显减弱(图3 A,3 B),尤其是3 nm SnO2在0.6 V左右的还原峰几乎完全消失,表明超细SnO2循环时只有少量Li2O副产物生成。 而同时6 nm SnO2在0.5 V/0.01 V的氧化还原电对峰明显增强,说明减小颗粒尺寸可增加比表面积,提供更多的电化学反应活性位置,有利于Li+的嵌入和脱出;但当颗粒尺寸进一步减小到3 nm时,该氧化还原峰对却有所减弱,这可能是由于:虽然作为非电化学活性物质的Li2O含量减少了,但缺少了其抑制电极材料粉化的媒介作用[23],SnO2纳米颗粒更易团聚;同时比表面积越大,与电解液副反应生成SEI膜增多,包裹SEI膜的纳米颗粒嵌在团聚体内,很难与Li+发生可逆反应。
图3 D和3 E为不同粒径纳米SnO2颗粒在电流密度为100 mA/g下的充放电曲线。 在首周放电过程中,3个样品在0.8 V左右均出现一个平台,但随粒径减小该平台容量明显减少,而后随着放电容量的继续增加,电压缓慢下降到截止电压0.01 V,3个样品首周充放电比容量和库仑效率如表1所示。 其中,6 nm SnO2的首周可逆容量和库仑效率均最高,这些均与CV测试结果一致。
| 表1 不同粒径纳米SnO2颗粒的首周充放电性质 Table 1 First charge and discharge properties of SnO2 nanoparticles with different particle size |
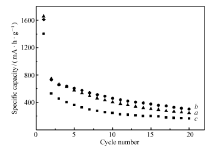
图4为不同粒径的纳米SnO2颗粒在电流密度为100 mA/g时的循环性能图。 很明显,纯SnO2的循环性能均较差,经过20次循环过后,3、6和60 nm的SnO2的比容量分别为246.1、303.8和164.5 mA·h/g。 对于3和6 nm的SnO2而言,一方面较小的颗粒可以在一定程度上抑制循环过程中的体积变化,同时颗粒减小也能够为锂离子提供相对较短的扩散路径,有利于循环的进行;另一方面,纳米材料作电极时,由于其比表面积大,在循环过程中易发生严重的电化学团聚,导致其循环性能下降。 因此,通过调控SnO2纳米颗粒尺寸可以在一定程度上优化其电化学性能。 综上所述,6 nm的SnO2表现出了相对较优的电化学性能。
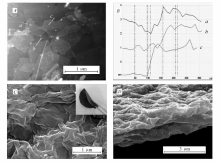
图5为氧化石墨烯(GO)的AFM图和通过抽滤和水热还原法制备的6 nm SnO2与石墨烯复合的纳米SnO2/石墨烯纸(GSP-6)的表面和断面SEM照片。 从图5 A可以清楚地看到大而薄的GO片层,其薄片尺寸~0.5~2 μm,厚度~2 nm(图5 B)。 GO片层尺寸远远大于本文选用的SnO2纳米颗粒(3~60 nm),层间可以很好的包覆和镶嵌大量SnO2颗粒,二者具有较好的尺寸匹配性,这也与后面SEM和TEM观测结果一致。 进一步通过仔细观察GSP样品表面(图5 C),未发现游离的SnO2颗粒,说明SnO2颗粒被包覆在石墨烯片层之间,其中的插图则展示了复合电极良好的柔软性和可折叠性。 样品的断面形貌(图5 D)呈现层状结构,隐约可见SnO2纳米颗粒均匀地分散在石墨烯片层间。 通过对GSP-6样品进行EDS分析,计算可知经过水热还原后样品中SnO2的质量分数约占60%,石墨烯的质量分数约为39.2%。
图6显示了不同粒径SnO2纳米颗粒与石墨烯复合制备GSP的TEM照片。 透射电子显微镜照片上我们首先可以清晰地看到石墨烯典型的褶皱结构。
 | 图6 不同粒径纳米SnO2颗粒与石墨烯复合制备GSP的TEM( A, C)和高分辨TEM( B, D)照片Fig.6 TEM( A, C) and HRTEM( B, D) images of GSP embedding SnO2nanoparticles with different particle size A, B.GSP-3; C, D.GSP-6 |
进一步观察,从图6 A和6 C可以看出,3 nm的SnO2团聚较为严重,而6 nm的SnO2较均匀地分布在石墨烯片层上,只有局部有轻微的团聚。 在高分辨TEM照片(图6 B和图6 D)中,虽然均可以看到SnO2的晶格条纹和边缘上石墨烯的层状结构,但由于GSP-3中的颗粒团聚更严重,相互重叠,其晶格条纹不如颗粒分散较好的GSP-6明显,这与2.1小节中纯SnO2的分散情况类似。
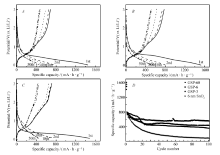
图7为不同粒径SnO2纳米颗粒与石墨烯复合制备GSP- n电极材料在100 mA/g的电流密度下的充放电曲线和循环性能图,充放电电压区间为0.01~3.0 V。如图所示,与纯SnO2的首周放电曲线相比(图3 D~3 F),GSP- n复合负极材料的首次放电曲线在0.8 V的平台均不明显,表明与石墨烯复合后SnO2生成Li2O副反应减少。 GSP-3、GSP-6和GSP-60电极的首周库仑效率分别为51.8%、56.3%和48%,较纯样均有大幅度提高,其中又以GSP-6的首周放电比容量和库仑效率最高;另外,GSP-6电极的循环稳定性也最好,100 mA/g的电流密度下经过100周循环后,其比容量高达555 mA·h/g,优于GSP-3的433 mA·h/g和GSP-60的357 mA·h/g,更是比纯6 nm的SnO2比容量提高了6倍,循环稳定性也大为改善。一方面,石墨烯不仅可以作为超强导电包覆层将SnO2紧密包覆,有效降低SnO2颗粒之间的界面电阻,提高电子传输速率;另一方面,其优异的柔韧性和弹性可以适应活性物质的体积膨胀/收缩,从而在充放电过程中为SnO2提供一个更好的保护层。 但是如何选择合适粒径的纳米颗粒与石墨烯复合尤为重要。 同时,制备的石墨烯薄膜电极可以省却导电乙炔黑和粘结剂,大大简化涂膜工艺,具有简便易行的优点。 目前,利用超细粒径SnO2与石墨烯复合制备柔性自支撑薄膜电极还鲜有报道。
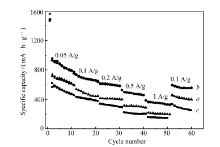 | 图8 不同粒径纳米SnO2颗粒与石墨烯复合制备GSP的倍率性能图Fig.8 Rate capabilities of GSP- n composite electrodes containing SnO2 nanoparticles with different particle size a.GSP-3; b.GSP-6; c.GSP-60 |
图8为含不同粒径SnO2纳米颗粒的GSP电极的倍率性能比较。 充放电电流密度从50 mA/g逐渐增加到1 A/g,然后再回复到100 mA/g,电势区间为0.01~3.0 V。从图8中可以看出,即使在大电流密度1 A/g时,GSP-6的可逆比容量可保持在329 mA·h/g左右,而GSP-3和GSP-60的比容量只有202和145 mA·h/g。 当电流密度回到100 mA/g时,GSP-6容量可快速恢复到550 mA·h/g,表现出了优异的倍率性能,远远高于另外两种纳米粒径的复合电极。
采用简便的抽滤和水热法制备了三明治结构的柔性自支撑SnO2/石墨烯纸薄膜复合电极,讨论了纳米SnO2颗粒的粒径对柔性电极材料电化学性能的影响,结果表明,减小SnO2颗粒尺寸可以在一定程度上抑制循环过程中的体积变化,为锂离子提供相对较短的扩散路径,使其循环稳定性得到一定改善。 通过与石墨烯抽纸复合,可以有效降低SnO2颗粒之间的界面电阻,提高电子传输速率;而且其优异的弹性可以适应活性物质的膨胀/收缩,使SnO2的循环性能得到了很大的改善。 SnO2颗粒尺寸对复合电极的电化学性能有重要影响,其中6 nm SnO2与石墨烯复合的GSP-6薄膜电极循环稳定性最好,经过100周循环后,其比容量高达555 mA·h/g,远高于未复合或粒径过小或过大的复合电极。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|