为设计新型布洛芬缓释体系提供实验依据,以氯化镁、氯化铝、布洛芬(IBU)及淀粉等为原料,采取共沉淀-焙烧还原法及冷冻-解冻法,制备了层状双氢氧化物-布洛芬插层复合物(LDH-IBU)、淀粉凝胶-布洛芬复合物(淀粉凝胶-IBU)及层状双氢氧化物/淀粉凝胶-布洛芬插层复合物(LDH/淀粉凝胶-IBU)。 通过傅里叶红外光谱仪(FT-IR)、X射线衍射仪(XRD)表征了上述3种复合物的结构,并研究了它们在模拟人体环境条件下的缓释性能。 结果表明,3种复合物中的IBU在不同的缓释介质中都具有一定的缓释效果,复合物释放速率大小为:LDH/淀粉凝胶-IBU>LDH-IBU>淀粉凝胶-IBU;在pH值为6.6和7.4以及0.9%生理盐水3种缓冲介质中释放速率依次减小。 释放动力学均符合准一级动力学方程。
To provide experimental basis for the design of new ibuprofen(IBU) sustained release system, the layered double hydroxide-ibuprofen intercalation compound(LDH-IBU), the starch gel-ibuprofen(starch gel-IBU) compound and layered double hydroxide/starch gel-ibuprofen(LDH/starch gel-IBU) intercalation compound were prepared by co-precipitation, roasting reduction and freeze-thaw methods based on magnesium chloride hexahydrate, aluminum chloride hexahydrate, IBU and starch as raw materials. The structures of three kinds of above composites were characterized by Fourier transform infrared spectrometer(FT-IR) and X-ray diffractometer(XRD). Their controlled release properties under the condition of simulated human body environment were studied. The results show that IBU in three kinds of complexes in different release media has certain controlled release effect. The release rates decrease in the order of LDH/starch gel-IBU, LDH-IBU and starch gel-IBU. The release rates in 3 buffer media decrease in the order of pH=6.6, pH=7.4 and 0.9% normal saline. The release kinetics can be fitted to the pseudo-first order kinetic model.
药物在生物体内的吸收、分布和代谢是一个持续改变的过程。 正常的给药方法使药物的浓度在人体内只能保持较短的时间。 然而适当的药物载体所产生的药物缓释作用,不但能减少药物达到相同药效的用药剂量,也可以减少药物的副作用[1,2,3]。 因此,通过设计药物的缓释材料来控制其释放过程,在当前临床医疗上具有重要研究意义[4]。
层状双氢氧化物(LDHs)是一种制备缓释材料的原料。 迄今为止,以LDHs为主体的许多药用材料已被合成出来,主要应用在磁性靶向给药[5,6]、缓释控制材料等领域[7,8]。 凝胶是一种通过适当的交联而具有三维网络结构的药用高分子材料[9],其中,淀粉凝胶因具有很好的生物相容性和可降解性,环境友好和污染性小等特点,被广泛用在药物传递系统中[10]。 布洛芬(IBU)是典型的抗炎、镇痛、解热药物,由于其在水中的溶解度低和相对分子质量小等特点而适用于药物负载,常被用来作为药物控释试验中的典型药物[11]。 当前,合成聚合物缓控体系生物相容性差,天然高分子缓控体系具有生物相容性和药物负载率高等优点,但其热稳定和成型性差;水滑石类层状无机缓控体系可改善药物分子在体内的热稳定性和溶解性,且低毒和生物相容性好。 目前,已有淀粉或水滑石的相关缓释材料研究[5,6,7,8,9,10],但关于二者复合的缓控材料尚未见报道。 有鉴于此,拟采取共沉淀法制备碳酸根型LDH,在此基础上,采取焙烧还原法和冷冻-解冻法,以IBU为客体,制得IBU插层的LDH/淀粉凝胶复合缓释材料,并研究了其在不同的缓释溶液中对IBU的缓释性能,期望制备出一种新型缓释体系。
可溶性淀粉、磷酸氢二钠、六水氯化镁、六水氯化铝、无水碳酸钠等购自于国药化学试剂公司,均为分析纯试剂;布洛芬购自于珠海润都制药股份有限公司,分析纯。
TENSOR27型傅里叶变换红外光谱仪(FTIR,德国Bruker公司);UV2250型紫外/可见分光光度计(UV-Vis,日本岛津制作所);XRD-6100型X射线衍射仪(XRD,日本岛津制作所),测试条件:Cu靶,光源波长 λ为0.154 nm,扫描角度2°~80°,扫描速度6°/min,步长0.02°。
1.2.1 布洛芬插层镁铝层状双氢氧化物的制备
分别将12.20 g六水氯化镁、4.83 g六水氯化铝和6.36 g无水碳酸钠溶于50 mL去离子水中,再将2.40 g氢氧化钠溶解于100 mL去离子水中配成溶液。 将上述氯化铝和碳酸钠溶液加入烧瓶中,用NaOH溶液调节pH=10,在65 ℃下搅拌,同时将氯化镁溶液缓慢滴入,并使pH值恒定。 滴完并在70 ℃下陈化24 h,抽滤洗涤后干燥,即得Mg-Al-C
1.2.2 布洛芬/淀粉凝胶制备
按照参考文献[13]的方法,制备出淀粉凝胶。 取淀粉凝胶0.5 g于50 mL 70 ℃去离子水中,搅拌,充分溶胀;另取0.5 g IBU溶于20 mL 50 ℃去离子水中,强烈搅拌下,缓慢加0.7 mol/mL NaOH溶液直到IBU完全溶解。 将上述2种溶液混合,70 ℃,加热搅拌,用10%氯化氢溶液调节pH值至中性,搅拌1 h,按照冷冻-解冻的方法制备淀粉凝胶-IBU复合物。
1.2.3 布洛芬插层镁铝层状双氢氧化物/淀粉凝胶复合物的制备
取0.5 g LDO和0.5 g淀粉于50 mL去离子水中,其余步骤同上述淀粉凝胶制备法,即采用上述冷冻-解冻法,制得LDH/淀粉凝胶复合物。 取0.5 g LDH/淀粉凝胶复合物于50 mL 70 ℃去离子水中,搅拌使其分散均匀;另取0.5 g IBU溶于20 mL 50 ℃去离子水中,并于强烈搅拌下缓慢加0.7 mol/mL NaOH溶液直到IBU完全溶解。将上述2种溶液混合,70 ℃,搅拌12 h,按上述冷冻-解冻法,即可制得药物插层复合物LDH/淀粉凝胶-IBU。
1.3.1 布洛芬标准曲线的绘制
分别称50 mg IBU,溶于50 mL pH=6.6和7.4的磷酸缓冲溶液或0.9%生理盐水中,配成1 g/L IBU标准溶液。 再配置0.125、0.25、0.5及0.75 g/L系列标准溶液,测其吸光度值,3种缓冲介质中均以IBU在264 nm处的吸光度值作纵坐标,其质量浓度作为横坐标,绘制其标准吸收曲线。 IBU在pH=7.4和6.6缓冲溶液及0.9%生理盐水中的标准吸收曲线分别为:
A1=1.30117 ρ1+0.07509, A2=1.2929 ρ2+0.0322, A3=0.3980 ρ3+0.0795
式中, A1、 A2、 A3为IBU的吸光度,量纲为1, ρ1、 ρ2、 ρ3为其质量浓度(g/L),且3条曲线的相关系数 r分别为0.9994、1.0000和0.9986。
1.3.2 布洛芬吸附及体外缓释实验
在制备LDH-IBU,淀粉凝胶-IBU及LDH/淀粉凝胶-IBU过程中分别收取各IBU负载反应的滤液和产物洗涤液,经定容后测其264 nm处的吸光度,由此得到未被包覆的IBU含量,进而推算出缓释剂的绝对释放量、载药率及包封率。 其包封率( EN)和载药量( LE)计算公式分别为:
EN/%=
式中, m0为绝对释放量(g), m1为缓释剂质量(g), m2为初始投药的质量(g)。
称50 mg负载药物的复合物分散到装有250 mL磷酸缓冲溶液或0.9%生理盐水的烧瓶内,37 ℃,搅拌8 h。 分别在不同时间点移取上清液3 mL于比色皿中,测其吸光度值后再倒回烧瓶内,继续搅拌。 不同时间点IBU的质量浓度 ρt( g/L)由上述标准曲线求得。 以释放作用达到平衡时(本实验取8 h)的质量浓度为最大释放值 ρmax(g/L),据公式 R/%=( ρt/ρmax)×100,算出各时刻( t)IBU的释放百分比( R),再绘制出 R与时间的函数关系曲线。
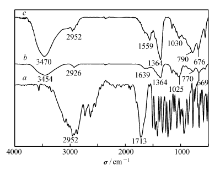
图1为IBU、Mg-Al-C
 | 图1 布洛芬IBU( a)、层状双氢氧化物Mg-Al-C |
图2为IBU、淀粉凝胶及淀粉凝胶-IBU的红外谱图。 由图2可知:对于淀粉凝胶,3411、2922、1645和1459 cm-1分别是淀粉凝胶的羟基伸缩振动吸收峰、CH2反对称伸缩振动吸收峰、淀粉中无定型区域的吸收峰和CH2弯曲振动吸收峰,1019、854、763及576 cm-1分别对应其无规线团结构吸收峰、CH2摇摆振动吸收峰、C—C伸缩振动吸收峰及其骨架振动吸收峰;而对于淀粉凝胶-IBU,不仅存在淀粉凝胶的特征红外吸收峰,且在2956、1511、1468及1716 cm-1处依然存在IBU分子结构中的C—H、苯环及C═O的伸缩振动吸收峰,表明IBU分子已经负载到淀粉凝胶中[15]。
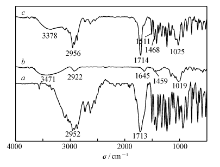 | 图2 IBU( a)、淀粉凝胶( b)及淀粉凝胶-IBU( c)的红外谱图Fig.2 FTIR spectra of IBU( a), starch gel( b) and starch gel-IBU( c) |
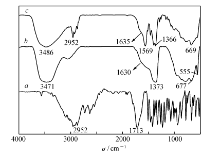
图3为IBU、LDH/淀粉凝胶及LDH/淀粉凝胶-IBU的红外谱。 由图3可知,对于LDH/淀粉凝胶,3454 cm-1是LDH和淀粉羟基的伸缩振动吸收峰,2926、1639、1364、1025及864 cm-1处分别是淀粉凝胶的—CH2反对称伸缩振动吸收峰、无定型区域的吸收峰、C—H弯曲振动吸收峰、无规线团结构吸收峰及—CH2摇摆振动吸收峰,同时在770和564 cm-1出现了淀粉C—C伸缩振动和骨架振动吸收峰,而在557和676 cm-1处存在LDH层板上Mg—O和Al—O的振动吸收峰;而对于LDH/淀粉凝胶-IBU,不仅存在LDH/淀粉凝胶的特征红外吸收峰,且在2952、1559及1452 cm-1处依然存在IBU分子结构中的C—H、苯环伸缩振动吸收峰,同样其在1713 cm-1处的羰基伸缩振动吸收峰因被掩盖而“消失”,表明IBU成功负载到LDH/淀粉凝胶中。
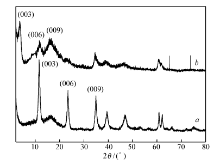
图4为 Mg-Al-C
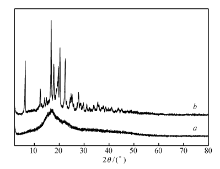
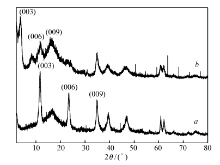
图5为淀粉凝胶和淀粉凝胶-IBU的XRD谱图。 由图5可知,淀粉凝胶在16.8°处有一个特征衍射峰;而淀粉凝胶-IBU复合物分别在6.3°、12.5°、16.8°、17.8°、19.7°、20.3°、22.5°处有较强的特征衍射峰,与淀粉凝胶相比,多出了一些IBU的特征衍射峰,表明IBU已经成功负载到淀粉凝胶上。图6为LDH/淀粉凝胶和LDH/淀粉凝胶-IBU的XRD谱图。 由图6可知,LDH/淀粉凝胶分别在11.6°、23.4°、34.9°处有3个较强的Mg-Al-C
由上述分析可知,试验已成功制备了IBU插层水滑石及IBU插层水滑石/淀粉凝胶复合材料,为研究此类复合材料的缓释效果,首先对缓释材料的绝对释放量、载药率及包封率进行基本测定,结果表明,上述实验方法制备的LDH-IBU、淀粉凝胶-IBU及LDH/淀粉凝胶-IBU的绝对释放量分别为0.054、0.077和0.086 g;其载药率分别为11.8%、15.4%及17.2%;而包封率分别为5.4%、15.4%及17.2%,其中LDH/淀粉凝胶-IBU载药和包封率率均最高。 下面对其缓释速率及动力学进行研究。 由图7可知,LDH-IBU在pH=6.6、7.4和0.9%生理盐水中层间IBU在4 h的释放百分比( R)分别为92.81%、90.47%和84.74%;而淀粉凝胶-IBU的分别为90.58%、88.59%和82.19%;LDH/淀粉凝胶-IBU的则分别为95.16%、92.92%和89.22%。 且上述3类缓释剂在不同缓冲溶液中在4 h后释放均趋于平缓。
图7为LDH-IBU( A)、淀粉凝胶-IBU( B)及LDH/淀粉凝胶-IBU( C)在不同缓释溶液中的 R-t曲线。 由图7也可知,3种IBU复合物在pH=7.4的磷酸缓冲溶液中IBU释放速率顺序为:LDH/淀粉凝胶-IBU插层复合物>LDH-IBU>淀粉凝胶-IBU;在3种释放介质中,3种IBU复合物释放速率规律相同,即LDH/淀粉凝胶-IBU插层复合物>LDH-IBU>淀粉凝胶-IBU。 出现上述现象的可能原因是,IBU负载到LDH上的方式有表面物理吸附和IBU插入到其层间两种,而IBU负载到凝胶上的方式为凝胶的溶胀吸附,可能是这种来自凝胶的吸附作用比后者的吸附方式更能束缚IBU分子释放,故LDH-IBU的释放速率大于淀粉凝胶-IBU的,而IBU负载到LDH/淀粉凝胶上的方式既包含表面物理吸附和插层负载方式,也包含凝胶的溶胀吸附,同时也受到LDH和淀粉凝胶的宏观相分离作用影响,且这种相分离作用的存在可能是显著加速IBU释放速率的主要作用。 同时由上述 R-t曲线分析可见,3种IBU复合物的释放规律均表现出快速释放、慢速释放和平衡3个阶段[17]。
将实验所得数据用药物释放动力学方程中的准一级动力学方程(ln ( qe- qt)=- k1 t+ln qc,式中, t为时间(min); k为释放速率常数(min-1); qe、 qt分别为平衡时刻和 t时刻的吸附量(mg/g))进行拟合,结果表明,3种IBU复合物在pH=7.4的缓冲溶液中及LDH/淀粉凝胶-IBU在3种不同的缓释溶液中,IBU的释放均符合准一级动力学方程(见图8),即ln ( qe- qt)与 t呈直线关系[17]。
图8 A曲线 a为LDH-IBU的拟合曲线,其线性相关系数 ra=-0.9942,速率常数 ka=0.6340;图8 A曲线 b为淀粉凝胶-IBU的拟合曲线, rb=-0.9949, kb=0.5862;图8 A曲线 c为LDH/淀粉凝胶-IBU的拟合曲线, rc=-0.9950, kc=0.6474。 可见, kc> ka> kb,表明LDH/淀粉凝胶-IBU中IBU的释放速率>LDH-IBU的>淀粉凝胶-IBU的。图8 B曲线 a为pH=6.6时的拟合曲线,其 ra=-0.9946, ka=0.7376;图8 B曲线 b为pH=7.4时的拟合曲线, rb=-0.9950, kb=0.6474;图8 B曲线 c为0.9%生理盐水时的拟合曲线, rc=-0.9881, kc=0.5786。 可见, ka> kb> kc,表明LDH/淀粉凝胶-IBU中IBU在pH=6.6时的释放速率>pH=7.4时的>0.9%生理盐水的。
利用共沉淀-焙烧还原及冷冻-解冻法制备了层状双氢氧化物-布洛芬插层复合物(LDH-IBU)、淀粉凝胶-IBU及LDH/淀粉凝胶-IBU等复合物。 FT-IR和XRD分析佐证2种含IBU的复合物中IBU均已成功负载并插入到MgAl LDH层间。 在3种释放介质中,3种复合物释放速率为:LDH/淀粉凝胶-IBU插层复合物>LDH-IBU>淀粉凝胶-IBU,其释放动力学均符合准一级动力学方程,同时3种缓释体系中IBU的释放规律均表现出快速释放、慢速释放和平衡3个阶段。 且3种复合物在3种缓冲介质中释放速率顺序依次为:pH=6.6>pH=7.4>0.9%生理盐水。 由此可见,通过上述设计的新型LDH/淀粉凝胶-IBU插层复合物药物缓释体系可以达到调控药物释放速度的目的,同时也为药物缓释体系的设计提供了良好的实验依据。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|