通过Pechmann法使间苯二酚和乙酰乙酸乙酯发生脱水缩合反应,合成了4-甲基-7-羟基香豆素,再与六次甲基四胺反应,生成7-羟基-4-甲基-8-甲酰基香豆素,最终与吲哚酰肼发生席夫碱反应合成一种香豆素类荧光探针L。 通过核磁共振波谱仪(NMR)、质谱(MS)、傅里叶变换红外光谱仪(FTIR)、荧光发射光谱仪和紫外可见分光光度计等技术手段研究该探针L的结构及其荧光性能。 结果表明,探针L与Zn2+的配合比为1:1,对Zn2+的检测限达到3.6×10-8 mol/L,降低了对Zn2+的检测浓度,同时探针L对锌离子具有高选择性,可应用于在生物体内Zn2+的检测。
A coumarin type fluorescent probe was synthesized from 1 H-indole-3-carbohydrazide hydrazide and 8-formyl 7-hydroxy-4-methylcoumarin, which was obtained by Pechmann condensation of resorcinol and ethyl acetoacetate followed by formylation employing hexamethylenetetramine. The structure and fluorescence properties of this probe were characterized by nuclear magnetic resonance spectroscopy(NMR), mass spectrometry(MS), fluorescence emission spectrometer and UV-visible absorption spectrum. The probe coordinated with Zn2+ in 1:1 ratio and led to high selectivity for the detection of Zn2+ with a detection limit at 3.6×10-8 mol/L. These demonstrate potential application of the probe for the detection of Zn2+ in biological studies.
锌是人体中含量仅次于铁的微量元素,分布于人体细胞和组织液中,在人体内的含量约为0.004%。 锌离子参与了神经信号传递、基因转录、信号转导和免疫反应等生理过程[1,2,3,4]。 如果锌离子在体内缺失,将引起一系列的精神疾病,如老年痴呆症、肌肉萎缩症、帕金森病、中风和癫痫、小孩生长迟缓、发育不良等症状[5,6,7]。 因此,及时、灵敏、高选择性地检测Zn2+对人类健康具有重大意义。
目前,绝大多数探针必须在非水介质中才能很好地识别锌离子,不能满足在水介质中的检测,极大限制了这些探针在实际中的应用。 由于Zn2+具有稳定的 d10电子构型,圆二色谱、核磁共振、电子顺磁共振、循环伏安法等分析方法均不适用于高效测定Zn2+[8],对锌离子的检测限只有2×10-7 mol/L[9]。 荧光分析法可用于分析检测金属离子,具有操作简单,选择专一、高灵敏、高选择、样品不需预处理等优点而备受关注,广泛地应用于生物分析领域[10,11]。 因此,构建新型Zn2+荧光探针已经成为目前研究的热点[12,13]。
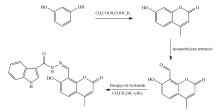
香豆素类化合物广泛存在于植物界,具有良好的荧光性能、稳定性和易于修饰官能团的特点,已被广泛应用于荧光探针的设计和合成[14,15,16,17]。 本文以间苯二酚为原料经席夫碱反应合成4-甲基-7-羟基香豆素,对其结构加以修饰,合成了8-(7-羟基-4-甲基-8-甲酰基)吲哚肼腙探针L(Scheme 1)。 将探针L用于检测Zn2+,研究了其荧光性能、选择性和抗干扰能力。
Avance DRX-400MHz型核磁谱仪(德国Bruke公司);Esquire 6000型液相色谱/质谱联用仪(德国Bruker公司);SGW A-4型显微熔点测定仪(上海精密科学仪器有限公司);Hitachi RF -4500型荧光光谱仪(日立高新技术公司);Perkin Elmer Lamda 35型紫外-可见分光光度计(珀金埃尔默仪器(上海)有限公司);Nexus 670型傅里叶红外光谱仪(美国Nicolet公司)。
吲哚-3-甲酸甲酯(≥99%)购自于韶远化学科技有限公司,其它所有合成原料以及试剂均为市售分析纯,实验用水为二次蒸馏水。
4-甲基-7-羟基香豆素[18]的合成 在250 mL三口瓶中,加入100 mL浓硫酸,-5 ℃,加入10 g间苯二酚和12 g乙酰乙酸乙酯,升温至10 ℃,反应过夜。 将反应液缓慢倒入约200 g碎冰的500 mL烧杯中,搅拌,析出大量白色沉淀,抽滤,去离子水洗涤沉淀2次,然后将沉淀溶解于350 mL质量分数为5%的NaOH溶液中,过滤,收集。 在滤液中,缓慢滴加稀HCl溶液,搅拌,析出沉淀,抽滤,并用去离子水将沉淀洗涤至中性,收集干燥。产物在无水乙醇中重结晶,得到11.2 g白色针状晶体,产率为74.2%,mp 190 ℃。1H NMR(400 MHz,DMSO), δ:10.53(s,1H),7.60(d, J=8.7 Hz,1H),6.81(dd, J=8.7,2.3 Hz,1H),6.71(d, J=2.3 Hz,1H),6.14(s,1H),2.37(s,3H)。
7-羟基-4-甲基-8-甲酰基香豆素[19]的合成 在250 mL梨形瓶中依次加入6.50 g 4-甲基-7-羟基香豆素、9.8 g六次甲基四胺、60 mL冰乙酸, 95 ℃,回流约3 h,使用TLC跟踪反应。 当原料点消失后,将体系冷却到室温,加入75 mL 20%稀盐酸,95 ℃,反应45 min,冷却到室温,使用二氯甲烷萃取3次,收集有机相,有机相用饱和食盐水洗涤1次,无水硫酸钠干燥,减压除去二氯甲烷。 在剩余液体中,倒入碎冰,搅拌,析出大量黄色固体,使用柱层析纯化, V(石油醚(PE)): V(乙酸乙酯(EA))=1:1的混合溶剂作洗脱剂,得到1.84 g 白色的固体,产率为38.8%,mp 182 ℃。1H NMR(400 MHz,DMSO), δ:11.90(s,1H),10.44(s,1H),7.93(d, J=8.9 Hz,1H),6.97(d, J=8.9 Hz,1H),6.30(s,1H),2.41(s,3H)。
8-(7-羟基-4-甲基-8-甲酰基)吲哚肼腙L的合成 在250 mL反应瓶中,依次加入50 mL无水乙醇、4.0 mmol 7-羟基-4-甲基-8-甲酰基香豆素,75 ℃,回流,然后加入吲哚酰肼的乙醇溶液,溶液变浑浊,待有淡黄色沉淀析出,继续回流12 h,热过滤,并用少许热的乙醇溶液洗涤沉淀,得到的0.997 g淡黄色固体产物,产率为66.3%,mp.290~293 ℃。1H NMR(600 MHz,DMSO), δ:12.94(s,123H),12.62(s,15H),12.06(s,8H),11.99(d, J=44.0 Hz,153H),11.84(s,152H),11.52(d, J=18.4 Hz,8H),9.01(s,136H),8.78(s,16H),8.33~8.15(m,265H),7.70(d, J=8.8 Hz,162H),7.51(d, J=7.9 Hz,132H),7.20(dt, J=14.6,7.0 Hz,277H),6.96(dd, J=24.7,8.8 Hz,152H),6.25(d, J=8.1 Hz,144H),4.35(s,8H),3.58~3.31(m,317H),3.31~3.30(m,6H),2.49(d, J=14.8 Hz,189H),2.40(d, J=11.6 Hz,527H),2.31(s,6H),2.18(s,19H),2.09(s,121H),2.02(d, J=20.0 Hz,61H),1.06(t, J=7.0 Hz,18H),0.00(s,35H),-0.05(s,6H);13C NMR(151 MHz,DMSO), δ:161.29,159.77,154.37,152.64,136.64,127.89,126.72,122.92,121.48,121.36,113.85,112.60,112.24,111.07,40.40,40.26,40.12,39.98,39.84,39.70,39.56,31.13,18.77;IR(KBr), σ/cm-1:3265(—OH),1695(C=O),1650(C=N);C20H15N3O4元素分析值/%:C 66.48,H 4.18,N 11.63,O 17.71;实测值/%:C 66.52,H 4.14,N 11.66,O 17.68(HRMS对C20H15N3O4的理论值361.1063,测量值361.1066)。
在紫外和荧光光谱的分析实验中,因为二甲基亚砜对配体L的溶解性好,所以用二甲基亚砜(DMSO)配制配体L溶液,如果配体浓度过大,导致检测离子的用量过多,同时受实验仪器的限制,所以配体的浓度为5.0×10-3 mol/L。 再用浓度为5.0×10-3 mol/L K+、Ca2+、Na+、Mn2+、Fe3+、Fe2+、Co2+、Ni2+、Cu2+、Cd2+、Hg2+、Pb2+、Al3+、Zn2+的水溶液作为储备液,在后续光谱测试分析中使用。
探针L的紫外及荧光光谱滴定实验均是在DMSO溶液中测定的,紫外和荧光光谱分析都是在室温下进行测定的,最大激发波长为378 nm,狭缝为3.5 nm。
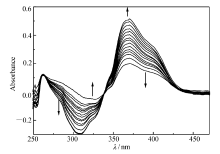
探针L(50 μL)在DMSO体系中随着Zn2+(5.0×10-3 mol/L)浓度增加的紫外吸收变化曲线,如图1所示。 可见,探针L在370 nm处有一个吸收峰,随着Zn2+的不断加入,在262和389 nm处的吸收峰强度不断减弱,在257和326 nm处吸收峰强度不断增强,说明配体L与Zn2+不断配合,形成了新的金属配合物。 在262、339和431 nm处明显的等吸收峰也充分的证明了配体L与Zn2+已经形成稳定的配合物。 在300~330 nm之间,由于DMSO本身的吸收非常强,而DMSO又可与探针L一起与锌离子形成混合配合物,这样随着锌离子浓度增加,混合配合物增多,干扰了吸光度,所以在这一波长范围内的吸光度产生了负值。
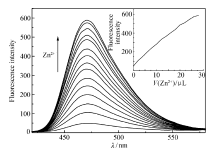
先向石英比色皿中加入2 mL的DMSO溶液,再加入20 μL配体L(5.0×10-3 mol/L)的DMSO溶液混匀,逐渐加入2 μL Zn2+,并测定每次加入后的荧光谱图。 在DMSO体系中,探针L的最大发射波长在472 nm处,随着Zn2+(5.0×10-3 mol/L)不断加入,荧光强度不断增加,并且最大发射光的波长移至470 nm处,在光诱导下螯合后的氮原子和氧原子与Zn2+之间的电子转移作用导致L的荧光增强[20]。图2为探针L(50 μL)在DMSO体系中随着Zn2+浓度增加的荧光光谱变化曲线。 右上角为锌离子用量与荧光强度的曲线图。
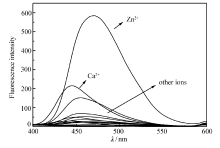
在检测配体L对不同金属离子识别能力的实验中,选择K+、Ca2+、Na+、Mn2+、Fe3+、Fe2+、Co2+、Ni2+、Cu2+、Cd2+、Hg2+、Pb2+、Al3+、Zn2+为识别对象,分别在含有20 μL配体L的缓冲溶液中加入同样比例的金属离子水溶液(5.0×10-3 mol/L),测定其荧光发射光谱变化曲线(图3)。 可见,除Ca2+外其它金属离子并未引起体系荧光强度明显的变化,其中Ca2+引起体系最大荧光强度下波长的蓝移,但比较荧光强度变化不大。 综上可以看出,探针L对Zn2+具有良好的选择性。
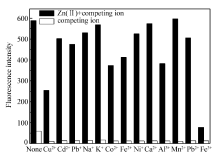
一种好的荧光探针,必须在其它金属离子存在的情况下,能对被识别的金属离子做出高选择性。 在图4中,白色柱条表示各种金属离子单独存在时探针L的荧光强度,黑色柱条表示和干扰离子共存时探针L的荧光强度。 在含有20 μL探针L的DMSO溶液中,加入2倍于探针L的金属离子,测定其荧光发射强度,之后再测定加入和探针L一倍化学计量Zn2+后荧光强度的变化。 实验表明,除了Cu2+、Fe2+对Zn2+具有明显干扰外,大多数金属离子对Zn2+的干扰很小,该探针L对Zn2+识别具有一定的抗干扰性,可作为一种具有良好选择性的荧光探针。
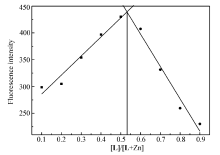
通过等物质的量连续变化法(Job's-Plot),研究了探针L与Zn2+的配合比,配制一系列L与Zn2+的混合溶液,体积比分别为1:9、2:8、3:7、4:6、5:5、6:4、7:3、8:2和9:1,总体积保持为20 μL,测定其最大荧光强度。 如图5所示,当探针L的摩尔比在0.5左右时,体系的荧光强度最大,说明探针L与Zn2+形成配合物的比例为1:1。
如图6 A所示,在DMSO体系中,加入20 μL探针L,Zn2+的浓度由0.1 μmol/L增加到0.6 μmol/L,得到低浓度的荧光滴定曲线。 经拟合得到线性回归方程 y=432.9694 x+6.5255, R2=0.9462(图6 B),最后利用Scatchard方程计算得到检测限为3.6×10-8 mol/L。
合成了一种香豆素类荧光探针L,其合成简便,原料便宜。 探针L在DMSO溶液中对Zn2+具有灵敏度高和选择性好,并对其他金属离子具有抗干扰能力。 探针L与Zn2+的配合比为1:1,在探针L的DMSO溶液中加入Zn2+后荧光强度显著增强,最大荧光发射波长发生移动,从472 nm移动到470 nm。 探针L对Zn2+的检测限达3.6×10-8 mol/L。 该探针对于生物系统及环境检测中检测Zn2+含量具有一定潜在应用前景。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|