金属有机骨架(Metal-Organic Framework,MOF)复合材料是一种新型功能性材料,其中金属氧化物@MOF复合材料因结合了金属氧化物和MOFs的许多特性而受到人们的广泛关注,成为近年来MOFs材料研究的一个重要方向。 本文综述了金属氧化物@MOF复合材料制备方法的研究进展,主要包括外延生长法、气相沉积法、模板法等,并分析了它们各自的优缺点;概述了金属氧化物@MOF复合材料在催化、传感、生物医药、吸附与分离方面的具体应用性能,以及在电化学研究领域的潜在应用;并提出今后金属氧化物@MOF复合材料研究的主要方向是开发简单高效的制备方法、选取新功能性金属氧化物以及探索复合材料的其它新型结构,以拓展其在工业上的应用。
Metal oxide@MOF(metal-organic framework) composite materials have emerged as a new class of functional materials and attracted considerable interests in many fields due to the unique properties in combination of metal oxide with MOF, which has been an important research direction of MOF materials in recent years. In this review, we systematically summarize the research progress towards various synthetic methods for metal oxide@MOF composite materials, such as epitaxial growth method, gas phase infiltration method and template method. The advantages and disadvantages of these methods are discussed, respectively. Applications of metal oxide@MOFs composite materials in adsorption and separation, catalysis, sensing, biomedical and potential applications of metal oxide@MOFs composite materials in electrochemical research are also discussed. In order to expand its application in industry, the improvement of synthetic methods, the preparation of new functional metal oxides and the exploration of new structures are proposed as the main future research and development directions of metal oxide@MOFs composite materials.
金属有机骨架材料(Metal-Organic Frameworks,MOFs)又称为多孔配位聚合物(Porous Coordination Polymers,PCPs),是一类具有多样拓扑结构的有机-无机杂化晶体材料[1,2]。 由于其具有高比表面积、可调节孔径和良好的热稳定性等多种优点[3,4],被广泛地应用于气体吸附/分离、载药、催化等方面[5,6,7]。 然而,MOFs也存在不足之处,其结构易受环境中水、氧气或溶剂影响而发生坍塌,部分MOFs的耐真空或低温能力差。 此外,与热稳定性高的沸石材料相比,大多数MOFs在高温条件下均会发生分解。 这些客观存在的缺点阻碍了MOFs的实际应用。
近年来,为了进一步提高MOFs性能和实用性,科研工作者开始致力于金属有机骨架复合材料的研究[8,9]。 这种复合材料不仅具有MOFs的特性,还具备其他功能材料的光学、电学、磁学和催化等特性[10,11,12],这些功能材料主要包括金属纳米粒子、多金属氧酸盐、金属氧化物、聚合物、石墨烯和碳纳米管等[13,14]。 本文探讨了由金属氧化物与MOFs形成复合材料的研究进展,主要包括制备方法及其应用。
金属氧化物@MOFs的制备方法主要包括外延生长法、气相沉积法以及模板法。
外延生长法是最常见的金属氧化物@MOFs复合材料的合成方法。 该方法能使MOFs前体在金属氧化物表面成核,再以晶核为中心向四周生长形成复合材料。 为了促进MOFs在金属氧化物表面成核,通常需要对金属氧化物表面进行官能团修饰。 根据不同的合成方式又可分为层层自组装法和分子自组装法。
Ke等[15]在室温下将巯基乙酸(MAA)改性的Fe3O4微球交替浸渍在醋酸铜(Cu(OAc)2)和均苯三甲酸(H3btc)乙醇溶液中,以层层自组装的方式制备了具有核壳异质结构的Fe3O4@[Cu3(btc)2]复合材料,如图1所示。 改性的Fe3O4微球表面的羧基基团与金属离子结合,然后在溶剂热的反应条件下,在微球表面形成MOFs晶体。 研究表明,改变交替浸渍次数和反应温度可以调控包覆尺寸以增大微球直径。 当交替浸渍次数由20次增加到50次时,微球直径由0.75 μm增加到1.6 μm;在同样的循环次数下,当反应温度由25 ℃上升到70 ℃时,微球直径由1 μm增加到2 μm。 采用类似的方法,Chen等[16]和Zhang等[17]成功制备了Fe3O4@MIL-100(chromium(Ⅲ) terephthalate),Sun等[18]也以该层层自组装的方式合成了Fe3O4@HKUST-1(Hong Kong University of Science and Technology)。
 | 图1 Fe3O4@[Cu3(btc)2]核壳微球制备流程及透射电子显微镜照片[15] Fig.1 Schematic representation of the step-by-step synthesis strategy(a); TEM images of individual core-shell magnetic microsphere of Fe3O4@[Cu3(btc)2](b~g)[15] |
Zhang等[19]应用一种阴离子型聚电解质聚乙烯磺酸钠(PSS)对Fe3O4颗粒进行表面预处理,大幅度提高了Fe3O4颗粒表面负电荷密度,PSS均匀分布在平均直径600 nm的Fe3O4微球表面,能吸附Zn2+促进ZIF-8晶体快速成核,最后形成Fe3O4@ZIF-8核壳异质磁性复合材料,如图2所示。 从TEM图像上来看,ZIF-8壳平均厚度为100 nm。 相比于层层自组装的方式,这种分子自组装法更加简便快捷,同时Fe3O4微球表面分散的MOFs晶体更加连续。 同样的方法,Zhang等[20]选用硫醇封端的ZnO纳米棒为基体,在溶剂热的反应条件下,成功制备了生长在有序分层结构ZnO纳米棒上的MOF-5薄膜。 Zacher等[21]也以该分子自组装的方式合成了一系列Al2O3@[Cu3(btc)2]复合材料。
 | 图2 Fe3O4@ZIF-8核壳微球制备流程(a)及形貌分析图(b,c)[19]Fig.2 Preparation procedure of Fe3O4@ZIF-8 core-shell microspheres(a), TEM images of ZIF-8 growth on functionalized Fe3O4(b) and SEM images of the Fe3O4 particles(c)[19] |
综上所述,外延生长法是一种有效的、常用的制备金属氧化物@MOFs复合材料的方法,并且实现了MOFs层厚度的控制。 但该方法制备步骤繁琐耗时,同时表面活性剂对MOFs结构和形貌存在潜在的影响。
金属有机化学气相沉积法(MOCVD)是由Fischer等[22]最先开发的一种将金属或金属氧化物纳米粒子掺入到多孔MOFs中的高效方法。 在一定的温度和压力下,气态金属有机化合物前体随载气(H2、Ar)进入化学沉积反应器,并通过气相边界层扩散到MOFs基体中,再经过氢还原或简单的热分解处理后形成金属氧化物@MOFs复合材料。
Herrmens等[23]通过将MOF-5暴露于挥发性有机金属化合物蒸气中制备了一系列[L nM] a@MOF-5复合材料,其中[L nM]表示前体分子,下角标 a表示MOF-5晶格的每个空腔中的有效前体分子数。 他们首先将前体溶液二乙基锌([Zn(C2H5)2])和MOF-5置于化学沉积反应器中,在10 Pa和27 ℃的条件下充分混合得到[Zn(C2H5)2]@MOF-5,然后在空气中缓慢水解24 h,最后的水解产物在250 ℃的真空条件下加热3 h得到(ZnO)2@MOF-5复合材料。 研究证实,MOF-5主体晶格和客体分子是通过范德华力相互作用,而前体分子和主体框架结构并不会发生任何变化。 受上述研究的启发,Esken等[24]将ZIF-8暴露于同样的挥发性有机金属化合物二乙基锌气氛下,得到[Zn(C2H5)2]0.38@ZIF-8,然后在含体积分数5%Ar气的氧气中进行氧化和热处理得到(ZnO)0.35@ZIF-8复合材料。
气相沉积法已经成功制备出多种金属氧化物@MOFs复合材料,并且其中金属氧化物纳米颗粒具有良好的分散性和小的粒径尺寸。 但该方法制备成本较高,能源消耗大,对制备条件要求相对苛刻,反应时间、金属有机前驱体浓度、气流性质、反应室温度和压力等因素对复合材料的结构及性能影响明显,同时,金属有机化合物前驱体需具有稳定的化学性质、高的饱和蒸汽压、合适的沉积速率等特性。
模板法是以金属氧化物作为MOFs生长的模板,同时也作为合成MOFs的金属源制备金属氧化物@MOFs复合材料的方法。 相比于外延生长法,该方法无需对金属氧化物表面进行功能化预处理,也能使所形成的MOFs晶体都生长在金属氧化物表面,且晶粒尺寸均一可控。
Zhan等[25]通过简单的自模板法制备了ZnO@ZIF-8核壳异质纳米棒复合材料,如图3所示。 在整个反应过程中,ZnO不仅提供Zn2+以促进ZIF-8晶粒在其表面结晶,而且还作为ZIF-8生长的载体;同时,2-甲基咪唑不仅作为合成ZIF-8的配体,而且还是侵蚀剂以溶解ZnO提供Zn2+。 研究表明,当反应温度为70 ℃,反应溶液中DMF/H2O(体积比为1:1)时,整个溶液能够很好地达到溶解-配位平衡,有助于在ZnO表面形成均匀有序的ZIF-8晶粒。 应用类似的方法,Wang等[26]制备了CuO@Cu3(BTC)2核壳异质复合材料,其中CuO作为模板和金属源。 随着反应时间的延长,复合材料中Cu3(BTC)2的含量也逐渐上升,当反应4和8 h后,CuO和Cu3(BTC)2的化学计量比分别为1:0.073和1:0.115。
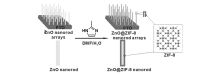 | 图3 ZnO@ZIF-8纳米棒复合材料制备流程[25]Fig.3 Schematic illustration of ZnO@ZIF-8 nanorods synthesized via the Self-Template strategy[25] |
此外,以MOFs为前驱体制备金属氧化物@MOFs复合材料也属于模板法的一种。 与传统模板法相比,MOFs模板法具有晶体颗粒大小形貌可控、无去模板过程、易碳化等优势,被广泛应用于制备先进功能材料,这些功能材料在催化、载药、电池等领域具有巨大的应用潜力[27,28]。 同时,MOFs可控的粒径和形貌可间接地控制金属氧化物的粒径和形貌。 Yang等[29]考虑到ZIF-8(420 ℃)的热稳定性远高于HKUST-1(280 ℃),将聚乙烯吡咯烷酮(PVP)改性的HKUST-1分散在Zn(NO3)2·6H2O溶液中,然后加入2-甲基咪唑,制备了HKUST-1@ZIF-8,最后在350 ℃下将产物煅烧0.5 h得到Cu xO@ZIF-8复合材料,其中ZIF-8有序的孔道结构有助于Cu xO纳米粒子的形成和均匀分散。 这种新颖的合成方法为制备金属有机骨架复合材料提供了新的思路。
与上述两种方法相比,模板法是一种成本较低、能源消耗少和简单快捷的新颖制备方法。 但该方法适用性有限,对溶剂、模板物质、后处理温度的选取相对困难。
除了上述制备方法以外,研究人员还在原先的方法上进行了改进,发明了一些简易高效的方法。 Faustini等[30]首次利用两步连续微流法制备了磁性Fe3O4@ZIF-8核壳异质复合材料,如图4所示。 他们首先在微流反应器中将Fe3O4前体溶液与油混合组成微液滴,然后将所产生的含有Fe3O4颗粒的液滴送入到第二微反应器中与ZIF-8前体溶液以及聚乙烯磺酸盐快速混合,使ZIF-8晶粒迅速生长在经聚乙烯磺酸阴离子基团改性的Fe3O4颗粒表面。 研究表明,制备Fe3O4@ZIF-8复合材料的整个过程仅需大约9 min,大大节省了合成时间。 同时,从SEM图像(图5)上来看,该复合材料呈球状,直径在(700±50) nm之间。 Chang等[31]利用简易的溶胶-凝胶法制备了具有强吸附性能的“分子泵”复合材料TiO2@MIL-100。
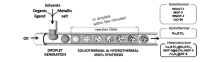 | 图4 两步微流法快速制备Fe3O4@ZIF-8流程图[30]Fig.4 Schematic representation of the general microchemical process[30] |
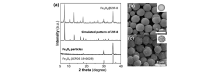 | 图5 Fe3O4@ZIF-8核壳异质结构XRD图(a)及扫描电子显微镜照片(b,c)[30]Fig.5 XRD patterns and SEM images of the Fe3O4@ZIF-8 particles a.XRD patterns of the Fe3O4, Fe3O4@ZIF-8 and Fe3O4(JCPDS 19-0629) particles and the simulated single-crystal XRD pattern of ZIF-8; b.SEM images of Fe3O4; c.SEM images of Fe3O4@ZIF-8 particles[30] |
金属氧化物纳米粒子具有光学、电学、磁学和催化等性质,同时,MOFs具有高比表面积和高度选择性等独特性能,金属氧化物@MOFs复合材料能结合了二者的优势性能,在催化、传感、生物医药、磁性分离等相关领域具有巨大的应用潜力。
由于MOFs材料具有大的比表面积和不饱和活性位点,因此,它在催化领域有着广阔的应用前景[32,33]。 然而,MOFs作为催化剂广泛应用于工业实际生产却还存在缺陷,其主要原因是MOFs的可回收性差,难以从反应介质中分离,从而影响其循环利用性。 另一方面,金属氧化物纳米粒子也是一种非常具有吸引力的新型催化剂[34,35],但是,在催化反应中这类纳米粒子极易发生团聚而导致中心区域失活,影响其催化效率。 而MOFs有序的孔道结构和高的比表面积可以为金属氧化物纳米粒子提供载体,有效抑制其团聚,同时,部分磁性金属氧化物与MOFs形成的复合材料在外磁场的作用下可快速从反应介质中分离,以便收集和循环利用。 到目前为止,金属氧化物@MOFs复合材料作为催化剂的应用主要集中在光催化反应和Knoevenagel缩合反应。
2.1.1 光催化反应 在MOFs结构中有机配体的“天线效应”下,作为半导体量子点的金属簇在光的激发下得以活化,促使MOFs成为一种高效的光催化剂[36,37]。 同时,金属氧化物纳米粒子,例如TiO2、Zn2GeO4和BiVO4等,作为传统的光催化剂也逐渐发展成熟[38,39]。 因此,金属氧化物@MOFs复合材料作为一种新型光催化剂能巧妙地结合二者的优点,其光催化活性得到了大大的提升。
1)光催化降解有机染料:Zhang等[17]制备的Fe3O4@MIL-100(Fe)核壳异质磁性复合材料可作为一种在可见光和紫外光下降解亚甲基蓝(MB)的高效光催化剂。 相比于传统的光催化剂C2N4和氮掺杂的TiO2,在可见光下Fe3O4@MIL-100(Fe)降解MB的速率常数t为0.01977/min(其中,ln ( c/c0)= kt; c和 co分别表示MB初始和分解后的浓度; k为常数),是C3N4(6.074×10-4/min)的33倍,氮掺杂TiO2(0.00121/min)的15倍,并且经过5次循环后Fe3O4@MIL-100(Fe)的速率常数基本保持不变,分别为0.0164/min、0.0162/min、0.0157/min和0.0151/min,证明了该新型光催化剂具有循环耐用、经济、绿色等优点。 同时,他们还发现H2O2的存在可以增强该复合材料的光催化活性。 在光照射下,MIL-100(Fe)中的价带(VB)电子受到激发后进入到导带(CB)中,促使光催化剂材料中出现大量的光生空穴-光生电子对,而作为电子受体的H2O2会接受电子以抑制电子-空穴对重组,进而产生更多的羟基自由基促进MB的降解(图6)。
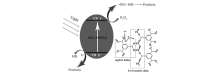 | 图6 光催化剂MIL-100(Fe)电子转移过程及其降解MB示意图[17]Fig.6 A schematic illustration of MB degradation over the MIL-100(Fe) photocatalyst under light irradiation(inset:the chemical structure of MIL-100(Fe) and the electron transfer processes that occurs in MIL-100(Fe) when irradiated by light)[17] |
此外,Xu等[40]利用简单的水热法制备了BiVO4@MIL-101复合材料,其在可见光下光催化降解有机染料罗丹明B(RhB)时表现出较高的活性。 研究表明,在可见光下,由RhB产生的光生电子被快速转移到BiVO4的导带中,促使其产生大量的光生空穴。 同时这些光生空穴又被吸附到MIL-101的价带中,有效地分离了光生电子-光生空穴对,从而提高了该复合材料对RhB的降解能力(图7)。
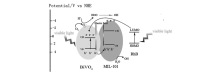 | 图7 可见光下BiVO4/MIL-101复合光催化剂分离电子-空穴对示意图[40]Fig.7 Schematic diagram of separation of electron-hole pairs over BiVO4/MIL-101 composite under visible light[40] |
2)光催化还原二氧化碳:近年来,MOFs结合具有光催化活性的金属氧化物纳米粒子催化还原二氧化碳的应用,引起了化工、能源、材料等领域科研工作者的广泛兴趣。 Crake等[41]报道了具有吸附和光催化还原二氧化碳双功能复合材料TiO2@NH2-UiO-66。 NH2-UiO-66具有高的比表面积和二氧化碳吸附能力,有利于二氧化碳与富集在TiO2表面的光催化活性位点充分接触;同时,NH2-UiO-66可以快速吸附TiO2受光照激发产生的光生空穴,有效抑制光生空穴-光生电子对的复合,增强该复合材料的光催化活性。 实验表明,随着NH2-UiO-66含量的增加,TiO2@NH2-UiO-66对二氧化碳的还原速率先上升后下降,当其质量分数达20%时,该复合材料具有最大的光催化活性,是纯TiO2活性的1.5倍(图8)。 受上述研究的启发,Liu等[42]将ZIF-8高效吸附溶解在水中二氧化碳的性质与Zn2GeO4的光催化活性结合,成功制备了ZIF-8@Zn2GeO4纳米复合材料。 该新型光催化剂可快速吸附溶解在水中的二氧化碳,并在光照下将其转化为甲醇。 实验发现,在10 h的光照下,含质量分数25%ZIF-8的复合材料吸附水中二氧化碳的量是纯Zn2GeO4的3.8倍,同时其对二氧化碳的转化率也增加了65%。
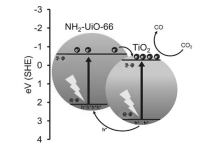 | 图8 TiO2@NH2-UiO-66复合材料光催化还原CO2 示意图[41]Fig.8 Proposed photocatalytic CO2 reduction pathway over TiO2/NH2-UiO-66[41] |
最近,Yan等[43]制备了ZIF-9@TiO2复合材料。 ZIF-9不仅具有高效吸附和活化二氧化碳的性能,而且还可快速分离TiO2界面的光生载流子,因此,ZIF-9作为助催化剂有效增强了TiO2光催化还原二氧化碳的能力。 他们发现,当ZIF-9和TiO2的质量比为3:97时,该复合材料具有最大的光催化活性。
2.1.2 Knoevenagel缩合反应 Knoevenagel缩合反应是在弱碱(胺、吡啶等)催化下,醛或酮与具有活泼 α-氢原子化合物缩合成 α, β-不饱和羰基化合物的一种反应[44]。 目前,一些均相催化剂和多相催化剂被广泛应用于Knoevenagel缩合反应,但是均存在反应物不易分离、重复性差、不利于循环使用等缺点。 因此,越来越多的科研工作者将注意力转移到金属有机骨架复合材料。 对于Knoevenagel缩合反应,这种复合材料是一种环保、经济、高催化活性且可循环利用的新型催化剂。
Faustini等[30]利用两步连续微流法制备的磁性Fe3O4@ZIF-8复合材料在应用于苯甲醛和氰基乙酸乙酯的Knoevenagel缩合反应时表现出较高的催化活性。 在外磁场下,该磁性复合材料可均匀分散在毛细管反应器的内壁上,有效加快了反应物和催化剂之间的扩散和传质,有助于催化反应的进行(图9)。 实验证实,当反应进行到5 min时,苯甲醛的转化率已经达到了55%,并且经过35 min后,转化率迅速增加到99%,远高于简单搅拌条件下苯甲醛的转化率(反应进行到5和50 min时的转化率分别为35%和49%)。 同时,通过外磁场的作用还可快速分离催化剂加以循环利用。 同年,受上述研究的启发,Zhang等[19]以分子自组装的方式制备了Fe3O4@ZIF-8复合材料,并应用于上述Knoevenagel缩合反应。 他们发现,磁性Fe3O4微球表面的ZIF-8晶体不仅分布均匀而且晶粒尺寸明显减小,能促进该反应的进行;另外,电感耦合等离子体原子发射光谱法(ICP-AES)结果显示,催化后的反应溶液中不存在Fe和Zn元素,从而证明该复合材料对流动反应体系具有耐浸蚀性。
MOFs材料的可调节孔尺寸和高比表面积,使其在检测有机分子和离子方面表现出良好的选择性和灵敏度[45,46]。 而MOFs传感器仍然存在稳定性差和不利于循环利用的缺点。 因此,人们开始关注金属有机骨架复合材料,其中金属氧化物@MOFs复合材料是解决上述问题的有效途径之一。
MOFs材料可以选择性吸附尺寸比MOFs孔径小的分子,这些被吸附的分子会与金属氧化物纳米粒子相互作用。 在MOFs和金属氧化物的协同作用下,被检测分子及浓度将转变为光、电、力学性能的变化。 Zhan等[25]以自模
 | 图10 ZnO@ZIF-8新型传感器工作原理及其对H2O2和AA光电流响应示意图[25]Fig.10 Photocurrent response of ZnO nanorod arrays against H2O2(0.1 mmol) and AA(0.1 mmol)[25] |
板法制备的ZnO@ZIF-8纳米复合材料可用于检测黏性溶液中的H2O2分子。 由于ZIF-8晶体的孔径大于H2O2分子但小于抗坏血酸分子(AA),所以该复合材料的光响应会随着H2O2浓度的增加而上升,随着AA浓度的增加而降低,从而有效地监控H2O2分子及其浓度,如图10所示。 同样的方法,Yang等[29]报道的CuxO@ZIF-8复合材料在应用于检测H2O2分子时表现出明显的优势:1)高度选择性。 Cu xO@ZIF-8复合材料中的ZIF-8壳,孔径小且结构规整,会阻碍大分子的穿过,如抗坏血酸(AA)、尿酸(UA)、多巴胺(DA)等,而对于H2O2这类小分子则可穿过ZIF-8壳与Cu xO作用产生响应电流,有效提高其检测H2O2的选择性和抗干扰能力;2)可重复使用性。 该电化学传感器在8次检测50 μmol/L H2O2中响应电流的相对标准差仅为4.1%;3)强稳定性。 Cu xO@ZIF-8新型传感器在经过6个循环伏安曲线电化学测试后仍具有完整的形态,同时,由价跃电位曲线的记录发现,其在空气中储存一个月后的响应电流仍保持原有值的97.8%。
此外,具有发光性能的复合MOFs材料也是目前研究较多的一类新型传感材料,其检测下限低且能产生肉眼可见的响应信号。 Wehner等[47]首次报道了一种具有超顺磁性和发光性双功能复合MOFs材料[Ln2Cl6(bipy)3]·2bipy@Fe3O4/SiO2(bipy=4,4'-联吡啶)。 MOFs发光性能受到水的影响会发生不可逆的淬灭,所以其可应用于检测有机溶剂中的水分子;同时,在外磁场的作用下,该磁性复合材料会发生聚集,这将增强光信号,有益于观测发光程度的变化和降低检测下限。 并且,相比于传统的实验滴定检测法,该新型传感器不仅高效简便,而且还可辅助光致发光光谱进行定量检测。
目前,MOFs材料已经被广泛用于气体、离子和有机小分子的吸附和分离[48,49,50]。 为了进一步扩大MOFs材料作为吸附剂的应用领域,以及增强吸附物与MOFs材料之间的相互作用力,科研工作者开始致力于研究MOFs复合材料。 Xiong等[51]以外延生长法制备的 γ-Fe2O3/C@HKUST-1复合MOFs材料对水溶液中污染物MB和重金属离子Cr6+有较好的吸附效率,并且通过磁分离可实现吸附剂的循环利用。 实验发现,相比于 γ-Fe2O3/C和活性炭,该复合材料对MB和Cr6+的吸附能力有大幅度的提升,最大吸附容量可分别达到370.2和101.4 mg/g,并且,在经过5个吸附-解吸附循环实验后,其仍然保留有90%的去除率,表现出较强的稳定性(图11)。 Chen等[16]报道的磁性Fe3O4@MIL-100核壳复合材料可作为高效吸附剂用于磁性固相萃取技术。 该技术在用于检测环境水样品中的多氯甲苯时表现出灵敏度高、线性范围宽(5~4000 ng/L)、检测下限低(1.07~1.57 ng/L)等特征。 同时,此研究也为环境污染物的吸附降解提供了新思路。
 | 图11 30 ℃下不同吸附剂对MB(a)和Cr(Ⅵ)(b)的等温吸附曲线[51]Fig.11 Adsorption isotherms for MB(a) and Cr(Ⅵ)(b) on different adsorbents at 303 K[51] |
此外,Qu等[52]最近报道了一种新型多层多孔高效吸附剂Cu-BTC/CuO/CFP(碳纤维纸)。 该复合材料中CuO纳米粒子和Cu-BTC及CFP之间均存在微孔,这种独特的孔结构促使其对CH4/N2的选择吸附性增强。 经6 h制备的Cu-BTC/CuO/CFP(摩尔比为0.3:0.13:0.57)复合吸附剂具有最好的选择吸附性,在1~100 kPa的压力范围内,0 ℃下,该新型吸附剂对CH4/N2的选择吸附性是等物质的量的纯Cu-BTC的1.65~2.15倍。
MOFs材料独特的空间拓扑结构、巨大的比表面积和良好的热稳定性等性质使其具备在生物医药上的应用潜质[53,54,55]。 金属氧化物@MOFs复合材料强化了其在药物输送和载药方面的应用,可同时实现高载药量和药物控制释放。 Ke等[56]报道的Fe3O4@HKUST-1复合材料可作为一种新型磁性药物载体。 研究表明,每克该复合材料可吸附高达0.2 g的抗胰腺癌药物尼美舒利,并且在37 ℃的生理盐水中经过11 d的时间可完全释放。考虑到Cu基HKUST-1潜在的生理毒性,他们[15]又制备了基于良好生物相容性和无毒性MIL-100(Fe)的磁性复合材料Fe3O4@MIL-100(Fe)。 同时,该复合材料在同样条件下释放尼美舒利的时间长达22 d,极大延长了药物释放时间,有助于药物的最大化利用。
另外,Li等[57]以外延生长法制备的Fe3O4@Mg-MOF-74磁性纳米复合材料可对人体血清中的糖肽进行选择性捕获。 研究表明,该复合材料可捕获1 μL人体血清中418个糖肽的441个 N-糖基化位点,是目前所报道的所有磁性核壳复合材料中最高的。 他们认为,其对糖肽的高效选择性捕获可能归功于Mg-MOF-74合适的孔径大小和亲水性质。
近年来,MOFs材料在电池方面的应用发展越来越快。 MOFs材料中金属源在电化学反应中可作为氧化还原物质,并且其高的比表面积和孔隙率有利于电子的迁移,同时良好的化学稳定性也促进了电池的循环使用[58]。 金属氧化物@MOFs复合材料加强了MOFs材料的电子传导能力,在电池方面的应用更具有潜力。 Vinogradov等[59]报道的TiO2@MIL-125复合材料可作为太阳能电池的光敏填充材料。 他们发现,当MIL-125摩尔分数占3%时,该复合材料具有最大的光电流响应(39 μA/cm),并且电池的光电转化率也达到了6.4%,同时其在空气中具有极高的稳定性(30 d)。 Sun等[18]首次以层层自组装的方式制备的Fe3O4@HKUST-1复合材料可作为锂离子电池中强稳定性阳极,并表现出优异的电化学性能。 研究表明,在100 mA/g的电流密度下进行100次充放电循环后,其对应的可逆储存容量仍保持在1002 mA·h/g左右。 该研究为设计下一代新型锂离子电池提供了思路。
正如前所述,在金属氧化物与MOFs的协同作用下,复合材料表现出高效的性能。 在催化领域,具有高比表面积和官能性MOFs结合磁性金属氧化物所组成的复合材料是一种可循环利用的高效催化剂;在传感领域,具有规整而均匀孔道结构的MOFs作为分子筛,结合金属氧化物制备出的复合材料是一种高效选择性传感材料;在吸附与分离领域,复合材料结合了高孔隙率MOFs与磁性金属氧化物的特点,并具有MOFs与金属氧化物层之间独特的微孔结构,促使其成为一种稳定的高效吸附分离材料;在生物医药领域,由高载药量MOFs结合磁性金属氧化物形成的复合材料,在交变磁场加热下实现药物定点释放,是一种高效药物释放载体材料[60]。
金属氧化物@MOFs复合材料因巧妙地结合了金属氧化物的特性(如光学、磁学、电学等特性),和MOFs独特的性质(如高比表面积、可调孔径、良好热稳定性等)而逐渐受到研究人员的关注。 从近10年的发展来看,金属氧化物@MOFs复合材料在催化、传感、生物医药和环境保护等相关领域显示出了良好的应用前景,但其工业应用仍然面临着一些挑战:1)在制备方法上,目前的方法步骤繁琐且仅限于实验室合成,因此开发简单高效的工业化生产制备方法具有重要意义。 譬如将制备分子筛或石墨烯材料的合成方法也应用于金属氧化物@MOFs复合材料;2)在功能材料选择上,目前所利用的金属氧化物纳米粒子种类依然偏少且性质较为单一,需要进一步开发具有新颖特性的金属氧化物纳米粒子,并加强其与MOFs材料的有效结合,制备高性能复合材料;3)在复合材料的结构上,目前大部分结构均为核壳结构,需要进一步探索其它新型结构(如中空、分散等结构),以拓展其在工业上的应用。
本文属于开放获取期刊,遵循CCAL协议,使用请注明出处。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|
| [49] |
|
| [50] |
|
| [51] |
|
| [52] |
|
| [53] |
|
| [54] |
|
| [55] |
|
| [56] |
|
| [57] |
|
| [58] |
|
| [59] |
|
| [60] |
|