采用模板导向法和高温固相法制备尖晶石型八面体结构的LiMn2O4锂离子电池正极材料,研究了该材料的结构和电化学性能。 电化学性能研究表明,该电极材料具有良好的循环稳定性和倍率性能,在2.5~4.5 V电压范围,电流密度为100 mA/g时,首周充放电比容量分别为147和179 mA·h/g,循环50周后,其充放电比容量仍分别保持在180/181 mA·h/g。 优良的电化学性能可能归因于尖晶石LiMn2O4的形貌结构特征,该方法为制备锂离子电池正极材料提供了思路和依据。
Spinel LiMn2O4 octahedral nanoparticles were prepared by template-directed and high temperature solid-phase methods as cathode materials for lithium-ion batteries. Their structure and electrochemical performances were investigated. The electrochemical performance results show that LiMn2O4 as lithium-ion batteries cathode displays excellent cycling stability, rate capability and high specific capacity. The initial charge-discharge specific capacities are 147 mA·h/g and 179 mA·h/g at a current density of 100 mA/g and the voltage of 2.5~4.5 V, respectively. The cathode materials retain reversible charge-discharge capacities of 180 mA·h/g and 181 mA·h/g after 50 cycles, respectively. Excellent electrochemical properties may be attributed to the octahedral LiMn2O4 structure. This method is instructive for fabrication and design of excellent electrode materials for lithium ion batteries.
锂离子电池因其能量密度高、循环寿命长和无记忆效应等优点,在便携式电子设备储能电池领域已得到广泛的应用[1,2,3,4]。 随着电动汽车的快速发展,与之配套的锂离子电池需要具有高能量密度、高功率密度、超长循环寿命、成本低及安全性好等特征[5,6]。 锂离子电池性能的提升受其正极材料的影响较大,寻求高性能的正极材料是提升锂离子电池优异性能的重要保障因素。
尖晶石型LiMn2O4因Mn元素自然丰度高,环境友好,制备过程简单,结构稳定,具有稳定的导电、储锂性能及较高放电平台等优点,其作为正极材料具有极大的优势[7,8,9,10]。 但是LiMn2O4在实际应用也存在容量衰减快、高倍率充放电效率低和循环稳定性差等缺点。 这主要是因为在循环过程中,尖晶石型LiMn2O4的八面体因John-Teller效应发生畸变,同时Mn3+歧化溶解,导致电极阻抗增大,容量衰减和循环性能降低[11,12,13,14,15,16]。 为了改善尖晶石型LiMn2O4材料的这些缺点,目前多通过掺杂、包覆、复合等方法来改善其循环性能[11,12,16],但这些方法会导致电极材料中活性材料的比例降低,比容量也随之降低,而材料的电化学性能并不能显著提升[17,18,19,20,21,22,23,24]。
材料的结晶度、晶粒形貌、晶粒大小和晶粒分布等对LiMn2O4材料的电化学性能也具有极大的影响。 优化制备方法,设计具有特定形貌的材料往往显示出优异的电化学性能[25]。 本文采用模板法和高温固相法,以八面体MnCO3为模板,与Li2CO3机械球磨混合后的产物,作为前驱体,经过高温固相煅烧,制备具有模板结构的尖晶石LiMn2O4,并研究其电化学性能。
所用试剂纯度均为分析纯(国药集团化学试剂有限公司),无需进一步纯化或加工;导电炭黑Super P Li(瑞士特密高TIMCAL);聚偏氟乙烯PVDF(法国阿科玛, Mw=1.00×107)。
采用SDT Q600型热重分析仪(TGA,美国TA公司)分析样品失重情况,测试条件为:在空气中,以10°/min的升温速率从室温升高到800 ℃;样品的结构采用D8型X射线衍射仪(XRD,德国Bruker公司)进行测试分析,用Cu靶 Kα辐射线( λ=0.154056 nm),管电压为40 kV,管电流为30 mA,测试角度2 θ在10°~80°范围内;样品的形貌分析采用PHILIP Quanta 200型扫描电子显微镜(SEM,美国FEI公司)进行;高清晰颗粒形貌分析采用Tecnai G20 Philip TEM型透射电子显微镜(TEM,美国FEI公司)进行。 Ar气手套箱(上海米开罗那机电有限公司);CHI660E型电化学工作站(上海辰华有限公司),电压范围为2.5~4.45 V,扫描速率为0.1 mV/s;蓝电CT2001A型电池测试系统(武汉市蓝电电子股份有限公司生产)。
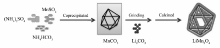
尖晶石型LiMn2O4八面体颗粒采用共沉淀、固相球磨和煅烧3步制备,制备路线如图1所示。 八面体结构MnCO3的制备:10 mmol硫酸锰(MnSO4·H2O)、5 mmol硫酸铵((NH4)2SO4溶解在200 mL水醇混合液中( V(去离子水)∶ V(乙醇)=4∶3)形成A溶液;100 mmol碳酸氢铵(NH4HCO3)溶解在100 mmol蒸馏水中形成B溶液。 然后将溶液B加入溶液A中超声并搅拌30 min,产生沉淀,在继续搅拌4 h。 将沉淀抽滤,并用去离子水洗涤数次,在80 ℃真空干燥后得到八面体结构MnCO3。 尖晶石型LiMn2O4的制备:将八面体结构的MnCO3与Li2CO3按化学计量比在球磨机中球磨2 h,然后将球磨产物在空气氛围下,分别在750、850和950 ℃温度下煅烧3 h(升温速度为3 ℃/min)。 煅烧后的样品即为尖晶石型八面体结构LiMn2O4,分别记为LMO-1、LMO-2和LMO-3。
将制备的尖晶石型LiMn2O4样品、导电剂Super P和粘结剂聚偏氟乙烯(PVDF)按质量比85∶10∶5研磨均匀,加入 N-甲基吡咯烷酮调成糊状,涂布到铝箔上,电极膜片置于真空干燥箱120 ℃干燥5 h,压实并切片成直径为1 cm的电极片。 半电池在手套箱中采用CR2016型扣式电池组装,负极为商品化圆形锂片(直径1.5 cm),隔膜为Celgard 2400聚丙烯隔膜,电解液为1 mol/L LiPF6的碳酸二乙酯(DEC)与碳酸乙烯酯(EC)混合电解液(二者体积比为1∶1),组装成半电池后进行电化学性能测试。
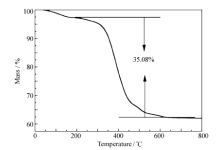
图2为球磨处理后粗产品在空气氛中进行热处理,升温速率为10 ℃/min,热重分析可以看出,失重主要分为两步:第一步是在低于200 ℃时,其归因于水和易挥发杂质约占3.8%,第二步是200~650 ℃之间主要是MnCO3与Li2CO3相互反应,碳酸盐的分解,生成尖晶石型LiMn2O4,失重约为35.08%。在650~800 ℃之间,样品质量基本保持不变,材料稳定存在。
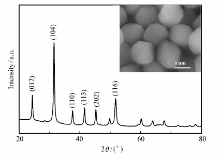
图3为采用共沉淀法制备的前驱体MnCO3的XRD图谱和SEM照片。 从图3可以看出,制备的MnCO3材料为纯相,晶型完美,与MnCO3标准的PDF卡相一致。 材料形貌、颗粒规整,为八面体颗粒,粒径在1 μm左右。
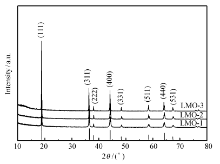
图4是材料LMO-1、LMO-2和LMO-3的XRD图谱。 由图4可见,三者衍射峰位于相同的衍射角度。 主要峰的2 θ位置在18.8°、36.3°、38.1°、43.9°、48.3°、58.7°、64.6°和67.7°处,与标准LiMn2O4的XRD图相(JCPDS 35-0782)比较分别对应于(111)、(311)、(222)、(400)、(331)、(511)、(440)和(531)晶面衍射[9,20,26]。 且无其它杂峰存在,表明烧结产物为尖晶石型LiMn2O4。 随着煅烧温度的升高,过程中氧的失去导致更多的Mn3+的出现,峰形越来越尖锐,表明其结晶度越来越好。
图5A、5B和5C为不同煅烧温度下目标产物LMO-1、LMO-2和LMO-3的SEM照片,图5D及插图分别为LMO-2样品的TEM和HRTEM照片。 由图5D可以看出,LMO-2形貌为八面体,粒径在1 μm左右,随着煅烧温度的升高而增大,材料的颗粒分散的更加均匀,无明显团聚现象。 但温度继续升高到950 ℃时,材料粒径在1~3 μm之间,尺寸显著增大。 从TEM和HRTEM图上可以看出,材料粒径均匀,晶面间距为0.475 nm,对应于尖晶石型的LiMn2O4的(111)面,与XRD结果相吻合[10]。
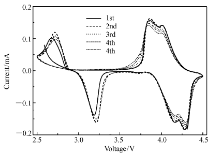
图6为样品LMO-2在2.5~4.5 V电压范围,0.1 mV/s扫速下的循环伏安(CV)曲线。CV曲线中出现了3对氧化还原峰,分别对应于3步反应。
因为LiMn2O4的脱嵌锂过程是一个相变过程,存在两个脱嵌锂电位。 两对氧化还原峰分别为4.15/4.28 V和3.85/4.00 V,是尖晶石LiMn2O4体系的特征峰,对应于Li+在两个不同四面体8a((0,0,0)(3/4,1/4,3/4))位置的脱嵌。 还有一对氧化还原峰电位在2.72和3.21 V,对应于Li+在空的16c((1/8,1/8,1/8)(7/8,3/8,5/8)(3/8,5/8,7/8)(5/8,7/8,3/8))八面体位置的脱嵌。 5次充放电测试之后,峰电位未发生明显的偏移,表明材料具有稳定的氧化还原电化学性能[26]。
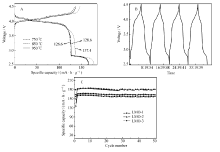
图7则为不同煅烧温度下LiMn2O4在100 mA/g的电流密度下的首周充放电比容量(图7A)以及相应的循环性能(图7B~7C)。 从图7A可以看到,在4.1和4.0 V左右出现LiMn2O4的两对特征充放电平台,对应于反应式(1)和(2)两步电化学反应,通过容量计算(~140 mA·h/g)发现转移1 mol电子。 另一平台在2.7 V,比容量约为70 mA·h/g,对应于0.5 mol电子的转移,峰电位与CV曲线相一致。 其中样品LMO-2电化学性能最优,首周充放电比容量分别为147和170 mA·h/g。
图7B为LMO-2的是电压-时间曲线。 从图7B可以看出,LMO-2具有较好的循环稳定性,在2.75、3.8和4.2 V各有一个放电平台,且2.75 V附近平台非常显著,多次充放电之后,其所有平台电压均未发生显著偏移,表明材料性能稳定,其结果与CV曲线相一致[13]。
图7C为不同煅烧温度下LiMn2O4的循环寿命曲线,对比三者发现,样品LMO-2电化学性能最优,循环50周后,其比容量仍然保持为180 mA·h/g,库伦效率接近100%。无明显衰减现象,表明电极材料具有良好的循环稳定性。
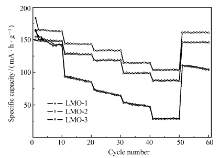 | 图8 不同煅烧温度下LiMn2O4的倍率曲线Fig.8 The rate curves of LiMn2O4 at different calcined temperatures E/V:2.5~4.5 |
图8为不同煅烧条件下LiMn2O4的倍率性能曲线,倍率从0.2 C逐渐增加到5 C,再回到0.2 C。 可以看到随着倍率的增大比容量逐渐降低。 其中,样品LMO-1在大电流充放电时,衰减较为严重,经过大电流充放电后,电流回到0.2 C,其容量保持率仅为67.7%。 LMO-2和LMO-3经过大电流充放电之后,其比容量分别为162和146 mA·h/g,其容量保持率分别为98.5%和96.8%,其中样品LMO-2性能最优,在5 C下电流密度下,其比容量超过100 mA·h/g,说明样品LMO-2在高倍率充放电测试条件下结构稳定,未出现结构坍塌,仍保持较好的尖晶石晶体结构。 与图7得出的结论相一致,均表示在850 ℃煅烧温度下,制备的尖晶石型LiMn2O4材料具有更优越的电化学性能。
由于正极材料的粒径对其电化学性能有一定影响,粒径过大,则比表面积较小,锂离子扩散路径增长;如果粒径较小,容易团聚,反而不利于电化学性能提高。 结合电化学性能分析,850 ℃煅烧温度下的样品其粒径大小合适,均一性好,电化学性能最为优异。
本文通过共沉淀法和机械球磨法制备前驱体,空气中热处理得到尖晶石型八面体结构的LiMn2O4。 煅烧温度既影响材料的结晶度和形貌,又影响材料的电化学性能。 在850 ℃下煅烧得到的LiMn2O4结晶性能好,形貌为八面体且粒径均匀分布在1 μm左右。 XRD图谱表明,LiMn2O4纯度较高、结晶性能好,SEM表明,LiMn2O4形貌为立方体且粒径均匀。 通过电化学性能测试表明,850 ℃煅烧温度下的样品性能最优,首周充放电比容量分别为147和179 mA·h/g,循环50周后,其充放电比容量保持在180和181 mA·h/g,库伦效率接近100%,循环性能稳定且倍率性能优异。 优异的电化学性能归因于尖晶石型LiMn2O4的微结构特征,有效缓解了John-Teller效应导致的容量衰减和Mn3+歧化反应导致的循环性能降低,有利于电化学性能的提高。 该制备方法为制备其它高性能的锂离子电池正极材料提供了一种新的思路。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|