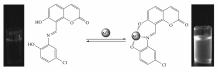
为了方便快捷地检测铝离子,本文以7-羟基香豆素为原料合成了铝离子荧光化学传感器。 通过质谱、核磁共振谱、紫外可见分光光度计等技术手段研究了传感器的结构和性能。 结果表明,该传感器对铝离子有很好的选择性,其检出限为8.5×10-8 mol/L,其识别过程具有可逆性,同时,Job's plot曲线表明二者形成配位比为1:1的稳定配合物。 该研究对生物体及环境领域中铝离子的实时监测具有潜在的应用价值。
For the sake of convenient and quick detection of aluminum ion, an aluminum ion fluorescent chemosensor was synthesized from 7-hydroxyl coumarin. Its structure was verified by mass spectrometry and nuclear magnetic resonance spectrum. The properties and structure of fluorescence chemosensor were characterized by mass spectrometry(MS), nuclear magnetic resonance spectroscopy(NMR), UV-vsisible absorption spectrum(UV-Vis). The results reveal that the sensor has good selectivity toward aluminum ion. The limit of detection is 8.5×10-8 mol/L, and the identification process is reversible. The Job's plot indicates that the sensor and aluminum ion forms stable complex in 1:1 ratio. Therefore, this fluorescent chemosensor has potential in real time monitoring aluminum ion in biological and environmental applications.
铝广泛地存在自然界中,在各种金属元素储量中,位居首位,产量仅次于钢铁[1]。 铝制品的广泛使用使人们经常接触到铝。 此外,土壤酸化会使环境污染中铝离子含量明显地升高[2,3]。 过多地摄入铝会影响人肠胃内钙的吸收,导致软骨病,器官萎缩。 而且对人体的中枢神经系统也会造成伤害,引起帕金森症和老年痴呆症等疾病[4,5]。 因此,需要寻求一种便捷的方法检测环境中铝离子的含量。
传统检测铝离子的方法包括原子吸收、原子发射、电化学分析法及多功能质谱。 这些方法耗时长,对仪器及样品要求高[6]。 相比而言,荧光化学传感器法由于操作简单、灵敏度高、选择性好及费用低等优点受到广大科研工作者的青睐[7]。 本文设计、合成了基于香豆素的荧光化学传感器,表征了其结构与组成,并对铝离子的识别过程和机理进行了探讨。
Bruker Esquire 6000型质谱仪(德国布鲁克公司);Varian Unity INOVA-400型超导核磁共振仪(美国瓦里安仪器公司);UV-2450型紫外分光光度计(日本岛津公司);970CRT型荧光分光光度计(上海仪电科学仪器股份有限公司);X-4型显微熔点测定仪(北京泰克仪器有限公司)。
六次甲基四胺、冰醋酸、盐酸、乙醚、甲醇、无水乙醇、无水硫酸钠(天津科密欧试剂公司);7-羟基香豆素、2-氨基-4-氯苯酚、硝酸锂、硝酸钠、硝酸钾、硝酸铅、硝酸银、硝酸锰、硝酸钡、硝酸汞、硝酸铝、四水合硝酸钙、六水合硝酸镁、九水合硝酸铁、三水合硝酸铜、六水合硝酸镍、四水合硝酸镉、六水合硝酸钴、九水合硝酸铬、六水合硝酸锌(上海阿拉丁试剂公司);以上试剂均为分析纯,实验用水为二次蒸馏水。
荧光化学传感器的合成路线如Scheme 1所示。
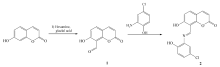 | Scheme 1 Synthesis of the Schiff base of 2-amino-4-chlorophenol with 7-hydroxy-coumarin-8- formaldehyde |
7-羟基-8-醛香豆素(1)的合成 向圆底烧瓶中加入5 g 7-羟基香豆素、10 g六次甲基四胺及50 mL冰醋酸,搅拌,加热回流5~6 h。 然后将75 mL、20%的盐酸溶液加入到反应后的溶液中,60 ℃,加热30 min。 冷却后,用乙醚进行萃取(50 mL×3),合并有机相,无水Na2SO4干燥,浓缩后得到粗产物,无水乙醇进行重结晶后,得到0.93 g淡黄色固体,产率16%。 mp 188.2~188.9 ℃。1H NMR(400 MHz,DMSO- d6), δ:11.90(s,1H),10.41(s,1H),8.01(d, J=9.5 Hz,1H),7.86(d, J=8.7 Hz,1H),6.94(d, J=8.7 Hz,1H),6.37(d, J=9.5 Hz,1H);13C NMR(101 MHz,DMSO- d6), δ:191.25,164.32,159.49,156.08,144.89,136.67,114.34,113.00,111.56,109.55;ESI-MS: m/z 191.2[M+H]+。
2-氨基-4-氯苯酚缩-7-羟基-8-醛香豆素席夫碱(2)的合成 将溶解在无水乙醇中的2-氨基-4-氯苯酚(0.1436 g,1.0 mmol)逐滴加入到含有化合物1(0.1902 g,1.0 mmol)的甲醇溶液中,搅拌回流24 h。 将反应后的溶液减压浓缩至原来的20%,冷却后过滤,用冷的甲醇淋洗3次,得到0.25 g棕红色固体粉末,产率80.5%。 mp 295.4~296.8 ℃。1H NMR(400 MHz,DMSO- d6), δ:15.92~15.07(m,1H),10.47(s,1H),9.32(d, J=1.8 Hz,1H),7.96(d, J=9.5 Hz,1H),7.84~7.55(m,2H),7.21(dd, J=8.6,2.5 Hz,1H),7.00(d, J=8.6 Hz,1H),6.81(d, J=8.8 Hz,1H),6.27(d, J=9.5 Hz,1H),3.34(s,3H),2.51(q, J=1.9 Hz,1H);13C NMR(101 MHz,DMSO- d6), δ:169.45,159.97,155.56,150.06,145.37,134.23,133.16,128.51,123.82,120.00,
118.22,116.52,111.27,109.46,106.50;ESI-MS: m/z 338.1[M+Na]+。
1.3.1 化合物2的选择性
通过条件实验确定所用溶剂为乙醇(pH=7.0,常温),分别配制1.0×10-3 mol/L的Li+、Na+、K+、Ca2+、Mg2+、Mn2+、Ba2+、Fe3+、Co2+、Ni2+、Cu2+、Zn2+、Cr3+,Cd2+,Pb2+,Ag+,Hg2+,Al3+溶液,再配制1.0×10-3 mol/L的化合物2溶液。 向荧光池中加入2 mL的乙醇溶液,然后加入20 μL的化合物2溶液,之后每次加入200 μL的Li+、Na+、K+、Ca2+、Mg2+、Mn2+、Ba2+、Fe3+、Co2+、Ni2+、Cu2+、Zn2+、Cr3+、Cd2+、Pb2+、Ag+、Hg2+和Al3+的金属离子溶液,在荧光分光光度计上测定其荧光强度。
1.3.2 化合物2的光谱滴定
分别进行荧光光谱和紫外光谱滴定,先向荧光池中加入2 mL的乙醇溶液,再加入20 μL的化合物2(1.0×10-5 mol/L)溶液,然后向荧光池中逐次滴加铝离子(1.0×10-3 mol/L)溶液。 分别测定其荧光光谱和紫外光谱。
1.3.3 选择性
理想的荧光化学传感器能够选择性的识别金属离子,而其它金属离子不产生干扰。 实验中先向荧光池中加入2 mL乙醇溶液,再加入20 μL的化合物2溶液,之后每次加入200 μL的Li+、Na+、K+、Ca2+、Mg2+、Mn2+、Ba2+、Fe3+、Co2+、Ni2+、Cu2+、Zn2+、Cr3+、Cd2+、Pb2+、Ag+、Hg2+和Al3+金属离子溶液,记录每次加入不同金属离子后的荧光强度。 最后再加入20 μL的Al3+(1.0×10-3 mol/L)溶液,记录其荧光强度的变化并作出柱状图。
1.3.4 检测限
传感器灵敏度的一个重要方面就是检测限的高低,在实验中,改变Al3+的浓度,测定其吸光度,并研究其线性关系,利用Stern-Volmer方程计算检测限。
1.3.5 可逆性
传感器的显著特征之一就是可逆性,向化合物2溶液中依次加入相同物质的量的Al3+、EDTA和Al3+,在紫外光下观察该溶液的荧光变化及最大发射波长540 nm处的荧光强度,了解可逆性过程。
1.3.6 化合物2与铝离子的配位方式
若确定金属离子与配体L(化合物2)的配位比,可采用Job's plot曲线。 Job's plot实验中,先向荧光池中加入2 mL的乙醇溶液,保持化合物2与铝离子浓度总和不变,调节化合物2与铝离子的不同比例,测出不同比例下的荧光强度,绘制曲线。 再由曲线确定配位比。在紫外光下观察配体L(化合物2)在加入铝离子前后的所产生荧光颜色的变化, 研究铝离子与配体L(化合物2)的结合方式及反应机理。
选择性好坏是传感器性质的一个重要指标。 如图1所示,可知只有Al3+的加入使荧光显著增强,增强幅度达到18倍,Mg2+的加入使荧光稍有增强,而其它金属离子加入后对化合物2荧光
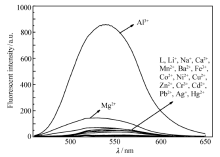 | 图1 化合物2(1.0×10-5 mol/L)乙醇溶液中加入不同金属离子后的荧光光谱Fig.1 The fluorescence spectra of compound 2(1.0×10-5 mol/L) in ethanol with adding different metal ions |
强度的影响不明显,由此说明化合物2对Al3+的识别有很好的选择性。 这可能是由于Al3+与化合物2的杂原子相互配位,阻碍了化合物2的分子内电荷转移和光诱导电子转移过程,从而引起分子空间结构的变化。
2.2.1 化合物2的荧光滴定
如图2所示,化合物2的最大发射光谱在540 nm处,随着Al3+的不断加入,荧光发射强度逐渐增强到18倍,由右上角的插图可以发现当Al3+的浓度增加到1.0化学计量时,荧光强度达到饱和且具有最大值,说明配体L(化合物2)与Al3+是1:1配位的。
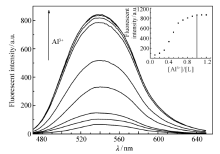 | 图2 在乙醇中化合物2(1.0×10-5 mol/L)随Al3+浓度变化的荧光光谱Fig.2 The fluorescence spectra of compound 2(1.0×10-5 mol/L) in ethanol with Al3+ in various concentrations |
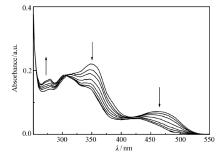
2.2.2 化合物2的紫外滴定
如图3所示,化合物2在350和464 nm波长处出现两个明显的吸收峰,随着Al3+的不断加入,两个峰的强度逐渐降低,在308和420 nm处形成两个等吸收点,这表明化合物2和Al3+形成了具有确定组成的配合物。
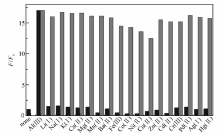
将化合物2在乙醇中的荧光强度看作单位1,纵坐标表示加入各金属离子后荧光强度与化合物2自身荧光强度的比值( F/F0),如图4所示,可以发现Al3+能够竞争过大多数金属离子,尽管Cu2+对荧光有一定的淬灭,但仍然可以区分,因而在其他金属离子共存条件下,化合物2对Al3+的识别具有很好的抗干扰性。
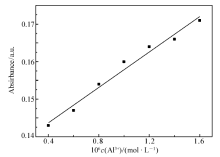
在乙醇溶液中,当Al3+的浓度在0.4×10-6~1.6×10-6 mol/L时,一定浓度的Al3+与1.0×10-5 mol/L的化合物2的吸光度具有良好的线性关系,如图5所示,
拟合线性方程为 y=0.0236 x+0.1343,线性相关系数 r=0.9834,依据Stern-Volmer方程,检测限LOD=3 σ/S,式中, σ为空白溶液紫外吸收强度多次测量的标准偏差, S是灵敏度,即线性回归方程的斜率的绝对值。 计算化合物2对Al3+的检出限为8.5×10-8 mol/L。 表明此化合物能够作为理想的检测Al3+的荧光化学传感器。
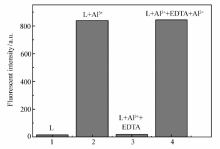
可逆性实验如图6所示,在1.0×10-5 mol/L的化合物2的乙醇溶液中,开始在紫外光下荧光很微弱,仅仅是配体自身微弱的荧光;当向该溶液加入2化学计量 Al3+后,化合物2在540 nm处产生强的荧光强度,该溶液在紫外光下发出明亮的黄色荧光;当再向该溶液加入2 equiv EDTA时,溶液重新恢复为很弱的荧光;当再向该溶液中加入2化学计量 Al3+后,化合物2再次在540 nm出现强的荧光强度,同时该溶液在紫外光下发出明亮的黄色荧光。 上述研究表明,化合物2对Al3+的识别是可逆的。
如图7所示,通过Job's plot曲线可知荧光强度具有最大值时对应的铝离子摩尔比为0.5,说明在乙醇溶液中化合物2与Al3+形成配合物的配位比为1:1。 这一点由荧光滴定实验同样可以证明。 该配体L(化合物2)的发光机理包含了分子内电荷转移和光诱导电子转移两个方面。 由于希夫碱氮原子上孤对电子的存在,它会对吸收的能量进行淬灭和转移从而淬灭荧光,所以用激发光源激发配体时几乎无荧光出现,如图8所示。 然而,随着铝离子的加入,铝离子和配体之间形成了配合物,抑制了分子内电荷转移和光诱导电子转移,氮原子上的孤对电子不能有效传递电荷和能量,所以配合物的荧光强度快速增强,发出明亮的黄色荧光,实现了对铝离子的有效检测。
'>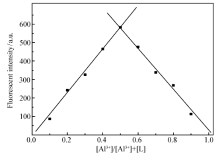 | 图7 乙醇中的Job's plot曲线Fig.7 The Job's plot in ethanol |
设计、合成了新型荧光化学传感器(化合物2),研究了其离子选择性、光谱滴定、竞争性实验、检出限、可逆性实验与配位比测定。 化合物2对Al3+具有很好的选择性,化合物2与Al3+形成有确定组成的稳定配合物,Al3+能够竞争过其它金属离子,并且其它金属离子不产生干扰,检出限为8.5×10-8 mol/L、识别过程具有可逆性、化合物2与Al3+的配位比为1:1。 综上所述,化合物2作为新型荧光化学传感器有着很好的性能,在生物体及环境领域的铝离子检测中具有潜在的应用价值。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|