四嗪类含能化合物因其高能、钝感、高燃速、低压力指数、良好的热安定性等特点被广泛应用于含能材料领域。 然而却存在低密度、低热稳定性的问题,为提高四嗪类化合物的这一性能,制备的一系列金属衍生物得到了广泛关注。 3,6-双(1-氢-1,2,3,4-四唑-5-氨基)-1,2,4,5-四嗪(BTATz)作为四嗪类高氮含能化合物一种,具有良好的催化性能及应用前景。 本文以BTATz钾与硝酸钴在水溶液中反应合成了1,2,4,5-四嗪( s-四嗪)的钴盐。 采用元素分析(EA)、傅里叶变换红外光谱分析(FTIR)及电感耦合等离子体质谱(ICP-MS)对其进行了结构表征,推测其化学式为Co(C4H2N14)·4H2O。 采用差示扫描量热仪(DSC)和热重分析仪(TG/DTG)研究了其热分解行为及主放热反应的动力学方程。 计算了自加速分解温度( TSADT)、热爆炸临界温度( Tb)、热点火温度( TTIT)和绝热至爆时间( tTIAD),其值分别为509.69 K、556.31 K、524.93 K和88.40 s,并以此来评价化合物的热安全性。 该金属盐的绝热至爆时间大于相应的Ca盐、Mg盐和Sr盐,放热量高于配体BTATz,有望成为良好的燃烧催化剂。
Tetrazine compounds have great applications in energetic materials field, which is attributed to its high energy, insensitivity, high burning rate, low pressure and good thermal stability properties. However, they have disadvantages of low density and thermal stability. To enhance the low properties of tetrazine compounds, a series of the tetrazine derivatives have attracted considerable attention. 3,6-Bis(1- H-1,2,3,4-tetrazole-5-amino)-1,2,4,5-tetrazine(BTATz), as a high-nitrogen energetic material, has good catalytic performance and application prospect. Therefore, we synthesized 1,2,4,5-tetrazine ( s-tetrazine) cobalt salt with potassium salt of BTATz and cobalt nitrate in an aqueous solution. Its structure was characterized with elemental analysis, Fourier transform infrared spectrometer(FTIR) and inductively coupled plasma mass spectrometry(ICP-MS). Its chemical formula is Co(C4H2N14)·4H2O. The thermal behavior and thermal decomposition reaction kinetics were also investigated with differential scanning calorimetric(DSC) and thermal gravimetric-differential thermal gravimetric(TG-DTG) methods. The self-accelerating decomposition temperature( TSADT), thermal ignition temperature( TTIT), critical temperature of thermal explosion( Tb) and the adiabatic time-to-explosion( tTIAD) were calculated as the important parameters to estimate the thermal safety, and the value were 509.69 K, 556.31 K, 524.93 K and 88.40 s, respectively. The adiabatic time-to-explosion is longer than those of Ca salt, Mg salt and Sr salt and the exothermic capacity is higher than that of its ligand BTATz. Therefore, it is expected to be a good combustion catalyst.
四嗪类化合物是近年来国内外研究较多的一类高氮化合物,其能量主要来源于其正生成焓,且大多不含硝基基团,感度较低,热稳定性较好;同时分子结构中的高氮、低碳氢含量不仅使其成气量大、燃烧产物少烟或者无烟,且易达到氧平衡。 该类化合物被广泛应用于低特征信号推进剂、气体发生剂、无烟焰火技术等各个领域[1]。
作为四嗪类化合物之一的3,6-双(1-氢-1,2,3,4四唑-5-氨基)-1,2,4,5-四嗪(BTATz)是分子中同时包含四嗪和四唑环的高氮含能化合物,最初由美国Los Alamos国家实验室的Hiskey等合成[2,3]。 因其具有含氮量高(79.02%)、密度高(1.76 g/cm3)及拥有正的生成焓(+883 kJ/mol)等优势引起了国内外研究者的广泛关注[2,3,4,5,6,7,8]。 此后众多的研究者对BTATz进行了进一步的研究,内容涉及到合成工艺的优化和量子化学[3]、燃烧性能[9]、溶解热[10]、BTATz衍生物的合成及性能[11,12,13,14,15,16]、甚至是将其部分替代黑索今(RDX)用于改性双基推进剂(CMDB)中[17]以及形成的BTATz-HNIW-CMDB(HNIW:六硝基六氮杂异伍兹烷)体系的热分解反应动力学机理及热安全性研究等方面[18]。
本文在前期研究[11,12,13,14]基础上,以BTATz钾盐为原料合成了其钴盐,并对其进行了结构表征。 采用差示扫描量热仪(DSC)和热重分析仪(TG/DTG)研究了其热分解行为及热分解反应动力学,并对自加速分解温度( TSADT)、热爆炸临界温度( Tb)、热点火温度( TTIT)和绝热至爆时间( tTIAD)进行计算研究,为其在推进剂中的应用提供必要的理论基础。
BTATz钾盐的制备按照文献[19]方法进行。 其余试剂药品均为分析纯,购自天津市科密欧化学试剂有限公司,使用前未经进一步精制。
X-5型显微熔点测定仪(控温型)(北京泰克仪器公司);VarioELⅢ型元素分析仪(德国艾乐曼公司);EQUINOX-55型傅里叶变换红外光谱仪(KBr压片,400~4000 cm-1)(德国布鲁克公司);Agilent 7700X型电感耦合等离子体质谱仪(美国Agilent公司);比热容测定采用法国(SETARAM)Micro-DSCⅢ型微量量热仪中的连续比热容测定模式进行,测定原理及仪器校正同文献[20];DSC曲线测定选用NETZSCH DSC204型热分析仪,TG/DTG曲线测定选用的SDT Q600型热分析仪(美国TA公司)。
将0.3684 g BTATz钾盐溶于30 mL水中,过滤,滤液于圆底烧瓶中。 逐渐滴加40 mL含有0.5820 g Co(NO3)2·6H2O的水溶液,室温下搅拌。 随着滴加的进行,溶液中出现黑色的沉淀,继续反应1 h后沉淀变为红棕色。 滴加完毕后继续反应6 h后抽滤,滤饼多次水洗后于50 ℃下真空干燥,得到红棕色粉末,产率67%。 反应历程如Scheme 1所示。
元素分析和ICP-MS分析测定值(计算值)/%:C 12.90(12.74),H 2.54(2.67),N 52.20(51.99),Co 13.00(15.63)。 推测该化合物的化学式为Co(C4H2N14)·4H2O。 IR(KBr), σ/cm-1:3519(O—H),3464,3244(N—H),2986,2756,1617(N=N),1530,1471(N—N),1060(C—N),995。
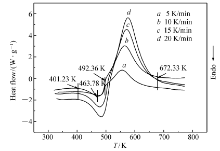
图1为Co(C4H2N14)·4H2O在5、10、15和20 K/min升温速率下的DSC曲线,图2为10 K/min下的TG/DTG曲线。
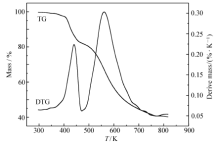 | 图2 Co(C4H2N14)·4H2O在10 K/min的TG/DTG曲线Fig.2 TG/DTG curves of Co(C4H2N14)·4H2O at the heating rate of 10 K/min |
从图1曲线 b可知,Co(C4H2N14)·4H2O的热分解由一个吸热过程和一个放热过程组成,且吸热和放热是连续的。吸热阶段始于401.23 K,终于492.36 K,峰温为463.78 K。 放热阶段始于吸热分解的终点,终于672.33 K,放热量为1152 J/g,该阶段对应TG/DTG曲线(图2)上第2个失重阶段。
TG/DTG图上存在两个失重阶段,第1个失重阶段出现在350~450 K温度范围内,失重率为18%,推测该阶段为失去4分子水的过程(计算值19.1%)。 第2个失重阶段出现在450~800 K,最后剩余残渣45%应为形成的高熔点聚合物。
本文计算热分解动力学参数值的方法主要有Kissinger法[21]、Flynn-Wall-Ozawa法[22]和积分方程法[23]。 通过常用的41种机理函数计算化合物的热分解反应动力学参数。 按照文献[24-25]进行合理地选择计算方法及物质分解反应的动力学参数和机理函数。
表1为在升温速率为5、10、15和20 K/min下由DSC曲线所获得的基本参数值( Te、 Tp值和Δ H)。 采用Kissinger和Ozawa两种方法求得表观活化能( Ea)、指前因子( A)和线性相关系数( r)分别列于表3中。
| 表1 由不同升温速率下的DSC曲线得到的参数值 Table 1 The parameters determined by DSC curves at different heating rates |
| 表2 不同升温速率下由DSC曲线得到的热分解数据 Table 2 Thermal decomposition data determined by DSC curves at different heating rates |
表2是在上述4个升温速率( β)下,放热分解过程任意反应分数( αi)所对应的分解温度( Ti)。 将不同 β对应的 Ti值代入Ozawa方程,计算出各升温速率下的等转化活化能 Ea,并作出对应的 Ea~ α曲线(图3)。 由图3可知,将反应分数 α在0.2~0.8之间时对应的活化能求算数平均值(平均值为150.90 kJ/mol),同时与以 Te, Tp值利用Ozawa和Kissinger所算出的数值相比发现它们较为接近(表3),并且不同方法算出的 A值也接近, r值均大于0.98,表明计算所得结果可信。
'>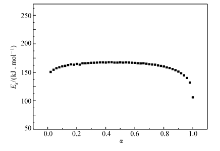 | 图3 不同 β时由Ozawa法得到的 Ea- α曲线Fig.3 Ea- α curve by the Ozawa's method at different heating rates |
| 表3 主要热分解阶段的动力学参数计算值 Table 3 Calculated values of the main stage of thermal decomposition kinetic parameters |
该化合物的主要热分解反应对应37号机理函数,其最可积机理函数的积分式是 f( α) =(1 -α)2,微分式是 G( α) =(1 -α) -1 -1。将 f( α) =(1 -α)2, E=150.90 kJ/mol, A =1011.88 s-1代入方程d α/d t= Af( α) e-E/RT中,得到Co(C4H2N14)·4H2O的热分解反应的动力学方程为:d a/d t=1011.88×(1- α)2×exp(-1.51×105/ RT)。
采用Micro-DSCⅢ微量量热仪测得Co(C4H2N14)·4H2O的比热容方程为:
计算得到298.15 K下的标准摩尔比热容为415.45 J/(mol·K)。 根据方程(1)及热力学函数与比热容的关系式(2)~(4),采用MATLAB[26]软件计算得到Co(C4H2N14)·4H2O基于298.15 K在283~353 K范围内的焓、熵和吉布斯自由能函数值。 所得结果分别列于表4中。
| 表4 Co(C4H2N14)·4H2O的热力学函数 Table 4 Themodynamic functions of Co(C4H2N14)·4H2O |
2.4.1 自加速分解温度( TSADT) 自加速分解温度( TSADT)是[23,27]将不同升温速率下所的到的 Te, Tp值代入到式(5)中,计算 β→0时的峰温 Te0和 Tp0:
式中, n和 m为常数。 根据 TSADT= Te0,可以得到 TSADT和 Tp0。 最后得出 TSADT=509.69 K, Tp0=539.45 K。
2.4.2 热爆炸临界温度( Tb)和热点火温度( TTIT) Tb和 TTIT由式(6)计算得到[23,27]:
式中,当 Eo取 Ep0, T取 Tp0时计算得到热爆炸临界温度 Tb;当 Eo取 Ee0, T取 Te0时即可得到热点火温度 TTIT。
将上述由Ozawa法得到的 Ee0、 Ep0和 Te0、 Tp0代入方程(6)中,计算得到BTATz钴盐的 Tb和 TTIT分别为556.31和524.93 K。
2.4.3 绝热至爆时间( tTIAD) 绝热至爆时间是评价含能物质热稳定性和热安全性的重要参数指标[28,29],其值可根据热分析方法所计算得到的热动力学参数值及比热容方程进行估算。 计算原理如式(7)~(9)所示。
将 Cp=11.36-0.10 T+3.72×10-4 T2-4.11×10-7 T3, E=EK=151.12×103 J/mol, A=AK=1011.95 s-1, Q=Δ Hd=1134.50 J/g, T=Tb=556.31 K, T0 =Te0=509.69 K, f( α) =(1 -α)2代入以上公式,求得绝热至爆时间 tTIAD=88.40 s。
合成了一种新的 s-四嗪含能金属盐——BTATz的钴盐Co(C4H2N14)·4H2O。 采用DSC和TG/DTG方法对其进行了热分解行为和热分解动力学研究。 结果表明,该含能金属盐的热分解过程包含一个吸热阶段和一个放热阶段,采用非等温法获得了放热阶段的热分解反应机理方程为d α/d t=1011.88×(1- α)2exp(-1.51×105/ RT)。 计算了自加速分解温度、热爆炸临界温度、热点火温度及绝热至爆时间分别为509.69 K、556.31 K、524.93 K和88.40 s。 从绝热至爆时间的大小可知,BTATz的钴盐的热安全性优于相应的Ca盐(52.98 s)[30]、Mg盐(45.42 s)[11]和Sr盐(71.93 s)[12]。 从放热量来说,该钴盐在4个升温速率下放热量的平均值为1134.50 J/g(表1)略高于其配体BTATz(1101 J/g)。 而BTATz作为燃烧催化剂已用于双基/改性双基推进剂中,并且显示了良好的催化性能[17]。 由此推断标题化合物有望成为良好的燃烧催化剂。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|