采用水溶液反应法,以不同粘均相对分子质量的聚六亚甲基双胍(PHMB)作为配体,合成出一系列稳定的由400 nm左右的小颗粒团聚而来的微米级四配位Ag(Ⅲ)-PHMB配合物,并对其进行表征证明了物质的结构与价态。 通过抗菌活性实验发现,Ag(Ⅲ)-PHMB配合物的抗菌活性随着配体PHMB的粘均相对分子质量的升高而增大,随着粒径增大而减小。 在低浓度条件下,微米级Ag(Ⅲ)-PHMB配合物的抗菌性能高于同等质量浓度的AgO、AgNO3与PHMB;随着质量浓度的升高,微米级Ag(Ⅲ)-PHMB配合物与细菌的实际接触面积、缓释出的抗菌活性物质增长趋缓,因而抗菌活性升高趋缓。
As the ligand and biological acceptable parts, polyhexamethylene biguanide hydrochloride(PHMB) are used for stabilizing Ag3+. A series of micron-sized quadricovalent cationic Ag(Ⅲ)-PHMB complexes was synthesized via oxidation of the monovalent silver, followed by stabilization of the oxidized high valence silver ions through complexation with PHMB. From the experimental result of agar well-diffusion method, it can be concluded that the antibacterial activity of Ag(Ⅲ)-PHMB complex is enhanced with increasing viscosity-average relative molecular mass of PHMB and weakened with the increase of the size of Ag(Ⅲ)-PHMB complex. The experimental results reveal that the complex yields the maximum antibacterial activity when the viscosity-average relative molecular mass of ligand is 5428. Though broth dilution method, micron-sized Ag(Ⅲ)-PHMB complex displays excellent antibacterial performance in low mass concentration towards Gram-positive and Gram-negative prokaryotes for excellent antibacterial activity of Ag3+. Compared with AgO, AgNO3 and PHMB, Ag(Ⅲ)-PHMB complex has lower minimal inhibitory concentration(MIC). With the increase of mass concentration, however, because of the reduction of the growth ratio of contacting area between Ag(Ⅲ)-PHMB complex and bacteria and the release radio of antimicrobial active substance, antibacterial activity of micron-sized Ag(Ⅲ)-PHMB complex shows slowly increasing rate.
烧伤和烫伤此类的大面积表皮损伤,以及由此引起的脱水、微生物感染、组织损伤及其它并发症严重威胁病人的生命安全[1,2,3,4]。 抗生素的应用使得烧伤、烫伤等大面积表皮损伤危险系数大大降低。 但随着抗生素的选择作用,细菌抗性越来越强,抗生素的研发速度渐渐无法满足临床需求[5]。 银系抗菌剂因其接触杀菌与光催化杀菌作用,并不针对某一定向靶点,使其具有广谱抗菌性能,应用数千年后仍无微生物对其有明显抗性而引起人们的广泛关注[6,7,8]。 银系抗菌剂的抗菌活性与其价态密切相关,价态越高,抗菌性能越强,研究表明Ag3+的抗菌活性是Ag+的200倍,Ag2+的抗菌活性是Ag+的60倍[9,10,11]。 然而,目前应用的银系抗菌剂主要是以磺胺嘧啶银、硝酸银为代表的单价银抗菌剂或纳米银抗菌剂,高价银抗菌剂的研发与应用却鲜见报道。 沈文宁[12]用过硫酸钾或者臭氧为氧化剂,合成AgO,并负载在磁性载体、硅藻土、多孔陶瓷等材料上得到高效抗菌材料;Sukdeb Pal等[17]以氯己定为配体来稳定Ag3+,得到高抗菌活性且耐氯离子的Ag(Ⅲ)-氯己定配合物。
为了将高抗菌活性的银抗菌剂直接应用于人体,采用的方法是与人体相容性好的物质进行配合。 一方面,可以控制银的缓释机制,增强了银抗菌剂的长效抗菌机制,并使其稳定存在;另一方面,最大限度减小银的细胞与组织毒性,降低对环境的污染[13,14,15]。 由于Ag3+极不稳定,目前大多数高价银配合物与氧化物多为Ag2+[16]。最近发现Ag3+与咔咯、卟啉衍生物、亚胺基肟和双胍可以形成配合物或用电化学氧化法得到Ag2O3[16,17,18,19,20,21]。 但是咔咯、卟啉衍生物、亚胺基肟与Ag3+的配合物光稳定性差,且在水中会分解。 双胍与Ag3+形成四配位的阳离子配合物稳定性较好,而且双胍作为阳离子表面活性剂,可以定向吸附在带负电的细菌、真菌等的微生物细胞膜上,通过疏水链来破坏细胞膜使其凋亡而对电中性的动植物细胞膜无害[22]。 聚双胍与双胍相似,同样有共轭单双键,并有π型非定域轨道来稳定Ag3+。 聚六亚甲基双胍(PHMB)与Ag3+进行配合,与小相对分子质量的双胍比较,PHMB有以下优点:PHMB的细胞和组织毒性更小,不会与受试皮肤产生排斥反应;在人体组织和创伤口表面能够保持高抗菌活性;在自然条件下可降解,环境污染更小;且可以直接溶解在水中,不需要做额外的调节;更重要的是,PHMB可以与抗生素协同抗菌[23,24,25,26],到目前为止,这是其它双胍所不具有的性质。
PHMB抗菌性能随粘均相对分子质量的变化略有改变,当其粘均相对分子质量小于1×104时,随粘均相对分子质量的增加,抗菌性能略有上升[26]。 本文以不同粘均相对分子质量的PHMB与Ag3+在水中反应,得到一系列稳定的配合物,并通过抗菌测试得出其抗菌活性变化规律,以期得到最佳抗菌活性的Ag(Ⅲ)-PHMB配合物。
Nova NanoSEM 230型场发射扫描电子显微镜(FESEM,美国FEI公司),AXIS ULTRA DLD型X射线光电子能谱(英国Kratos公司),Nicolet 6700型傅里叶变换红外光谱仪(美国Thermo公司),LA-910型纳米激光粒度仪(日本HORIBA公司)。
无水乙醇(EtOH)、硝酸银(AgNO3)、过硫酸钾(K2S2O8)、磷酸二氢钾(KH2PO4)、磷酸氢二钠(Na2HPO4)、氯化钠(NaCl)、己二胺盐酸盐(C6H18Cl2N2)、氯化钾(KCl)及浓盐酸均为分析纯,购自国药集团化学试剂有限公司;纯度为96%的双氰胺钠(C2N3Na)购自上海麦克林生化科技有限公司;营养琼脂培养基购自杭州微生物试剂有限公司;米勒-海顿(MH)肉汤购自杭州百思生物技术有限公司;大肠杆菌,金黄色葡萄球菌购自广州微生物研究所;自制去离子水。
按照 n(己二胺盐酸盐): n(双氰胺钠)=1:2.1的摩尔比取己二胺盐酸盐和双氰胺钠溶解在正丁醇中,在溶剂沸腾条件下,反应8 h,蒸出溶剂正丁醇,并将所得白色固体1,6-双氰基胍基己烷用水与无水乙醇反复洗涤至熔点在210 ℃以上。
将所得1,6-双氰基胍基己烷与己二胺盐酸盐按照等摩尔比加入到四口烧瓶中,加入少量水,并用稀盐酸调节pH值在6.8左右,使其充分混合。 在55 ℃下,真空除水,待水完全除去用N2气保护并升温至155~160 ℃反应60~180 min,每隔30 min,取样1次,得到粘均相对分子质量在2133、3245、4406、5248和6607的PHMB。
将PHMB溶解在去离子水中,配成质量分数20%的水溶液备用。 在250 mL三口烧瓶中,加入76 mL去离子水,加入880 μL 20%的PHMB水溶液,并搅拌均匀。 在避光条件下,先后慢慢向其中滴加0.04 mol/L的AgNO3 10 mL和0.08 mol/L的K2S2O8 12 mL,用pH=14的NaOH溶液调节pH值在11~12之间,反应16 h。 反应完毕后将离心所得橙棕色固体,用去离子水洗去可溶性杂质,然后在45 ℃下干燥。
1.4.1 不同Ag(Ⅲ)-PHMB配合物抗菌性能测试 测试菌包含革兰氏阴性菌(大肠杆菌)、革兰氏阳性菌(金黄色葡萄球菌),接种在已经高压灭菌的MH肉汤中,在生化培养箱中37 ℃培养4 h,取出后离心分离,在磷酸盐缓冲液(PBS)中重悬浮。 取500 μL PBS,与高压灭菌的液态营养琼脂充分混合。
取Ag(Ⅲ)-PHMB配合物粉末加水配成0.4%的悬浊液,待超声分散均匀后,取5 μL悬浊液涂在先前挖好的直径5 mm的孔洞之中,并在生化培养箱中37 ℃培养24 h,通过抑菌环大小来比较抗菌活性。
1.4.2 最低抑菌浓度法比较不同抗菌剂抗菌活性 为表征Ag(Ⅲ)-PHMB配合物的高抗菌活性,选择配体粘均相对分子质量在3245的Ag(Ⅲ)-PHMB配合物,通过常量肉汤稀释法与AgNO3、AgO、PHMB( Mv=3245)比较抗菌活性大小。
用接种环挑取待测菌并接种在4~5 mL MH肉汤中37 ℃下培养4 h,并用MH肉汤稀释至0.5麦氏比浊度,按照1:100的体积比用MH肉汤将菌悬液稀释备用。
取13支高压灭菌后的试管,第1支试管中加入1.6 mL MH肉汤,其它试管加入1 mL MH肉汤,取配好的质量浓度为1280 mg/L的抗菌原液加入到第1支试管中,并在旋涡混合器上混合均匀后,取1 mL混合液到下一支试管,如此倍比稀释到第11支试管,从第11管中吸取1 mL弃去,第12管和13管为不含药物的生长对照。 取稀释好的菌悬液1 mL,分别加到13支试管中,初始菌液浓度约为5×105 cfu/mL,使得第1管至第11管药物浓度分别为128、64、32、16、8、4、2、1、0.5、0.25、0.125 mg/L。 将试管转移到生化培养箱中37 ℃下培养16~20 h取出,用平板计数法测定细菌浓度。
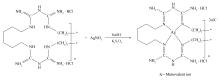
Ag(Ⅲ)-PHMB配合物的合成机理如Scheme 1所示。 在碱性条件下,AgNO3在K2S2O8氧化作用和PHMB四配位条件下,生成高抗菌活性的Ag(Ⅲ)-PHMB配合物。
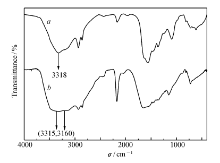
图1是粘均相对分子质量为2133的PHMB与配体粘均相对分子质量为2133的Ag(Ⅲ)-PHMB配合物的红外吸收光谱。 从图中可以看出,Ag(Ⅲ)-PHMB配合物在—N(H)—处的吸收峰只有3318 cm-1处有吸收峰,PHMB在3315和3160 cm-1有2处吸收峰,说明Ag3+与PHMB通过—N(H)—进行配合,说明有配合物的生成。
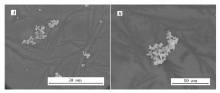
图2是Ag(Ⅲ)-PHMB配合物的SEM照片。 可见,微米级Ag(Ⅲ)-PHMB配合物是由许多纳米级形状规整的颗粒团聚而形成的。 用Nano Measurer进行对纳米颗粒粒径分布计算知其粒径在400 nm左右。 纳米级配合物在成核与生长过程中,不断与其它颗粒碰撞,随机组合在一起,形成没有固定形貌的微米级Ag(Ⅲ)-PHMB配合物。
取少量Ag(Ⅲ)-PHMB配合物的悬浊液用纳米激光粒度仪测试其粒径分布如图3所示。 从图中可以看出,随着配体PHMB粘均相对分子质量的升高,Ag(Ⅲ)-PHMB配合物的粒径分布范围变化不大,随着配体PHMB粘均相对分子质量的升高,Ag(Ⅲ)-PHMB配合物的数均粒径分别为3.81、5.05、7.29、8.61和10.44 μm。 结合Ag(Ⅲ)-PHMB配合物的SEM照片分析可知,随着PHMB粘均相对分子质量的增大,纳米级Ag(Ⅲ)-PHMB配合物颗粒单体逐渐增大;纳米级颗粒在碰撞过程中,随机与其它颗粒团聚,形成无固定形貌的微米级Ag(Ⅲ)-PHMB配合物。 由此可以推断出,在温度,浓度和搅拌速度固定的条件下,配合物粒径增长原因在于纳米级颗粒粒径的增长;配体PHMB的粘均相对分子质量大小不会影响到微米级 Ag(Ⅲ)-PHMB配合物的形貌,微米级颗粒形貌的主要影响因素是温度、浓度和搅拌速度。
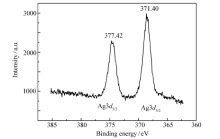
银的氧化态可以通过银XPS谱图的结合能加以区别[17,18]。 为测定配合物中银的氧化态,用多功能X射线光电子能谱,使用短波长Mg Kα X射线(1253.6 eV),分谱通能20 eV,分辨率为0.1 eV的X光对所得到的配体粘均相对分子质量为2133的Ag(Ⅲ)-PHMB配合物进行扫描,结果如图4所示。 配合物中Ag3 d3/2和Ag3 d5/2的结合能的峰出现在371.40和377.42 eV附近,说明配合物中的银为+3价。
2.4.1 不同Ag(Ⅲ)-PHMB配合物抗菌性能测试 在PHMB粘均相对分子质量小于1×104时,其抗菌性能随着相对分子质量的升高缓慢增强[26],不同粘均相对分子质量的PHMB与Ag3+的配合物通过琼脂孔洞扩散法得到对大肠杆菌和金黄色葡萄球菌的抑菌环的抗菌结果如图5所示,按照顺时针方向,配体PHMB的粘均相对分子质量逐渐增大,具体抑菌环尺寸如表1所示。 从Ag(Ⅲ)-PHMB配合物对大肠杆菌与金黄色葡萄球菌的抗菌结果来看,当配合物PHMB的粘均相对分子质量小于5428时,Ag(Ⅲ)-PHMB配合物的抗菌性能随着配体PHMB粘均相对分子质量的升高而增大,当配体PHMB粘均相对分子质量在5428时达到最大,对大肠杆菌的抑菌环为9.62 mm,对金黄色葡萄球菌的抑菌环为9.16 mm。 而PHMB粘均相对分子质量到6607时,其抗菌性能不再增加,并稍有下降趋势,结合对Ag(Ⅲ)-PHMB配合物的粒径分析可知,随着粒径增大,Ag(Ⅲ)-PHMB配合物与细菌的接触面积减小,影响到抗菌活性因子的释放,进而使抗菌活性减弱。
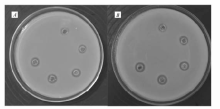 | 图5 Ag(Ⅲ)-PHMB(3245)配合物对金黄色葡萄球菌( A)和大肠杆菌( B)的琼脂孔洞扩散法抑菌结果Fig.5 Photographs of bactericidal activity of Ag(Ⅲ)-PHMB(3245) complex against S.aureus( A) and E.coli( B) |
| 表1 不同Ag(Ⅲ)-PHMB配合物对大肠杆菌和金黄色葡萄球菌的抑菌环 Table 1 Inhibition zone of Escherichia coli and Staphylococcus aureus for different Ag(Ⅲ)-PHMB complex |
2.4.2 最低抑菌浓度法比较不同抗菌剂抗菌活性 通过平板计数法精确测定常量肉汤稀释法中金黄色葡萄球菌的初始浓度为4.3×105 cfu/mL,大肠杆菌的初始浓度为5.6×105 cfu/mL,结合图4中的细菌计数曲线分别得到PHMB( Mv=3245)、AgNO3、AgO、Ag(Ⅲ)-PHMB( Mv=3245)配合物的最低抑菌浓度(MIC)与最低杀菌浓度(MBC),如表2所示。
| 表2 Ag(Ⅲ)-PHMB配合物、AgNO3、AgO、PHMB的最低抑菌浓度(MIC)和最低杀菌浓度(MBC) Table 2 Minimal inhibitory concentration(MIC) and minimum bactericidal concentration(MBC) of Ag(Ⅲ)-PHMB complex, AgNO3, AgO and PHMB |
图6为常量肉汤稀释法,比较Ag(Ⅲ)-PHMB配合物,AgNO3、AgO和PHMB对大肠杆菌与金黄色葡萄球菌抗菌性能随浓度变化曲线。 从图中细菌浓度随抗菌剂浓度的变化曲线可以看出, Ag(Ⅲ)-PHMB配合物的抗菌性能在低浓度时高于同等质量浓度的AgNO3、PHMB和AgO,Ag(Ⅲ)-PHMB配合物对大肠杆菌和金黄色葡萄球菌的MIC均小于AgNO3、PHMB和AgO的MIC。 在同等质量浓度的条件下,银的价态越高,抗菌性能越强[9,10,11]。 但随着浓度的继续上升,Ag(Ⅲ)-PHMB配合物和AgO的抗菌性能增加速度不及AgNO3和PHMB,Ag(Ⅲ)-PHMB配合物和AgO在水溶液中溶解度低,会在试管底部形成沉淀。 AgNO3可以溶解在水中,使得AgNO3的抗菌活性增长速度高于Ag(Ⅲ)-PHMB配合物和AgO,当测试菌为金黄色葡萄球菌,AgNO3浓度为11.71 mg/L;测试菌为大肠杆菌,AgNO3浓度为11.55 mg/L时抗菌性能超过Ag(Ⅲ)-PHMB配合物。 由此推断,随着质量浓度的升高,与AgNO3相比,微米级的Ag(Ⅲ)-PHMB配合物与细菌的有效接触面积增长缓慢,缓释出的抗菌活性物质少,抗菌活性随浓度升高增长较慢。
 | 图6 常量肉汤稀释法测得的大肠杆菌( A)和金黄色葡萄球菌( B)细菌计数结果图Fig.6 Bactericidal activity against E.coli( A) and S.aureus( B) using constant broth dilution method a.PHMB; b.AgO; c.Ag(Ⅲ)-PHMB; d.AgNO3 |
PHMB作为阳离子表面活性剂,能够定向吸附在带负电的细菌细胞膜或者细胞壁表面,取代Ca2+和Mg2+,破坏细菌细胞的运输系统,PHMB的疏水的六甲撑在桥接到细胞膜上时不会变形,导致磷脂质的重新排布,最终使细胞膜破裂[26,27];银离子通过库仑力吸附在细菌表面,破坏细菌的运输系统的同时,与细菌蛋白质的S—H结合,破坏蛋白质三维结构,且银离子价态越高抗菌性能越强[9,10,11]。 Ag(Ⅲ)-PHMB配合物集合了二者的优点,有更强的抗菌效果。
本文应用不同粘均相对分子质量的聚六亚甲基双胍(PHMB)作为配体,在水中调控pH值在11~12,反应16 h,得到一系列由形状规整的400 nm左右四配位的Ag(Ⅲ)-PHMB配合物团聚而来的无固定形貌的微米级颗粒。 随着配体PHMB粘均相对分子质量的上升,纳米级Ag(Ⅲ)-PHMB配合物粒径逐渐增大,团聚而来的微米级Ag(Ⅲ)-PHMB配合物粒径也逐渐增大;微米级颗粒的形貌主要与搅拌速度,温度和浓度相关,与配体的粘均相对分子质量无关。 微米级Ag(Ⅲ)-PHMB配合物结合了PHMB与Ag3+的抗菌优势,抗菌性能与Ag3+,PHMB粘均相对分子质量和粒径分布相关,且随着配体PHMB粘均相对分子质量的升高而增大,随着配合物粒径增大而减小。 通过常量肉汤稀释法比较可以看出,受到粒径和溶解度的限制因素, Ag(Ⅲ)-PHMB配合物的抗菌性能只在低浓度条件下高于同等质量浓度的AgNO3、PHMB和AgO;因此今后深入合成更小粒径的Ag(Ⅲ)-PHMB配合物可进一步提高其抗菌活性。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|