传统超级电容器受低能量密度的限制,在当今器件研发中需更加关注电极材料结构-组成-性能研究。 本文总结了新型赝电容器的发展历程及其研发过程中存在的挑战与解决措施,着重从胶体离子超级电容器电极材料等新型的电极材料和氧化还原电解质两个方面进行综述。 原位合成的胶体离子超级电容器电极材料比非原位合成的电极材料具有更高的反应活性,并且以近似离子的状态存在,有效增加了电极材料的比容量。 氧化还原电解质的使用在不改变电极材料的前提下,进一步提高了超级电容器的能量密度。 初步介绍了新型锂离子电容器。 锂离子电容器同时使用电池型材料和电容型材料,可提高其能量密度。 依据当前超级电容器的研发现状,未来有望将电池材料和电容器材料结合使用,进而形成电池电容器或电容电池,使其同时具有高的能量密度和功率密度。
Traditional supercapacitors have low energy density, which in most cases hinders their further practical applications, therefore, people more focus on studies of the structure-composition-property relationship of electrode materials towards high performance supercapacitors during present research and development of electrochemical energy storage devices. This article summarizes the history of research and development of novel supercapacitors, as well as their challenges and strategies, with the aim to find novel supercapacitor systems via searching for high efficient electrode materials and electrolytes. Novel electrode materials and redox electrolytes are thus particularly emphasized herein, for example, some promising electrode materials of colloidal ion supercapacitor systems have shown some advantages compared to those ex-situ prepared electrode materials, which indicates high electrochemical reactivity existing in the colloidal state of constituent transitional and rare earth metal cations. Furthermore, we also introduce novel lithium-ion supercapacitors as some promising research and development directions. On the basis of the current status of research and development of supercapacitors, it is highly expected to combine the advantages of both battery electrode materials and supercapacitor electrode materials towards the so-called supercapattery or supercabattery, which may be dominant in the field of future electrochemical energy storage devices.
超级电容器是通过电极材料的离子吸附与脱附或快速的表面氧化还原反应来实现能量存储的高功率密度器件[1]。 其充、放电迅速,在几秒至几分钟内即可完成;具有高功率密度,可达500~10000 W/kg;一般大于50万次的循环寿命[2];工作温度范围比电池宽,它可以在-40 ℃条件下正常使用;并且超级电容器在高功率充放电时比电池更安全[3]。 但是,超级电容器存储的电荷量比电池低3~30倍,它的低能量密度限制了其广泛应用[4]。 针对智能电网调频的运行工况以及规模化应用需求,急需完成超级电容器的基础理论、关键材料、应用与评价技术研究,开发出具有高比能量、长寿命、低成本的功率型储能器件,实现超级电容器储能系统在电网调频中的应用。 截止目前,超级电容器已成功应用于电动大巴、轨道交通、能量回收、电能质量调控等方面[5]。
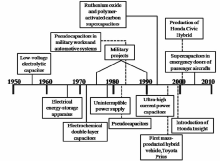
图1展示了超级电容器发展的几个重要的里程碑[6]。 1957年,美国通用公司申请了第一个低电压双电层电容器的专利[7]。 1969年,SOHIO第一次尝试将电化学电容器推向市场[8]。 在Conway等发表第一篇有关赝电容性RuO2膜的文章之后,1975年,Ottawa小组和Continental集团合作首次研发了RuO2商业电化学电容器[9]。 在20世纪90年代,俄国的非对称水溶液体系超级电容器C/Ni(OH)2的出现使得能量密度进一步提升,其能量密度大于10 Wh/kg,但功率密度不到1000 W/kg,充电时间约需10 min[4,10]。 90年代后期,电化学电容器广泛应用在混合电动汽车领域。 美国能源部于1989年发起超级电容器的发展计划,1998~2003年的短期目标为功率密度达到500 W/kg的同时能量密度达到5 Wh/kg,2003年之后的长期目标为功率密度达到1500 W/kg的同时能量密度达到15 Wh/kg[11]。 2014年,IDTechEx市场调研公司预测:超级电容器的能量密度现阶段目标为35 Wh/kg,下一个10年,在其它参数能实现的条件下,能量密度达100 Wh/kg,最终可能实现500 Wh/kg,是最好的锂离子电池能量密度的2~4倍[12]。 在电池电容器体系中可以实现500 Wh/kg,既具有电池的高能量密度又具有电容器的高功率密度。 到2024年,超级电容器的全球市场价值将达到65亿美元[12]。
超级电容器的低能量密度,是其发展过程中存在的主要挑战。 根据能量密度的计算公式 E=CU2/2(式中, U为单体的电压区间, C为单体的比容量)可知,提高超级电容器的能量密度,可以从提高电压区间和比容量两个角度考虑。 电压区间主要由电解液的分解电压决定,比容量主要由电极材料决定。 水系电解液分解电压约为1.2 V,有机电解液分解电压一般为3.5 V,离子液体电解液分解电压为4.5 V[13]。 对于电极材料来说,可以通过改变电极材料的组成、晶体结构和微结构来提高比容量[14]。 许多电极材料使用时需要添加导电剂,以改进电子从体相导出的问题,例如碳材料。提高单体的能量密度,可以用比容量大的电极材料进行匹配,组成非对称超级电容器,也可以引入氧化还原电解质来实现。
超级电容器常见的电极材料有碳基材料、金属氧化物和导电聚合物。 高电化学活性电极材料的研发是实现超级电容器高能量密度和高功率密度的重要措施之一。 最近,薛冬峰研究小组[15,16,17,18,19,20,21,22,23,24,25,26,27]制备了胶体离子电极材料,例如,FeCl3原位制备的Fe2O3·H2O胶体,在2 mol/L KOH电解液中,3 A/g的电流密度下可产生977 F/g的容量[18]。 CoCl2胶体电极在2 mol/L KOH电解液中,1 A/g的电流密度下可产生1962 F/g的容量[20]。 这种新型电极材料合成过程简单,它由商用的稀土盐或过渡金属盐在碱性电解液中通过循环伏安法进行电化学原位合成,所用的盐发生了化学和电化学辅助共沉淀进而形成活性物质,原位合成活性胶体环境与电容性能测试环境一致,均在碱性电解质中进行,因而具有很高的电化学活性。 胶体离子电极材料是最近研究的一种新型的赝电容类超级电容器电极材料,该材料能够充分利用多价态金属阳离子的多电子氧化还原反应,产生更高的比容量,从而提高超级电容器的能量密度。 由于胶体离子的存在,缩短了电子、离子的扩散距离,加快了氧化还原反应的速度,从而保持高的功率密度[15]。 过渡金属元素往往具有多个氧化态,并且相应化合物具有不同的结晶相和形态,因此过渡金属元素在设计和发展新颖功能无机材料方面具有重要的应用价值。 目前,钛、钒、铬、锰、铁、钴、镍等过渡金属基氧化物、氢氧化物、硫化物等作为超级电容器电极材料被广泛研究[16]。 薛冬峰研究小组[17]近期研发出稀土阳离子和过渡金属阳离子胶体电极材料。 目前使用的胶体阳离子主要是一些多价态的金属阳离子,例如Fe3+[18,19]、Co2+[20]、Ni2+[21]、Mn2+[22]、Cu2+[23]、Sn4+[24]、Ce3+[25]、Yb3+[26]和Er3+[27]等,还可从单一阳离子发展到双阳离子胶体电极材料。 胶体离子电极材料因为其尺寸很小,主要以分散的胶体粒子形式存在,其比表面积比传统的电极材料增加了许多,活性物质的利用率显著提升,因而增加了电极材料的比容量,从而可以提高超级电容器的能量密度。 在电化学反应中,识别出活性物质的存在形式对研究电极反应机理和提高比容量具有重要价值。 在胶体离子超级电容器电极材料中,活性物质主要以准离子态的胶体形式存在,为了更准确的核算以及更好的探究金属阳离子的利用率及其电化学反应机理。 薛冬峰研究小组[28]提出了以阳离子为标准核算比容量,并与传统的以氢氧化物和氧化物为标准的核算方式进行了比较,最终结果证明以离子形式核算比容量的方式,可以很容易地判断出超级电容器中电极材料发生的是单电子还是多电子法拉第反应。 在胶体离子电极反应的过程中,可以发生多个电子的反应,因此胶体离子电极材料通常产生高出一个电子反应的比容量,表明胶体离子超级电容器电极材料在提高能量密度方面具有潜在优势,有望突破现有电化学储能器件难以同时具备高功率密度和高能量密度的技术瓶颈,开发出下一代高性能储能器件。
但在现有的胶体离子电极材料体系中,还存在着一些需要克服的挑战,例如,高电化学活性的胶体离子电极材料其循环稳定性还有待提高。 为了提高胶体离子电极材料的循环稳定性,需要研究电极界面反应动力学行为,发展表界面调控策略,考察表界面演化机制。
超级电容器的电解质分为液体电解质和固体电解质,液体电解质使用的溶剂要求包括:宽的电压窗口、高电化学稳定性、低电阻率、低粘度、低挥发性、低毒性、低成本以及可以高度纯化[13]。 氧化还原电解质的引入能够大幅度地增加超级电容器的比容量和能量密度,因而引起了国内外的广泛关注。
当前,涉及氧化还原电解质的超级电容器,仍存在以下3个问题[29]:使用电容来描述电荷存储能力的有效性;含有氧化还原电解质的超级电容器的性能度量;电荷存储能力提高的机理。
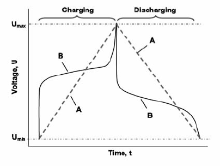
使用电容来描述电荷存储能力的有效性:图2给出了传统超级电容器和含有氧化还原电解质的超级电容器的恒流充放电曲线的比较[29]。 传统超级电容器的充放电曲线如图2A所示为线性的;含有氧化还原电解质的超级电容器的充放电曲线为非线性的。 在恒流充放电条件下,这两条曲线有相同的电荷总量(Δ Q),相同的电压区间(Δ U)。对于充电或者放电过程,有相同的Δ Q/Δ U比率。 对于线性的图2A来说,Δ Q/Δ U比率是其电容,但是对于图2B曲线来说,相同的Δ Q/Δ U比率并不是其真正的电容。 恒流充放电测试对于测试器件存储或者释放的能量是非常重要的。 对于恒流充电过程或者是恒流放电过程,均可以用下面的公式来计算存储或释放的能量。
对于 U( t)是线性的函数,该公式可以简化成以下形式:
式中, C是曲线斜率, U是电压差。
因此,对于恒流充放电曲线为非线性的,不适合用斜率计算电容,可以先算出积分面积,再求出对应的电容。
含有氧化还原电解质的超级电容器的性能度量:氧化还原电解质的使用能够增加超级电容器的电荷存储能力,但是很少有报道考虑了氧化还原电解质作为活性物质对电容器容量的贡献。 为了准确地比较电荷存储能力,考虑氧化还原电解质作为器件活性物质的一部分是十分必要的。
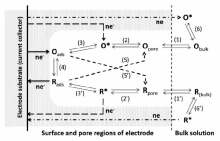 | 图3 在氧化还原电解质中超级电容器多孔碳电极的电荷存储机理图[29]Fig.3 Illustration of charge storage mechanisms in the porous carbon electrode of a supercapacitor with a redox electrolyte[29] |
电荷存储能力提高的机理:超级电容器有两种电荷存储机理—双电层电容和赝电容。 但是,对于引进了氧化还原电解质的超级电容器来说,电荷存储能力提高的机理更为复杂。 这里的氧化还原电解质指的是可以提升超级电容器充放电性能的同时本身不被消耗。 在图3中,O和R是电解液中氧化还原电对的氧化态和还原态。 为了参与电荷存储的过程,溶液体相里的氧化还原电对需要首先扩散至电极材料的孔里,这个过程可以用步骤(1)或(1')来解释,它表示氧化还原电对进入或离开孔时,去溶剂化和溶剂化的平衡过程。 在传统的电极反应里,发生电子转移反应之前,孔里面的氧化还原电对必须通过步骤(2)或(2')达到过渡态(O*或R*)。 步骤(3)和(3')表示从过渡态转变到吸附态(Oads和 Rads)的过程,这个过程在传统的电极反应里可能并不存在,但是对于可以很好保持容量的具有氧化还原电解质的超级电容器来说是十分必要的。 因为集流体表面吸附态的氧化还原电对可以迅速地参与反应,并且不容易溶解到体相电解液里,使得容量能够很好的保持,因而从过渡态到吸附态的过程是很重要的。 步骤(4)过程发生的电子转移会造成吸附在电极内外表面的氧化还原电对的氧化态和还原态之间进行迅速地转变,这个过程是电荷存储能力提升的直接原因。 氧化还原电对(O*和R*)一旦处于过渡态,可能没有进行吸附就直接与集流体之间发生电子转移反应。 也可能是被吸附的电对(Oads或 Rads)通过步骤(5)或(5')发生电子转移反应,形成一种能够通过孔并且能进入体相电解液的可溶产物(Opore或Rpore)。 这两种情况下,如果是充电过程,充电产物溶解到体相电解液中,那么电化学过程不是完全可逆的。 另外电子转移不仅发生在孔的内部,也通过步骤(6)或(6')的过程发生在电极的外表面。 对于多孔电极材料来说,因为其外表面积通常比内表面积小得多,所以步骤(6)或(6')起到的作用是不明显的。 因此,在超级电容器里想要充分利用氧化还原电解质的电荷存储能力,电极材料必须具备能够容纳氧化还原电对的合适多孔结构。
利用氧化还原电解质来增强电荷存储能力的常见机理[29]:1)利用电极表面电吸附的阴离子来增强电荷存储。 通过调节电极材料中的孔体积和尺寸分布、比表面积和表面官能团,有利于氧化还原电对的电吸附,从而增强电荷存储能力。 例如,活性炭和碘化钾、溴化钾之间,活性炭吸附碘离子、溴离子增加电荷存储能力。 2)利用过渡金属阳离子的化学吸附增强电荷存储。 功能化的电极表面的阳离子亲和性的基团可能化学吸附阳离子。 众所周知,碳原子的边缘部位比固体碳内部有更高的反应活性,这些边缘部位可以容易地被氧化形成各种含氧基团,如—OH和—COOH,这些表面含氧基团可以化学吸附金属阳离子从而使表面能够发生氧化还原反应。 例如,功能化碳表面化学吸附CuCl2-HNO3电解液中的铜离子[30]。 3)通过氧化还原电解质和电极材料之间的电子转移来增强电荷储存。 具有氧化还原活性的电极材料与氧化还原电解质之间可以发生直接的电子转移。 氧化还原电解质的参与增加了电极材料转移的电子数。
因此,涉及氧化还原电解质的超级电容器应该与传统的超级电容器分开考虑与解释。 同时,需要进一步研究器件的物理化学现象与相应的电性能之间的联系。
表1展示了氧化还原电解质的部分研究情况。 以活性炭为电极材料的C/C双电层电容器为例,电解质为LiClO4时,超级电容器的能量密度为17.77 Wh/kg,加入对苯二胺(PPD)后,电容器的能量密度高达54.46 Wh/kg,提高了2倍多[31]。 电解质为KOH时,超级电容器的能量密度为4.46 Wh/kg,加入PPD后,电容器的能量密度高达19.86 Wh/kg,提高了3倍多[32]。 电解质为KOH时,超级电容器的比容量为36.43 F/g,加入间苯二胺(MPD)后,超级电容器的比容量为78.01 F/g,提高了1倍多[33]。 电解质为KOH和聚乙烯醇(PVA)时,超级电容器的比容量为135.93 F/g,加入KI后,超级电容器的比容量为236.90 F/g,提高接近1倍[34]。 电解质为KOH时,超级电容器的比容量为165 F/g,电解质为K4[Fe(CN)6]时,超级电容器的比容量为272 F/g,提高接近1倍[35]。表1的结果说明氧化还原电解质能够大幅度地增加超级电容器的比容量和能量密度。
| 表1 有代表性的氧化还原电解质对部分电极材料及超级电容器的影响 Table 1 Improved performance of partial electrode materials and specific capacities(SCs) through some typical redox electrolytes |
现有的氧化还原电解质体系包括水和有机试剂为溶剂的电解液以及离子体液。 水系电解液可以提供更高的离子浓度和更低的电阻。 并且水系电解液制备和使用时不需要苛刻的环境条件。 但是,水系电解液的最大缺点是具有较窄的工作电压,大约为1.2 V[13]。 较低的工作电压主要受限于水的分解电压1.23 V。 因此,根据能量密度的计算公式可知,水系电解液因为其工作电压比较窄,限制了能量密度的提高;有机电解液可以提供高达3.5 V的工作电压,这是其巨大的优势。 乙腈和碳酸丙烯酯(PC)是最常用的溶剂,乙腈可以比其它溶剂溶解更大量的盐,但是存在沸点低和毒性大等问题,基于PC的电解液是对环境友好的、可以提供宽的工作电压窗口、宽的工作温度范围以及良好电导率。 但是,有机电解液的水含量必须低于百万分之3~5,否则,应用有机电解液的超级电容器的电压将显著减小[13];离子液体是在所需的温度下可以以液体形式存在的无溶剂的有机盐[13]。 盐可以被熔化,即“液化”,通过给系统提供热量去平衡盐的晶格能,这样的系统被称为熔融盐或离子液体。 离子液体具有低的蒸气压、较高的热稳定性、化学稳定性、低的可燃性和宽的稳定的工作电压,从2~6 V,典型的约为4.5 V[36]。 但是,离子液体的粘度高,导致处理困难。室温下电导率比水系电解液低许多。这些缺点限制了离子液体在超级电容器中的应用。
既具有电池的电化学特性又具有超级电容器的电化学特性,电容性能主导时叫做电池电容器,电池性能主导时叫做电容电池。 电池电容器概念的提出是用来描述兼具超级电容器和电池电荷存储机理的混合体系,可以是电极材料水平也可以是器件水平的混合[29]。 在电极材料水平,电极材料是由双电层储能材料和氧化还原反应储能材料组成的纳米结构复合材料,例如,碳纳米管和二氧化锰纳米复合材料[37]。 如图4 C所示,电池电容器的一个电极材料的电压随充放电时间进行非线性变化,表现出电池特性,另一个电极材料的电压随充放电时间进行线性变化,表现出电容特性,但器件整体的电压随充放电时间进行近似线性变化。 电容电池中,既有电池类电极又有电容类电极,混合器件性能更像电池。
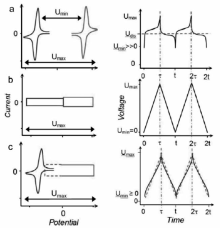 | 图4 储能器件的电化学特性示意图[29]Fig.4 Schematic illustration of the electrochemical characteristics of batteries(a), supercapacitors(b) and supercapatteries(c), represented by the cyclic voltammograms(left) and galvanostatic charging and discharging plots(right)( Udis:Average discharging voltage)[29] |
锂离子电容器是一种先进的非对称超级电容器,它具有电池和传统双电层电容器的功能,可以在比传统的双电层电容器多存储5~10倍的能量同时具有高功率和长循环寿命等优点[38]。 典型的锂离子电容器以高比表面积的活性炭为正极,能够支持锂离子快速可逆地嵌入和脱出的石墨、软硬碳、或其它材料为负极。 在锂离子电容器充电过程中,锂离子嵌入到负极材料的体相中,而阴离子在正极材料的表面发生吸附。 在放电过程中,锂离子从负极材料体相中脱出,而阴离子在活性炭正极材料的表面发生脱附[36]。 因此,锂离子电容器可以保证高功率密度,同时具有较高的能量密度。
传统超级电容器受低能量密度的限制,在当今器件研发中需更加关注超级电容器的基础理论和关键电极材料研究,可以使用新型的胶体离子超级电容器电极材料和氧化还原电解质来提升超级电容器的能量密度。 挖掘“材料结构-组成成分-电化学性能”之间的构效关系,阐明离子在体相和界面中输运机理,建立实验模型,优化材料体系,创新单体设计,开发高比能量、长寿命、低成本的超级电容器。 依据当前超级电容器的研发现状,未来有望将电池材料和电容器材料结合使用,构建电池电容器或电容电池。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|