设定了Visual minteq软件 F--Al3+体系的物种及平衡常数。 模拟滴定和实验滴定结果的相似性证明了软件设定的合理。 对F-(0.01/0.1 mol/L)-Al3+ (0.02 mol/L)-OH-体系的模拟和分析表明,当F与Al摩尔比相差大时,体系平衡物种分布不同,OH-掩蔽铝的机理也不同,但是在pH值11~12铝都被成功掩蔽;不同的反应机理导致F与Al摩尔比大的体系模拟和滴定曲线差别较大。 进一步模拟得到了此pH值区间的最大可掩蔽铝浓度。 考虑OH-对氟离子电极的影响,最终确定高氟(0.01~0.1 mol/L)高铝体系氟的测定条件:控制pH值为(11.5±0.2),不大于0.02 mol/L的铝。 误差分析表明,当电势测定误差较大时,标准曲线法比标准加入法误差小。
The species and equilibrium constants were assigned for F--Al3+ system in Visual MINTEQ software. The similarity between the simulated titration curves and experimental ones, and the accordance confirms this assignment. The masking effect of sodium hydroxide and masking mechanism was investigated according to the equilibrium distribution simulation of F-(0.01/0.1 mol/L)-Al3+(0.02 mol/L)-OH- system. Although the species and aluminum masking mechanism are different in these two systems, aluminum can be masked efficiently at pH 11~12. The larger discrepancy between the simulated titration curve and the experimental curve in the latter system is due to the slower reaction rate of the latter system. Furthermore, the permissible aluminum concentration at pH 11~12 was obtained by simulation. Considering the interference of OH- to fluoride ion selective electrode, pH is limited to 11.5±0.2 for the determination of fluoride at 0.01~0.1 mol/L, and the maximum aluminum concentration masked at pH 11.5 is 0.02 mol/L. This method suits for the determination of high F concentration in the F-Al system. The error analysis indicates that the standard calibration curve method is more accurate than standard addition method if the potential error is larger than the error of electrode slope constant.
由于氟易和伴生金属元素铝、钍、锆、铁等生成稳定性高的配合物[1],与钙、镁等元素生成固体氟化物,所以氟矿石如氟化铝、冰晶石、萤石中氟含量测定前需要将氟和这些干扰元素分离。 通常采用蒸馏法分离、容量法测定,如YS/T 273.3-2012冰晶石、YS/T 581.3-2012氟化铝中氟的测定和GB/T 5195.1萤石氟化钙含量的测定。 蒸馏-容量法费时费力,越来越多的研究者[1,2]倾向于使用氟离子电极测定高浓度氟。 氟离子电极测定低含量氟的研究很多,如饮用水、海水、卤水、茶叶、牛奶中氟的测定等[3],用于高含量氟体系的测定研究不多。 文献[4]报道,冰晶石和氟化铝碱解浸提后先用酸调节到体系无固体生成,再用碱调节pH值到酚酞变红,然后加入pH=10.4的乙酸胺和氯化钠总离子强度调节剂(TISAB),可以测定0.01 mol/L的氟。 Borjigin等[5,6]以酒石酸盐和三羟甲基甲胺为基础的TISAB成功掩蔽0.05 mol/L氟中0.025 mol/L的铝,并用于含硼体系中氟的测定。 以上测定氟的pH值均比较高,前者10.4,后者加入TISAB前pH值调节到11,本文作者推测以上研究实际起掩蔽作用的是OH-。 Oliver和Clayton[7]声称,只要F-活度比OH-离子活度大,采用氢氧化物掩蔽铝将更有优势。 Bebeshko[1]对F--M n+(Al3+、Be2+、Fe3+、Zr4+和U4+)-H2O体系在全pH值范围进行热力学分析,以F--Al3+体系为例,当F-水溶液活度5×10-6~5×10-2 mol/kg时,pH值8.5~9.4,Al(OH)3沉淀和F-共存。 当F与Al摩尔比小于0.1时,在此pH值区间固液不分离,75 ℃测定,2 mmol/L以上的氟回收率良好。
Bebeshko[1]分析F--Al3+体系热力学时未考虑羟基氟铝配合物。 羟基氟铝配合物是F--Al3+体系近中性时的主要物质[8],Lisbona和Steel[9]也认为它存在于F--Al3+-OH-体系。 本文在Bebeshko[1]的研究基础上,增加羟基氟铝配合物,采用Visual MINTEQ软件[10]进行F--Al3+-OH-体系的热力学平衡研究,考察氢氧化物对铝的掩蔽效果及原理,以确定高氟高铝体系中氟的测定条件。 这里高氟高铝指的是氟浓度在0.01~0.1之间,铝浓度10-2 mol/L数量级。 氟离子电极除了对F-有响应外,对OH-也有响应,所以采用氢氧化物作掩蔽剂时,需要控制电极使用的pH值范围,以减少OH-的干扰。 OH-/F-小于0.1时OH-的影响可以忽略,即测定0.01和0.1 mol/L F-浓度时,OH-干扰可以忽略的最大pH值分别是11和12,所以本文pH值考察范围不超过12。
1.1.1 铝的掩蔽 氟和羟基都与铝生成配合物,如式(1)和(2)所示,羟基和铝还能生成氢氧化铝沉淀,如式(3)。 从热力学看,生成羟基铝配合物的平衡常数要大于氟铝配合物平衡常数,如表1所示。 平衡常数决定于反应物和生成物的自由能之差,反应速率决定于活化自由能,所以平衡常数和反应速率一般无对应关系[11],但是羟基和铝的配位反应速率比氟和铝配位反应速率快。 即羟基和铝的反应在热力学和动力学上均是有利的,采用氢氧化物掩蔽铝释放F-在理论上是可行的。
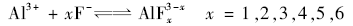
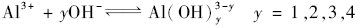
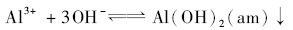
| 表1 氟化铝和羟基铝配合物25 ℃的平衡常数 a Table 1 Equilibrium constants of aluminum fluoride complex and hydroxyl aluminum complex at 25 ℃ |
1.1.2 氟的测定 氟离子选择电极是基于能斯特方程(4)测定F-浓度。
式中, E0为标准电极电势, cF为F-浓度, γF为F-活度系数,当离子强度固定时, γF为常数,从而得到式(5)。 其中 B是电极斜率常数,和温度有关,理论上25 ℃时 B为59.1 mV。
本底离子强度0.1~0.8 mol/L,加入被测离子后的离子强度变化不超过30%时,电势变化不超过1 mV[12]。 因此,本底离子强度1 mol/L时,加入0.01~0.1 mol/L的氟盐和一定量铝盐后,离子强度波动较小,假定 γF是常数合理,式(5)有效。 以下采用NaCl调节体系本底强度1 mol/L。
试剂不做说明均为分析纯试剂,购自天津光复化学品公司。
标准氟化钠储备液0.5 mol/L,标准氢氧化钠溶液0.9988 mol/L,氯化铝溶液0.1 mol/L,TISAB氯化钠溶液5 mol/L。雷磁PHS-25型数字pH计(海仪电科学仪器股份有限公司),读数准确到0.01;HANNA pH计(罗马尼亚制造),电势准确读到0.1 mV;罗素702型复合氟离子选择电极(上海罗素科技有限公司),线性范围10-6~0.1 mol/L。
准确移取一定体积标准氟化钠储备液、10 mL氯化铝溶液、10 mL氯化钠溶液配制成50 mL一定F-浓度的NaF-AlCl3(0.02 mol/L)-NaCl(1 mol/L)被滴定液,转移到250 mL烧杯中,放入氟离子电极和pH电极。 在电磁搅拌下,采用标准氢氧化钠溶液逐次滴定,当pH和电势读数基本稳定时,记录滴定体积、相应pH和电势。滴定到pH=12停止,耗时约40 min。
如引言所述,F--Al3+-OH-体系可能生成氟铝配合物、氟铝羟基配合物、羟基铝配合物和氢氧化铝沉淀,如式(6)所示。
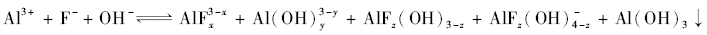
式中, x, y同式(1)和(2), z = 1,2,3。
Visual MINTEQ是一款简单易用的溶液平衡模拟软件,内含溶液中可能出现的离子、离子对、分子、固体沉淀相应的平衡常数和生成焓。 根据F--Al3+体系特点,对软件进行如下设定和改变:添加软件缺少的高配位氟铝配合物和羟基氟铝配合物及相应的平衡常数[9];离子对结合力弱,且存在更易和氟结合的离子,所以排除软件内含的氟化钠离子对;铝水解后最初以无定型氢氧化铝析出,老化后逐渐转化为其他形式的沉淀如三水铝石等[13],软件提供了氢氧化铝的多种沉淀形式,由于实际沉淀生成后不老化,所以设定体系析出的固体为无定型氢氧化铝。
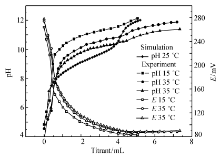
软件模拟F--Al3+体系的滴定曲线,并和实验滴定曲线比较,如图1所示。
由图1可知,电势随着滴定体积增加逐渐降低,最后稳定。 A、B体系pH值为11.5左右的电势分别为139.3 mV和83.1,由此计算得到电极斜率为56.2 mV,结果合理。
实验滴定曲线和模拟滴定曲线变化趋势一致;滴定曲线的两端差异小,中间差异大;0.01 mol/L的氟铝体系,模拟滴定曲线和实验滴定曲线一致性较好,0.1 mol/L的氟铝体系,相差较远,特别是pH值7~11之间。 分析认为,由于软件模拟的是25 ℃平衡状态下的滴定曲线,而实验测定的是有限时间内的滴定曲线,每滴加一定碱液后,记录的是未达平衡的数据,所以模拟滴定曲线和实验曲线存在差距,反应速率越慢,差距越大。 两端是主要发生的是较快的铝和氟的配位反应、铝和氢氧根的配位反应,差异小。 中间pH值发生羟基和氟竞争和铝的慢反应,差异大。 F-浓度越高,OH-和F-竞争和铝的反应速率越慢、越难达到平衡,所以F/Al摩尔比高的体系中间差异较大。 设想升高温度后,反应速率加快,在相同滴定时间内,反应将更接近平衡,模拟和实验值差距减小。 为了证实以上设想,测定了高F/Al比体系不同温度下的滴定曲线,模拟发现实验温度下和25 ℃的滴定曲线几乎重合,说明虽然温度影响平衡常数,但是对滴定曲线影响不大,所以以下将不同温度下的实验滴定曲线和25 ℃模拟滴定曲线比较,如图2所示。
图2表明,不同温度下电势值有差别,温度越高,电势值越高。 温度越高,实验滴定曲线和模拟滴定曲线差距越小,证实了以上分析和设想。 换句话说,实验数据由于动力学因素未达平衡,导致和模拟数据存在差异。 可以预想,如果实验测定的是达到平衡的数据,一致性会增加。 以上说明,F--Al3+体系软件设定合理、平衡模拟有效。
以NaF(0.01 mol/L,0.1 mol/L)-AlCl3(0.02 mol/L)-NaCl(1 mol/L)体系为例,模拟F--Al3+-OH-体系的平衡组分分布,如图3所示,考察OH-对铝的掩蔽效果。 其中忽略浓度低于总氟浓度1%的组分,Al(OH)3(am,amorphous solid)沉淀的浓度是沉淀的摩尔量和溶液体积之比。 由图3可知,一定浓度铝下,总氟浓度和pH值对体系平衡组分分布影响很大。 根据图3 A和图3 B,将体系组分随pH值变化(氢氧化钠的滴加)的过程以式(7)和式(8)表示,分析不同总氟浓度下OH-掩蔽铝的机理。
图3 A:
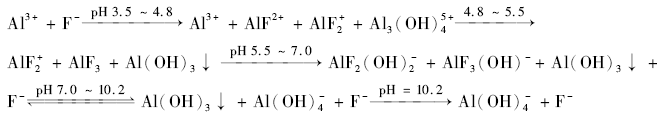
图3 B:
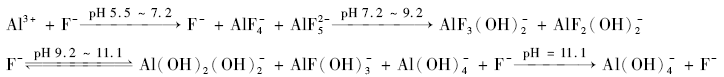
A体系的F/Al摩尔比低,低pH值时,存在Al3+、AlF x(x=1~3)和少量多聚铝酸盐;随着pH值增加,Al3+转换成Al(OH)3沉淀,AlF x加成OH逐渐生成AlF z(OH)-4- z、AlF z(OH)3- z(z=1-3),且随着pH值增加,F逐渐被OH取代,F配位数减小OH配位数增加;pH值继续增加,羟基氟铝配合物完全转变成Al(OH
可以看出,pH值为7以下,两个体系主要物质是AlF x,这和文献[14]报道的氟铝配合物是F--Al3+体系酸性条件下的主要组分是一致的。 当NaOH开始滴加后,A体系Al3+优先和OH反应生成Al(OH)3沉淀,随着pH值增加,OH主要加成到AlF x中,并逐步取代F释放F-;由于Al(OH)3沉淀和F-反应的平衡时间长达2 h[15],此反应可忽略,所以A体系Al(OH)3沉淀存在于很宽的pH值范围且沉淀量几乎不变。B体系由于总氟浓度高,一开始体系无自由Al3+,NaOH连续滴加时,OH逐渐取代AlF x中F,直至生成Al(OH
虽然不同F/Al比体系,添加NaOH逐步掩蔽铝的机理是不同的,但是在pH值11~12,铝以四羟基铝的形式被掩蔽,氟几乎完全游离出来,F-分布分数在pH=11.5达到99.5%。
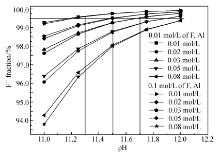
以上模拟说明0.01~0.1 mol/L的氟、0.02 mol/L的铝,氢氧化钠在pH值11~12掩蔽效果较好,有必要研究更高浓度的铝在pH值11~12能否被有效掩蔽。软件模拟了0.01~0.08 mol/L铝浓度,0.01和0.1 mol/L的总氟在pH值11~12的F-分布分数,如图4所示。
可以看出,pH值越高,掩蔽效果越好,F-分布分数越大;铝浓度越大,铝越难被掩蔽,相同pH值下的F-分布分数越低。 在所研究的范围,总氟浓度对F-分布分数几乎没有影响。 文献[17]认为F-分布分数99%以上铝被有效掩蔽,这里假设F-分布分数99.5%时,铝被有效掩蔽。
2.4.1 测定条件 氢氧化钠做掩蔽剂时,pH值除了满足掩蔽铝的条件外,应尽量减小OH-对氟离子电极的干扰。 测定0.01~0.1 mol/L的氟时,pH=11.5时,OH-引入0.3%~3%的误差。 由图4可得, pH=11.3时,最大掩蔽0.015 mol/L铝,pH=11.7时,最大掩蔽0.03 mol/L铝,控制pH值为11.5±0.2时,铝浓度0.02 mol/L合适。 在此条件下,成功测定了三氟化硼络合物的三氟化硼含量[18]。
2.4.2 测定方法 采用标准曲线法和标准加入法测定0.01~0.1 mol/L的氟,假设电势误差和电极斜率误差均为1 mV,根据文献[19]的误差计算公式,计算了标准曲线法和标准加入法测定结果的相对误差,如图5所示。
 | 图5 电势误差( A)和电极斜率误差( B)误差为1 mV时,标准曲线法和标准加入法测定结果的相对误差Fig.5 Relative error of calibration method and standard addition method at 1 mV of potential error( A) or slope error( B) |
由图5可知,电势误差对标准加入法测定结果误差影响较大,随着被测浓度增加而线性增加,对标准曲线法影响小,且不随被测浓度的变化而变化;电极斜率误差对标准曲线法影响较大,随着被测浓度增加而减小。 实验发现,电势误差较大,高达0.5 mV,而电极斜率比较稳定,误差不超过0.2 mV,所以选择标准曲线法测定结果更准确。
虽然F--Al3+体系的滴定曲线由于动力学原因未达平衡,但是实验和模拟曲线趋势的一致性以及软件模拟结果和实验现象的一致性,均证明了模拟的合理性。 当F/Al摩尔比低时,体系初始以Al3+和AlF x(x=1~3)为主,随着pH值增高,Al3+快速生成Al(OH)3沉淀,pH值继续增加,沉淀几乎不变,OH和AlF x的加成反应成为主要反应,由于沉淀和加成反应易达到平衡,所以实验和模拟滴定曲线一致性好。 当F/Al摩尔比高时,体系初始以F-和AlF x(x=3~5)为主,随着pH值增加,OH取代AlF x中F的反应是主导反应,过量F-抑制铝向Al(OH)3转化,所以此体系无沉淀生成。 由于取代反应难达到平衡,所以实验和模拟滴定曲线相差较大。 以上掩蔽机理虽然相差很大,但是在pH值11~12之间,0.01~0.1 mol/L氟、0.02 mol/L铝被有效掩蔽。 由于OH-对氟离子电极有干扰,所以测定0.01~0.1 mol/L氟时,控制pH值为11.5±0.2,铝浓度控制在pH=11.5的最大可掩蔽铝浓度0.02 mol/L之内。 误差分析表明,如果电势测定误差较电极斜率误差大时,标准曲线法更准确。 总之,采用氢氧化钠做掩蔽剂、氟离子电极法测定高氟高铝体系中氟,已成功用于三氟化硼络合物中氟的测定。 合理确定测定条件,有望用于冰晶石、氟化铝等矿石原料中氟的测定。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|