以SiO2为载体,铜氨溶液为前驱体,采用蒸氨法在不同蒸氨压力下制备了系列铜负载量质量分数为20.0%的Cu/SiO2催化剂。 采用X射线衍射(XRD)、H2-程序升温还(H2-TPR)、高分辨透射电子显微镜(HRTEM)、X射线诱导俄歇电子能谱(XAES)等技术手段对催化剂的物理化学性能进行了表征。 考察了蒸氨速率对催化剂物化结构及其草酸二甲酯催化加氢制乙二醇的催化性能影响。 在反应温度 200 ℃、压力3.0 MPa、液时空速LHSV=0.4 h-1、氢气草酸二甲酯摩尔比80:1的反应条件下测定了催化剂的活性。 结果表明,在蒸氨压力为31.3 kPa条件下制备的催化剂表现出了最佳活性和选择性,草酸二甲酯转化率达到了99.9%,乙二醇选择性达94.4%。 H2-TPR、XRD、TEM、FTIR及XAES表征结果表明,较低蒸氨压力有利于铜氨离子快速分解负载在载体上,避免铜粒子聚集长大,还原后形成Cu2O和Cu0物种颗粒尺寸较小,分散比较均匀,催化活性,尤其是乙二醇的选择性更佳。
A series of Cu/SiO2 catalysts with 20.0% mass fraction of Cu loading was prepared by the ammonia evaporation method using SiO2 as the support and Cu(NH3)42+ aqueous solutions as the precursor. The catalysts were characterized through X-ray diffraction(XRD), H2-temperaure programmed reduction(H2-TPR), transmission electronic microscopy(TEM) and X-ray Auger spectra(XAES) to investigate the influence of the ammonia evaporation rate on the catalyst physical and chemical structure and its catalytic performance for the hydrogenation of dimethyl oxalate(DMO) to ethylene glycol(EG). The catalytic activity measurement experiments were performed under working conditions of 200 ℃, p=3.0 MPa, LHSV=0.4 h-1 and the molar ratio of hydrogen to DMO( n(H2): n(DMO)=80:1). The results indicate that the catalyst prepared under high vacuum during ammonia evaporation has better catalytic performance. For the catalyst prepared under ammonia evaporation pressure of 31.3 kPa, 99.9% conversion of DMO and 94.4% selectivity to EG are obtained. Characterizations through XRD, H2-TPR, TEM and XAES suggest that the higher the ammonia evaporation rate, the faster and more uniform distribution of copper precursors upon the SiO2 support, and the coagulation and growth of the Cu particles during calcination and reduction can be reduced, which guarantees the high catalytic activity, particularly the selectivity to EG.
乙二醇(EG)具有重要工业用途,可作为生产聚酯纤维、润滑剂、炸药和表面活性剂等产品的添加剂[1]。 乙二醇可通过石化法和C1法合成,石化法合成乙二醇以环氧乙烷为原料,工艺流程长,能耗大,乙二醇选择性较低。 考虑到全球石油资源日益紧缺,我国资源多煤贫油的实际情况,由煤基合成气通过草酸二甲酯制取乙二醇的C1法更具战略意义[2]。 草酸二甲酯催化加氢包括以下反应:
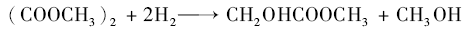

乙二醇过度加氢则生成乙醇:
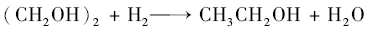
因此,催化剂需要较高加氢活性又不能太高,才能同时满足转化率和乙二醇选择性要求。 Cu/SiO2催化剂用于草酸二甲酯催化加氢制乙二醇最近研究广泛,其制备方法包括浸渍法,沉淀法,溶胶凝胶法以及蒸氨法[3,4,5,6]。 浸渍法不能很好地分散Cu物种,催化活性差;蒸氨法制备的催化剂Cu分散度好,活性高,通过掺杂可以实现良好稳定性[7],而且蒸氨法还可适合其它中孔载体[8],或制备成整体催化剂[9]。 对蒸氨法制备Cu/SiO2催化剂过程研究发现,蒸氨温度为90 ℃时催化剂活性最好[10]。 由于蒸氨是Cu(NH3)42+向Cu2+转变并与催化剂载体相互作用,并最终沉积在催化剂内孔表面的过程。 除了前驱体溶液浓度,蒸氨温度外,蒸氨压力也会影响催化剂形态和活性。 本文采用蒸氨法,控制蒸氨过程的压力制备了Cu/SiO2系列催化剂,考察了催化草酸二甲酯加氢制乙二醇反应性能,探讨蒸氨压力对活性铜物种粒径大小、分散状态等对催化性能的影响。
氢气程序升温还原于自制TPR装置进行测试;D/Max2500V型X射线衍射仪(日本理学公司),扫描范围2 θ=10°~90°;JEM-2100型高分辨透射电子显微镜(HRTEM,日本电子公司),观察催化剂的形貌、活性物种分布,工作电压为200 kV;Quantum 2000 Scanning ESCA Microprob型俄歇电子能谱仪(XAES,美国Physical Electronics公司),以Al- Kα为辐射源,扫描数次。
Cu(NO3)2·3H2O(分析纯,上海国药公司);NH3·H2O(浓度28.0%,上海国药公司);硅胶(Degussa A300,平均粒径9.0 nm,上海迪科实业有限公司)。
3.8 g Cu(NO3)2·3H2O溶于80.0 mL去离子水中,室温下滴加NH3·H2O至溶液pH值为9.0,搅拌30 min。 加入4.0 g硅胶,继续搅拌4.0 h,升温至90 ℃,通过真空表连接的三通阀控制蒸氨的压力分别为101.3、91.3、71.3和51.3 kPa以及31.3 kPa,直至溶液pH值降为7.0左右。 抽滤、分离,去离子水洗涤2~3次,100 ℃下干燥12.0 h,空气中以1 ℃/min升温速率升温至450 ℃焙烧4.0 h,选取0.25~0.38 mm颗粒催化剂备用。
H2-TPR:称取50.0 mg 0.25~0.38 mm催化剂,在300 ℃时用50 mL/min Ar气吹扫2.0 h,脱除表面物理吸附物种,冷却至室温。 Ar气切换为5%H2-95%Ar气混合气,以10 ℃/min的升温速率线性升温至750 ℃进行还原,过程经TCD检测氢气浓度变化。
XRD:将系列催化剂研磨至0.075~0.15 mm,用氢气于300 ℃下还原催化剂4.0 h,N2气气氛中降温至150 ℃左右,再用2%O2-98%N2气混合气钝化处理1.0 h作为试样。
HRTEM:催化剂研磨粉末后取颗粒尺寸小于0.075 nm的粉末,和XRD相同方法制样。 采用图像分析方法求解平均粒径大小。
XAES:以表面污染碳的C1 s结合能( Eb=284.6 eV)为内标校正其它元素的结合能。
催化剂活性测试在连续流动固定床反应器中进行。 将1.5 g颗粒大小0.25~0.38 mm催化剂装入反应管中。 反应前,在温度300 ℃、压力1.0 MPa条件下通入50.0 mL/min 高纯H2还原4.0 h。 将温度降为200 ℃、压力升至3.0 MPa、H2流量调至80.0 mL/min,将反应原料质量分数为15.0%草酸二甲酯甲醇溶液通入汽化室于220 ℃汽化后与氢气混合,进入反应器。 产物经冷却收集,由日本岛津GC-2014C型气相色谱FID检测器分析,色谱柱为HP-INNOWAX型的毛细管柱,填充物为聚乙二醇。 选择正丁醇为内标。
为更准确地表示蒸氨速率,每隔一定时间测定铜氨溶液pH值,结果见图1。
 | 图1 不同蒸氨压力下溶液pH值随时间变化Fig.1 Influence of ammonia evaporation pressure upon the pH value change of the aqueous solution |
随着蒸氨过程进行,Cu(NH3)42+迅速分解,游离氨被蒸出,溶液pH值减小至中性。 当蒸氨压力较低时,Cu(NH3)42+分解速度加快,除游离氨速率加快,溶液pH值减小趋势加快,溶液达中性所需时间减少。 Cu(NO3)2溶液中滴加过量氨水发生以下反应:
升温时,[Cu(NH3)4]2+受热分解:
根据电荷守恒原则,2 c(Cu2+)+ c (H+)+ c(N
 | 图2 不同蒸氨速率下溶液中N |
| 表1 不同蒸氨压力下溶液中N |
从中可以看出,当蒸氨压力较低时,[Cu(NH3)4]2+分解速度大大加快,氨脱除速率加快,溶液pH值迅速接近7.0。
2.2.1 H2-TPR CuO还原温度的不同归因于Cu物种尺寸、载体与Cu物种相互作用强度以及Cu物种分散度的差异[3]。 从H2-TPR谱图(图3)中看出,在31.3 kPa条件下蒸氨时,CuO还原峰为269 ℃,随着蒸氨压力增加,催化剂中的CuO还原温度升高,在101.3 kPa条件下蒸氨时CuO还原温度升至298 ℃。还原温度高于260 ℃,表明催化剂中主要存在晶相CuO[10]。 蒸氨压力较低时,CuO还原温度较低,表明晶相CuO粒径较小。 在较低压力下蒸氨时,Cu(NH3
 | 图3 不同蒸氨速率下制备的Cu/SiO2催化剂H2-TPR谱图Fig.3 H2-TPR profile of Cu/SiO2 catalysts prepared under different ammonia evaporation pressure p/kPa: a.31.3; b.51.3; c.71.3; d.91.3; e.101.3 |
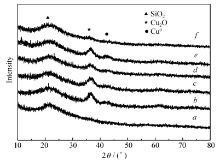
2.2.2 XRD表征结果 还原前和还原后的催化剂XRD表征结果见图4。 从图4可以看出,还原前催化剂的XRD谱呈弥散状态,只呈现出载体SiO2衍射峰。 在经过H2还原活化之后,在2 θ=36.5°左右出现Cu2O的衍射峰,2 θ=43.3°左右出现非常微弱的Cu0衍射峰。 Cu2O衍射峰较为明显,说明催化剂经还原后含Cu+较多。 Cu0衍射峰较弱,表明蒸氨法制备的Cu/SiO2催化剂中还原后Cu0晶粒很小。 还原前的催化剂中并没有CuO晶相衍射峰,表明Cu物种是高度分散在SiO2表面,或者CuO的晶粒尺寸小于3.0 nm。 随着蒸氨压力增加,Cu2O和Cu0晶相衍射峰强度变大,表明催化剂还原后,其中的Cu2O和Cu0晶粒尺寸较大。 在31.3 kPa蒸氨压力下制备的催化剂,其还原Cu+和Cu0的衍射峰均不明显,说明活性Cu物种颗粒小,分散均匀[13]。
2.2.3 HR-TEM图5为不同蒸氨压力下制备的催化剂还原后的HR-TEM表征结果。 图中黑色颗粒归属于铜物种[14],从图5可以明显看出,蒸氨压力对活性还原后Cu物种尺寸和分散度具有明显的影响。 较低蒸氨压力有利于形成超细Cu物种。 通过图像分析后得到的平均Cu晶粒的大小与蒸氨压力之间存在正相关,即蒸氨压力愈小,平均Cu晶粒也越小。 蒸氨压力为101.3 kPa时,Cu物种平均粒径大小为7.0 nm,降低蒸氨压力至91.3 kPa时,Cu物种平均粒径大小为5.9 nm,降低蒸氨压力为71.3 kPa时,Cu物种的平均粒径为5.1 nm,而蒸氨压力为51.3和31.3 kPa时,Cu物种的平均粒径大小分别为4.4和3.2 nm。 快速蒸氨有利于Cu物种在载体表面的分散,这与XRD、H2-TPR的表征结果也是一致的。
2.2.4 XAES 由于Cu2 p3/2 XPS谱图中Cu+和Cu0的结合能差别微小,因此还原后的催化剂表面Cu+和Cu0的化学环境由Cu LMM俄歇跃迁的区分。图6为不同蒸氨压力下制备的催化剂还原后的Cu LMM XAES,分峰得到的结果如表2所示。 从中可以看出,还原后的Cu/SiO2催化剂表面存在Cu+和Cu0,且Cu+/(Cu++Cu0)随蒸氨压力减小而变大,由29.53%增至58.51%,即最大比出现在蒸氨压力为31.3 kPa时。 这与文献报道结果吻合[15,16],在较低蒸氨压力下铜物种迅速分散地负载到SiO2载体孔道内表面,被还原为Cu0后易被钝化为Cu+,而常压下催化剂铜物种与硅胶结合较弱易被还原至Cu0,且铜物种间有团聚被钝化量少,所以Cu+含量低。也证明了蒸氨压力越低催化剂越分散与XRD、H2-TPR以及HR-TEM的表征结果也是一致的。
| 表2 由Cu LMM得到的还原后催化剂表面同物种的结合能及含量 Table 2 Cu species and binding energy on the Cu/SiO2 catalyst derived from Cu LMM spectra |
以不同蒸氨速率制备的Cu/SiO2催化剂上DMO的转化率和EG的选择性见图7。 在反应温度200 ℃、压力3.0 MPa、液时空速LHSV=0.4 h-1、氢气草酸二甲酯摩尔比=80:1的反应条件下,不同蒸氨压力下制备的催化剂上DMO的转化率无显著差别,但是EG的选择性差距很大。 蒸氨压力为101.3 kPa时,EG选择性仅为43.6%,但蒸氨压力降为91.3和71.3 kPa时,乙二醇的选择性分别增加到57.4%和61.3%,当蒸氨压力为31.3 kPa时,DMO的转化率接近100%,EG的选择性也达到了94.4%。 有关Cu0、Cu+及Cu2+在DMO加氢转化制乙二醇反应中的作用并未形成定论,但相关文献进行了一定程度探讨[6,15,16]。 李振花等[6]认为,在Cu/SiO2催化剂中还原后同时存在Cu+和Cu0,Cu+决定DMO的转化率,而Cu0决定EG的选择性。 Chen等[5]发现,Cu+与Cu0之间的协同作用决定了催化剂DMO加氢活性。 Yin等[18]认为高的金属分散度和合适的 Cu0/Cu+比例均有助于提高催化剂活性。 在本工作中采用蒸氨法制备含Cu质量分数为20.0%Cu/SiO2催化剂中,蒸氨压力对还原后催化剂中的Cu2O及Cu0的存在形态产生了重要影响,XRD表征结果表明,在31.3 kPa条件下蒸氨制备的催化剂还原后Cu2O和Cu0晶粒均非常小,TEM表征也证明了Cu物种在31.3 kPa条件下蒸氨时其在催化剂表面的分散度更好,而H2-TPR结果表明在31.3 kPa下蒸氨时催化剂中Cu物种的可还原性能最好,因此在DMO加氢制取EG的反应中,31.3 kPa蒸氨条件下制备的催化剂表现出了几乎完全转化,同时EG选择性达94.4%的优异催化性能。 结果还表明,小尺寸的Cu2O物种更有利于DMO的转化,因此,对DMO加氢制取EG的Cu/SiO2催化剂而言,同时获得小尺寸的Cu2O和Cu0,通过控制还原条件其反应条件下的还原气氛,可以维持优化的Cu+/Cu0比例,可以同时获得高的DMO转化率和EG选择性。
采用蒸氨法制备Cu/SiO2催化剂过程中,蒸氨压力对Cu物种颗粒尺寸大小及其在载体上的分散度有很大影响。 蒸氨压力小时,即真空度较大时,Cu(NH3)42+分解后快速负载到SiO2载体孔道内表面,而蒸氨压力接近常压时,易造成Cu物种在载体表面分散不均匀。 在较低蒸氨压力下制备的催化剂经还原后得到的Cu2O及Cu0物种晶粒尺寸更小,在DMO加氢制取EG的反应中表现出了优异的催化性能,DMO转化率接近100%,而EG的选择性达到了94.4%。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|