采用绿色水介质体系一步合成了3种不同尺寸的ZnO纳米片层结构。 通过微热量技术获取其原位生长过程的热谱曲线,从动力学和热力学角度分析其生长机理;利用电化学方法测定了不同温度下纳米ZnO与块体ZnO原电池的电势差,结合热力学基本公式求算出ZnO纳米片层结构的热力学函数值,并与生长机理关联讨论。 结果表明,ZnO纳米片层结构的生长经历了先表观吸热后表观放热,放热减慢,最后到达放热平台的热量变化阶段。 标准摩尔熵、标准摩尔生成Gibbs自由能及标准摩尔生成焓均随着尺寸减小而逐渐增大。 本文为纳米材料的原位生长机理与热力学函数的关联研究提供了新的思路和方法。
Three different sizes of ZnO nanosheet structures were prepared in one step by using the green water reaction system at room temperature. Microcalorimetry was used to obtain the in-situ growth heat curves, whose thermodynamic information of growth can be recorded in-situ and the corresponding growth mechanism was discussed from the point of thermodynamics. In addition, the electromotive forces were performed by a primary battery assembled by applying the prepared nano-ZnO and purchased bulk ZnO onto the surface of two zinc electrodes under different temperatures. The thermodynamic functions of nano-ZnO were gained by combining with basic formula of thermodynamic and associated with the growth mechanism. The results reveal that the growth of the ZnO nanosheet structures undergoes three stages for heat change. The standard molar entropy, standard molar Gibbs free energy, and standard molar enthalpy are increased along with the decreasing particle size. This paper provides a new method for investigating the in-situ growth mechanism and the thermodynamic functions of nanomaterials.
纳米材料独特的尺寸和形貌结构决定了其极高的表面能与反应活性[1,2,3],不同的生长热动力学行为是导致尺寸和形貌产生多样性的主要原因[4,5,6]。 为了理解纳米反应的本质及其潜在的应用,研究纳米材料的生长机理非常必要[7,8,9]。 然而目前关于纳米材料生长热动力学机理并关联热力学函数的探究却少有报道。 因此,采用何种科学方法获取纳米材料的热力学函数,如何关联热力学函数与原位生长热力学机理并就其演变规律给予合理诠释,已经成为纳米材料化学及热力学亟待解决的基本问题。
具有高精度、高灵敏度的原位微热量技术能实时在线监测体系的生长变化过程热力学及动力学信息,结合化学热动力学基本理论获得纳米材料的热力学函数及变化规律,应用于研究纳米材料生长机理具有普适性和科学性[10,11]。 我们课题组[12,13,14,15]已采用该技术并结合热动力学原理及动力学过渡状态理论成功获取纳米材料热力学函数,而本文则在此基础上,采用电化学方法测定纳米材料热力学函数并关联其生长机理。
本文采用微热量技术原位合成ZnO纳米片层结构并探讨其生长过程热动力学机理,基于纳米ZnO电极和块体ZnO电极的电势差,利用电化学方法测定了该原电池在不同温度下的电动势,依据热力学函数关系式求算出ZnO纳米片层结构的标准摩尔熵、标准摩尔生成Gibbs自由能、标准摩尔生成焓并讨论其演变规律。
盐酸和无水乙醇(分析纯,成都市科龙化工试剂厂),硝酸钾(分析纯,汕头西陇化工股份有限公司),锌片和氧化锌(分析纯,天津市科密欧化学试剂有限公司),二水合磷酸二氢钠、十二水合磷酸一氢钠(广东光华科技股份有限公司),块体ZnO(99.99%,阿拉丁试剂有限公司)。 RD496-CK2000型微热量仪(绵阳中物热分析仪器有限公司),Philips PW1710型X射线衍射仪(美国AMC公司),Cu Kα射线, λ=0.15406 nm,JEOL JSM-6700F型场发射扫描电子显微镜(日本JEOL公司),Gaoss Union EC550型电化学工作站(武汉高仕睿联科技有限公司),锌电极(武汉高仕睿联科技有限公司)。
稀盐酸除去锌片表面的氧化层,去离子水清洗并置于N2气中干燥;将相同大小的锌片置于微热量仪的大样品池,1 mL一定浓度的KNO3溶液(分别为0.1、0.3和0.5 mol/L)置于小样品池,封装后置入微热量仪主体,设置298.15 K恒温,待基线稳定时捅破小样品池,此时KNO3溶液与锌片接触并反应,微热量仪实时记录氧化锌纳米片层结构原位生长过程的热谱曲线。 上述3种浓度的KNO3与锌片反应的产物依次标记为Ⅰ、Ⅱ和Ⅲ,反应1 h后,分别用无水乙醇、去离子水洗涤3种产物,并于常温真空干燥。
将锌电极用0.05 μm的 α-Al2O3悬糊抛光至镜面后,依次用无水乙醇及蒸馏水超声清洗,并用N2干燥,取等体积的纳米和块体ZnO悬浮液分别滴涂于两个锌电极表面,干燥后备用。 配制0.2 mol/L,pH=7.0的磷酸盐缓冲溶液作为电解液,纳米氧化锌电极和块体氧化锌电极为工作电极和对电极,饱和甘汞电极为参比电极,连接电化学工作站,分别在293.15、297.15、299.15、303.15和305.15 K温度下测定原电池的电动势,通过电动势与反应热力学的关系式求取热力学函数。
图1为ZnO纳米片层结构的XRD图谱。 谱线 a、 b和 c分别对应产物Ⅰ、Ⅱ和Ⅲ。 图中所有衍射峰均与六方相结构ZnO(JCPDS card No.36-1451)相一致,且衍射峰的晶格参数为 a=0.3249 nm, c=0.5206 nm,未出现其它杂质峰,表明制得的纳米氧化锌较为纯净;尖锐的衍射峰和较高的衍射强度说明样品的晶型单一、结晶度良好。图2谱线 a、 b和 c分别对应产物Ⅰ、Ⅱ和Ⅲ的SEM照片。 由图2可知,产物均为二维纳米片层结构,形貌规则、表面光滑且分布均匀。 三者平均厚度约为4.6 nm,长度均在210~220 nm,平均宽度分别为30、53和67 nm。
 | 图1 产物Ⅰ( a)、Ⅱ( b)和Ⅲ( c) ZnO纳米片层结构的XRD图Fig.1 XRD patterns of the prepared ZnO nanosheet structures of productsⅠ( a), Ⅱ( b) and Ⅲ( c) |
采用3种不同浓度的KNO3溶液与锌片原位合成了3种不同尺寸的ZnO纳米结构片层,通过微热量仪获取其原位生长的热谱曲线。 当pH=7.0时,其反应式为Zn+KNO3 →ZnO+KNO3[16]。
由于该反应是在中性条件下进行,因此推测其反应机理如式(1),(2)所示:
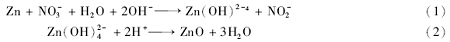
如生长机理图(图3)所示,单质Zn首先被氧化,与水中的OH-和N
图4 A为298.15 K下3种ZnO纳米片层结构的热电势随时间变化曲线,其生长机理可由热电势变化的3个阶段进行分析:
1)0~200 s。 由图4 A可知,三体系的热电势均呈现先下降后迅速上升,体系先是表观吸热后为表观放热。 这是因为Zn与OH-迅速反应结合成生长基元Zn(OH
2)200~500 s。 如图4 A所示,体系热电势上升至最高点后开始下降,体系仍为表观放热。 但从图4 B~4D中可以看出,与0~200 s内相比,其放热速率有所下降,这是因为晶粒初始生长的过程中会发生Ostwald熟化(即小粒子溶解,大粒子长大),溶解过程为吸热,但主要以晶体生长为主且此过程多数构晶离子已经形成晶体ZnO,所以体系仍然表现为表观放热。
3)500~3000 s。 体系热电势逐渐下降后进入平台期,放热速率继续降低最后趋于恒定。 这是由于大量的ZnO覆盖在Zn片表层,而少量剩余的构晶离子依然进行着结晶过程,所以体系仍是放热的。图4 B~4D显示1500 s以后,晶体以稳定、缓慢的生长速率进入了纳米ZnO片层形貌生长阶段。
由于纳米材料的非平衡态生长的细微差异可导致产物在尺寸、结构、形貌等方面的不同,于是3个体系中采用3种不同浓度的反应液而出现不同尺寸的纳米氧化锌。 一方面,增加硝酸钾的浓度,使反应物浓度大于某一临界值,加快了氧化锌的成核速率;另一方面,在高的过饱和比下,构晶分子绝大多数形成新核,导致构晶分子过度亏损,这就使浓度大的硝酸钾溶液中晶核的生长受到遏制,但浓度过大也导致了晶核的团聚,于是,样品Ⅰ、Ⅱ和Ⅲ的尺寸依次增大,生长过程放出的热量依次增加。
由电化学方法测定纳米ZnO与块体ZnO的电极电势差,根据二者的热力学关系式求算纳米ZnO片层结构的热力学函数值,该方法测定纳米材料的热力学函数,简单可行,实验结果更加准确,并且有效地避免纳米材料热力学性质的研究中面临的纳米材料吸附空气中水分子和纳米材料的结构遭到破坏等问题[17,18]。
电极反应方程式:
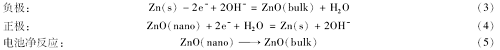
基于电池净反应,并结合电池电动势、温度系数与反应热力学函数的关系,可得关系式(6)、(7)和(8):
根据兰氏手册[19],块体ZnO的热力学函数依次为:
 | 图5 由产物Ⅰ( A)、Ⅱ( B)和Ⅲ( C)组装的原电池的 Eθ-T曲线Fig.5 Eθ-T curves of constructed primary batteries from products Ⅰ( A), Ⅱ( B) and Ⅲ( C) |
| 表1 所制备ZnO纳米片层结构的热力学函数 Table 1 Thermodynamic function values of prepared ZnO with nanosheet structures |
由表1可知,标准摩尔熵
纳米氧化锌标准摩尔生成Gibbs自由能随粒径减小而增大,且均大于块体。由于纳米材料在生长过程中不断地将本体原子迁移到表面,表面原子数量增加,这种高比表面使表面比内部占优势,所以纳米氧化锌 Δf
标准摩尔生成焓亦呈现同样的规律: 随着粒径减小,产物Ⅰ、Ⅱ和Ⅲ三体系焓变规律为: Δf
综上所述,本文利用高精度高灵敏度的微热量技术获得了3种不同尺寸的ZnO纳米片层结构原位生长的热谱曲线,并探讨了其生长机理;将纳米ZnO与块体ZnO分别滴涂于锌电极并组成原电池,运用电化学方法获得了所制备的不同尺寸ZnO纳米片层结构的标准摩尔熵、标准摩尔生成Gibbs自由能和标准摩尔生成焓。 结果表明,ZnO纳米片层结构的生长经历了先表观吸热后表观放热,放热减慢,最后到达放热平台的热量变化阶段;纳米氧化锌片层结构随着其尺寸增加,标准摩尔熵、标准摩尔生成Gibbs自由能及标准摩尔生成焓均减小。 与传统方法相比,将原位微热量技术与电化学方法联合,探讨纳米材料生长机理和热力学性质的方法简单可行且具有普适性,对纳米材料热力学方法论的发展具有重要意义。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|






