钯是一种重要的贵金属,在制药、燃料电池、电子电气和珠宝等行业得到广泛的应用。 然而,它的大量使用不可避免会造成其在环境中的残留,产生毒害,因此对钯的检测与识别具有重要的意义。 荧光探针具有较高的选择性、较高灵敏度、对设备依赖小、操作简单、检测限低等优点。 本文综述了近年应用于低浓度检测钯离子荧光分子探针的设计方法及作用机制。 按照荧光探针检测钯离子的响应模式,主要分为淬灭型、增强型、比率型3种方式进行评述。 尽管钯离子探针的研究在分子设计上取得了重要进展,但荧光染料与钯离子的响应时间尚且不能人为控制,尤其对于复杂体系中钯离子的检测效果尚待进一步改进。 因此,开发钯离子响应时间短、灵敏度高、专一识别性高并能应用于复杂体系的荧光探针,可能是今后主要发展方向。
A significant quantity of palladium is widely used in various materials, such as pharmacy, fuel cell, dental alloys and electronics, which inevitably cause its residues in the environment with pernicious effect on the body health. Therefore, it is of great significance to the detection and recognition of palladium. Owing to simple operation, high sensitivity, high sensitivity, low limit of detection, excellent high spatial and temporal resolution and especially nondestructive characteristics, fluorescent technique has been paid special attention. A variety of methods are discussed and introduced, which are applied in the design of fluorescent probes developed to detect the low concentration of palladium as well as mechanism of action in this review. Subsequently, the type of fluorescent probes mainly is classified into three kinds:quenching, turn-on and ratio based on response models. Although the molecular design of fluorescence probes of palladium has made an important progress, the response time of probes towards palladium is still uncontrollable. Additionally, it is not ideal for most fluorescent sensors to the detection of palladium in complex system. Developing rapid, high sensitive and selective fluorescent probes are suggested for future research to the detection of palladium ions in complex bio-system.
重金属在物理、化学和环境等科学中发挥着重要的作用,其中,钯金属由于其特殊的物理化学性质已被广泛应用在各个行业[1]。 然而,钯的大量使用不可避免会造成其在环境中的残留,引起环境重金属污染问题和人们的健康问题。 因此,钯离子的检测尤为重要。 研究人员发现健康人群每天机体的最大摄取量应该小于15 μg。 在制药行业中,药品中钯的残留量规定值为5~10 mg/kg。 大量负载钯及其化合物的排放会迅速提高土壤、植被、河流和海洋等不同环境中钯的含量[2],机体通过食物链富集效应对钯的过量摄入,吸收后的钯很快被运至肝脏、肾脏和脾等器官,会对身体造成非常严重的危害[3]。 经研究证实,在体内钯离子与氨基酸、蛋白质、DNA和维生素B6等生物大分子结合后发生作用,扰乱细胞正常的信号传导与生理活动等过程。 宏观症状表现患哮喘、脱发、流产、恶心和其它严重的身体疾病的机率随着增大[4,5]。 除此之外,对于易受感染的人群,即使在受到很低的钯离子入侵下也会引起严重的过敏反应。 因此构建高效、高选择性、高灵敏性和短时间响应定量检测钯的方法是人们目前亟待解决的问题[6,7,8,9,10,11,12,13]。
荧光探针是指其荧光性质(发射波长、强度和寿命等)可随着所处的环境(比如极性、粘度、温度和识别客体等)改变而灵敏地改变的一类荧光性分子[14]。 这里集中以近年来发展迅速的有机小分子钯离子的荧光探针作为评述对象。 有机小分子荧光染料在结构上一般由3部分构成:荧光信号基团(荧光团)、反应位点或者配体(识别位点)和连接臂[15,16]。 当探针分子与客体分子相互识别后,可能会通过光诱导电子转移(Photoinduced electron transfer,PET)、分子内电荷转移(Intermolecular charge transfer,ICT)、荧光共振能量传递(Fluorescence resonance energy transfer,FRET)和形成激基缔合物(Excimer)等机理而引发荧光光谱(包括荧光强度、荧光发射波长和荧光寿命等)的光物理性质的变化,从而提供可被检测的荧光信号[17]。 荧光探针具有选择性好、灵敏度高、对设备依赖小、操作简单和检测限低等优点[17,18,19,20],而且和激光扫描单/双光子荧光显微镜成像以及荧光寿命成像技术相结合,可以实现活体水平上在线无损原位的检测。 自从20世纪80年代初Tsien[21]报道了钙离子荧光探针的工作后,荧光探针得到快速的发展,日益成为现代生命科学、疾病早期诊断和临床治疗等领域不可缺少的研究工具[22]。
由于钯离子在水、土壤和沉积物等环境的样品中含量非常低,所以很难对它精确地检测。 尽管传统的检测方法(电感耦合等离子体 、原子吸收光谱、原子发射光谱和高效液相色谱法等)能得到较高的测量精度,但是需要昂贵的仪器与运行成本以及专业的操作技术人员[23,24,25]。 另外,在传统的检测方法中,为了避免污染或者损坏仪器,仍需要对样品进行繁杂的前处理。 综上所述,这些因素将大大限制传统仪器在日常检测中的广泛应用。 相比较而言,荧光探针法不仅能够克服传统方法的不足,而且还能快速、准确对客体响应。 因此,该检测方法近年来备受研究人员的关注。 随着荧光探针的改进以及光学仪器的发展,开发新型的钯离子荧光探针采取可视化研究其在生物体系中参与的生命历程与代谢活动,具有非常重要的生命意义[26]。 本综述主要涉及钯离子溶液中荧光探针的识别体系和识别机理,从淬灭型、增强型和比率型3种荧光探针与客体响应模式,简单概述了近年来相关的研究进展。
在荧光有机小分子识别客体体系中,荧光信号的淬灭(ON-OFF型)往往不利于其检测[26]。 但是作为荧光信号的响应模式之一,在这里我们只举两个案例来简单的表述。 Pd2+离子(4 d8构型)的 d轨道未充满,当其与荧光有机小分子结合后,构成荧光团-过渡金属配合物,可以通过光致电子转移等机理来淬灭荧光团的荧光。
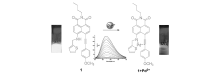
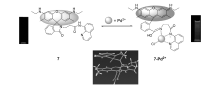
华东理工大学Qian课题组[27]2008年报道了一例高选择性的钯离子荧光探针1。 该荧光探针以经典的1,8-萘酰亚胺为母体,4位苯乙炔局部结构单元和5位噻吩甲基胺结构单元所形成的合适的配位空间作为识别位点(见图1)。 他们主要从以下两个方面考虑设计:Pd2+是一种“软”金属,与含硫的氨基酸、多肽和蛋白质容易形成稳定的复合物;Pd2+具有亲- π属性,很容易和炔烃配位( π-d贡献)。在乙醇/水(体积比60:40)测试体系中,随着钯离子加入量的增加,紫外光谱中除了340 nm吸收增强和458 nm吸收展宽之外,在270 nm位置出现一个新的吸收峰,预示着可能有一个稳定的配合物的形成。 在加入钯离子1 min后,溶液的颜色由淡黄色变成黑红色,可以通过比色方法,实现裸眼识别。 在相对应的荧光光谱中,在365 nm光源激发下,565 nm处荧光强度逐渐减弱,并且荧光量子产率由0.24减少到0.03(罗丹明B的甲醇溶液 ϕ=0.49为参比),可能是由于荧光团与过渡金属离子之间电子转移或者能量传递造成的。 通过Job's plot滴定实验与质谱分析结合,最终确定了探针1与钯离子配位比为1:1。 在选择性检测过程中,分别加入锌离子、汞离子、亚铜离子、铂离子、银离子、钴离子、铜离子、铅离子和钯离子到测试体系中,只有钯离子淬灭探针分子1的荧光,表明探针具有良好的选择性。 基于以上的实验结果,说明该染料对于检测水溶液中的钯离子具有很强的潜在应用价值。
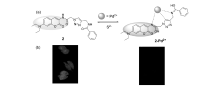
四川大学Yu课题组[28]在2013年设计了第一例含三唑结构的钯离子淬灭型探针分子2(见图2),该探针选用了香豆素为荧光团,经过“Click Reaction”反应连接适宜的配体,构成了酰胺-三唑-酰胺独特的序列配体结构。 配体中往往含有富电子的元素,比如N、S、烯/炔不饱和化学键等。 该探针2突出的优点是,在磷酸盐缓冲溶液(10 mmol/L,pH=7.2,PBS,0.5%DMF)体系中实现对Pd2+有专一识别性和高灵敏度响应。 探针识别Pd2+机理见图2,未识别Pd2+离子之前,激发波长选定在410 nm,荧光发射出491 nm波长香豆素的荧光。 加入Pd2+反应5 min后,由于其具有未充满 d轨道,可能会通过荧光团-过渡金属体系的PET/EET过程,造成探针分子荧光被淬灭。 探针与钯离子配位的结构经过核磁滴定进行了确定,其配位比为1:1。 另外,作者还通过理论计算模拟配位结构,从而进一步验证推理的正确性。 经过荧光滴定计算出该荧光探针2对钯离子的检测限为2.6×10-7 mol/L,能够满足实际样品检测的要求。 由于荧光分子具有较好的膜通透性和低的细胞毒性,最后,Yu课题组利用单光子共聚焦荧光显微镜对HeLa细胞中的Pd2+荧光成像(图2(b))。 该工作在分子设计上提供了一种通过改变构象结合识别位点的思想,可以为将来设计离子荧光探针提供一种策略,不足点在于激发与发射波长都比较短,尤其对生物样品光损伤较大,不利于用来研究其参与的生命历程和代谢活动可视化荧光成像。
根据仪器的敏感性能,对微小变化的荧光信号,荧光增强型信号比荧光淬灭型信号能更灵敏地被检测到,而且得到的数据更准确,因此,开发增强型荧光探针比淬灭型更具有实际的应用价值。 然而,在经典的荧光母体中,罗丹明开-闭环体系 是设计增强型荧光探针的经典平台,选择合适的配体或者反应位点修饰罗丹明的螺环部分,可以选择性与客体进行配位或者反应,促使螺环打开,最终导致荧光团母体的荧光得以恢复。 鉴于利用罗丹明开-闭环平台开发的钯离子的荧光探针较多,本节将重点介绍近年来该类型的增强型荧光探针。
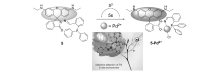
匹兹堡大学Koide课题组[29]在2007年设计合成一例增强型的Pd0荧光探针分子3。 该探针以荧光素为荧光母体,端位烯丙基醚作为反应位点(见图3)。 探针分子3是用丙烯酰氯与荧光素母体的羟基反应,合成过程较简单,收率较高。 该探针分子识别机理是基于Tsuji-Trost反应,具体过程表现为探针分子对零价钯发生氧化反应,生成活泼的中间体。 随后,烯丙基与钯配位的反面受到亲核试剂进攻,导致C—O化学键断裂,释放出荧光素强的荧光。 在硼酸盐缓冲体系(pH=10)中,加入Pd0或者高氧化态钯被还原成Pd(0),保护羟基的烃基脱除变为3-Pd2+,526 nm处荧光强度增加了442倍。 在Pd(0)的浓度0.03×10-7~3.0×10-7 mol/L范围内,探针对其的响应具有良好的线性关系( R2=0.99),可实现对样品中少量残留钯的痕量检测。 开发的钯荧光染料已被商业化,技术成功转化,进一步证实有机小分子染料在荧光检测中的实用价值。 该探针缺点在于其选择性会受到铂离子干扰,仍需要进一步优化探针分子的结构,提高其专一识别性。
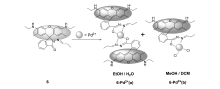
我们课题组[30]在2009年利用罗丹明为母体设计合成了一例对钯响应灵敏的探针分子4。 该探针分子对Pd2+和Pd0-复合物具有高选择性以及潜在的应用价值。 其识别机理是通过将Pd2+还原成Pd0,填满 d轨道,进而抑制Pd2+对母体荧光的淬灭效应。 Pd0与配体络合之后,诱导罗丹明分子内酰胺螺环打开,释放出荧光信号(见图4)。 在乙醇/水(体积比1:1)测试体系中,激发波长选在530 nm,随着Pd2+溶度的增加,在580 nm荧光强度逐渐增强,0~1.0×10-5 mol/L浓度范围内有呈现良好的线性关系,可以实现低溶度的定量检测。 通过计算得出,探针分子4在水体系的检测限为1.85×10-7 mol/L,实现了受钯污染水体中钯的检测。 为了进一步开发利用该探针分子,我们课题组还将其成功应用于试纸的开发。 试纸的便携、快速、定性识别将极大推进探针4产业化的可能性。 我们课题组[31]在原来设计荧光探针的基础上于2012年首次报道了将三齿PNO(磷、氮、氧)配体作为识别位点的探针分子5(见图5),效果有明显的改善。 在乙醇测试体系中,激发波长选在505 nm,加入Pd2+离子,钯离子与三齿PNO配体络合诱导螺环开环,释放出552 nm荧光信号。 该探针分子除了对Pd2+具有较高的灵敏度(检测限为5.0×10-9 mol/L)和良好的选择性,其测试体系溶液的颜色由无色变为粉红色,实现了对Pd2+的裸眼检测。 更重要的是,在室温下实现了对Pd2+快速(响应时间只有5 s)、可逆的荧光识别,使得对Pd2+离子在复杂体系的动态检测成为可能。 同时,该探针避免了铂和钌等同族元素的干扰,提高了可靠性和实用性。 探针5对药物分子、水、土壤和叶子等样品的模拟测试实验表明,该分子对这些样品中痕量钯也有较好的响应,具有高的实际应用价值。 随后2013年,我们课题组[32]在此基础上还通过改变不同配体进行调控,设计合成了增强型性能较好的Pd2+荧光探针6,发现探针分子在不同的测试体系与客体钯离子形成不同配比的配合物。 在乙醇/水(体积比1:1)体系,荧光分子6与钯离子配位的化学计量比为2:1(图6(a));在甲醇/二氯甲烷(体积比1:1)混合体系,探针分子6与钯离子化学计量比为1:1(图6(b))。 主客体识别环境的不同造成主客体配位化学计量比的不同,凸显了识别体系在配位过程中的重要性。
 | 图4 探针4分子识别Pd2+机理(a)以及选择性(b)[30]Fig.4 Mechanism(a) and selectivity(b) of the probe 4 recognition for Pd2+[30] |
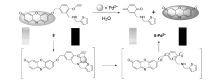
孟加拉国工程技术大学Goswami等[33]在2011年利用罗丹明为荧光团设计合成了一例探针分子7,该分子通过含有N、O富电子元素的柔性链桥连8-氨基喹啉。 探针分子7的优势是能够在乙醇和水(体积比1:1)的HEPES缓冲溶液(50 mmol/L,pH=7.2)中灵敏地识别溶液中Pd2+离子。 探针识别机理是Pd2+通过与有机小分子荧光探针中N元素有效的配位后,诱导螺环开环使罗丹明的荧光恢复(见图7)。 未识别Pd2+之前,溶液中的探针没有荧光信号;Pd2+识别之后,激发波长在505 nm,发射波长在562 nm附近有较强的荧光发射。 荧光量子产率由0.021增大到0.125(罗丹明B的甲醇溶液 ϕ=0.49为参比),提高了5.95倍,有利于荧光检测。 经过Job's plot滴定曲线与质谱鉴定相结合确认出荧光探针分子7与客体Pd2+配比为1:1。 除此之外,Goswami等还通过培养单晶实验,利用X射线衍射(XRD)技术对晶体结构解析(图7),进一步验证探针分子与Pd2+配比。 这为探究探针的主客体识别机制提供了强有力的研究工具。
韩国高丽大学Kim课题组[34]在2012年报道了一例在温和的条件下对钯快速响应的荧光探针分子8。 该探针以试卤灵为荧光母体,噻吩甲基胺结构单元和乙炔醚结构单元组合成的识别位点(见图8)。 钯离子与配体配位之后,催化裂解乙炔醚结构中的C—O化学键,最终使试卤灵荧光恢复。 在甲醇和磷酸盐缓冲溶液(10 mmol/L,pH=7.4)(体积比8:2)体系中,激发波长在550 nm,随着钯离子加入量的不断增加,响应时间30 min, 586 nm处的荧光强度逐渐增强。 在0~5×10-6 mol/L范围内,探针对其的响应具有良好的线性关系( R2=0.99),经计算得出检测限5.0×10-8 mol/L,具有实际应用的潜力。 为了探究其物理光谱学的行为,该课题组还采用DFT理论计算来优化主客体识别过程中结构,理论计算结果与实验测试基本吻合,这为今后分子设计提供一种行之有效的参照工具。 韩国檀国大学Kim课题组[35]在2014年利用荧光量子产率高、摩尔消光系数高、光稳定性好的氟硼二吡咯类(BODIPY类)为荧光母体设计合成一例增强型荧光探针9。 由于在荧光母体引入重原子碘,促使激发态电子由S-T态系间穿越,进而淬灭BODIPY母体荧光。 在乙醇/水(体积比1:4)测试体系中,Pd2+离子被还原成的Pd0聚集形成钯的纳米颗粒,在原位可以有效地催化碳-碘化学键断裂使碘离去(见图9),进而BODIPY的荧光得以恢复。 催化反应的响应时间30 min到达平衡,反应前后荧光量子产率从0.017(罗丹明6G的乙醇溶液 ϕ=0.98为参比)增大到0.55(荧光素的0.1 mol/L氢氧化钠溶液 ϕ=0.95为参比)。 通过选择性实验分析,该探针分子对Pd2+具有专一的选择性,对(激发波长选在465 nm)1.0×10-5 ~5.0×10-5 mol/L浓度范围内的钯离子具有良好的线性关系,相关系数 R2为0.98,计算得出最低检测限为1.0×10-8 mol/L。 表明该探针在化学样品和环境中钯的定性与定量分析中具有潜在的应用价值。
 | 图9 探针9分子识别Pd2+机理(a)以及滴定线性(b)[35]Fig.9 The mechanism of the probe 9 recognition for Pd2+(a) and fluorescence titration spectra of probe 9 in the presence of different concentrations of Pd2+(b)[35] |
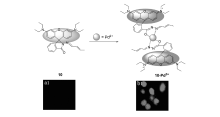
西北大学Yang等[36]在2014年利用罗丹明母体为荧光团开发出一例具有专一选择性的Pd2+探针分子10。 其设计思想是Pd2+诱导螺环开环,导致荧光增强,共存其它离子干扰可以忽略,可以实现复杂体系中钯离子的检测(见图10)。 在甲醇与PBS体积比1:1体系中,识别Pd2+后溶液由无色变为粉红色,实现了对钯离子的裸眼识别。 激发波长在535 nm,随着钯离子加入量增大,发射波长在578 nm处荧光强度随之增强。 在0~10×10-6 mol/L范围内,探针10对钯离子的响应具有良好的线性关系( R2=0.9939),经计算得出检测限为1.9×10-5 mol/L,使实际样品的痕量检测成为可能。 为了拓展该荧光探针的应用价值,作者还成功将其做成试纸,对钯离子检测更便捷、方便。 最后,Yang等还将探针应用于HepG2细胞荧光成像,表明探针10可以用来检测HepG2细胞中Pd2+离子,这为研究重金属钯离子在细胞中化学生物学的生命活动提供了便利。
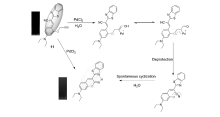
浙江理工大学Han课题组[37]在2016年报道了一例增强型的荧光探针11。 在PBS与乙醇体积比1:1测试体系中,加入钯离子,在水参与下经历诱导脱除炔丙基,氧负离子对氰基亲核成环,最终形成类似经典香豆素荧光团的衍生物。 分子内氢键的存在,促使分子趋于平面性(见图11)。 激发波长选在510 nm,随着钯离子加入量的不断增加,发射波长在542 nm,荧光强度逐渐增强。 在低溶度范围内,探针对其响应具有良好的线性关系( R2=0.9923),经计算得出检测限为9.3×10-8 mol/L,具有潜在的实际应用价值。 选择性与干扰性实验表明,该探针分子对钯离子具有专一性响应。 基于以上探针11优良的性能,Han课题组将该探针用于Hela活细胞激光共聚焦荧光成像。
现在文献报道的大部分荧光探针是以荧光强度的增加或者减小作为响应信号,但是这种信号很容易受外界条件(探针分布浓度、环境的pH值、极性、温度和粘度等)和仪器自身(激发光源和检测限灵敏度等)等不确定性因素的干扰[38,39]。 然而,比率型荧光探针通过两个峰的强度比值进行自校准,最大程度地减小其它因素的干扰,进而使检测结果更精确、可靠。
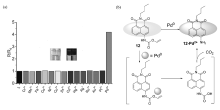 | 图12 探针12分子对不同离子的选择性(a);探针12分子识别Pd2+机理(b)[40]Fig.12 Fluorescence intensity R/R0( R=I524/ I498) of probe 11 in the presence of various metal species(a); the mechanism of the probe 12 recognition for Pd2+(b)[40] |
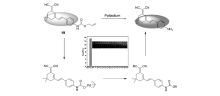
兰州大学Liu等[40]在2011年利用萘酰亚胺为母体开发了一例比率型荧光探针12。 该探针分子在钯的催化下,最终通过诱导酰胺键的断裂,释放母体的荧光信号。 在识别过程中,该探针表现出高的选择性,加入Pd2+后,反应在30 min之后达到平衡,溶液的颜色由无色变为黄色,荧光发射由蓝色变为绿色,可实现比色与比率双模式检测。 在测试体系乙腈/水(体积比为4:1)中,激发波长403 nm,随着Pd2+的量的增加,发射波长在524 nm荧光信号增强,498 nm荧光信号减弱,但是荧光强度比率值( I524/ I498)与Pd2+的滴定量呈线性关系,可以实现定量检测水体系中的Pd2+的含量。 所开发的荧光染料12对钯离子检测限6.1×10-9 mol/L,能够检测实际环境低浓度钯离子浓度。
湖南大学Lin课题组[41]在2013年合成了一例近红外比例型荧光探针13,该探针以花菁染料为分子骨架,端部炔丙基醚为识别位点。 探针分子突出的优点在于采用了组织穿透能力强和能够避免机体自发背景荧光干扰的近红外荧光染料。 响应机理为该探针分子上的三键与钯识别(见图13),使得炔丙基从荧光分子上脱去,荧光得以恢复。 激发波长在690 nm,发射波长714 nm,在偏碱性(pH值为7.35~7.45)的活体内反应后的酚羟基上的质子很容易离去。 离去后的氧负离子有很强的给电子能力,半花菁染料的氮正离子有很有强的拉电子能力,分子内形成一个推拉电子体系,促使分子发生分子内电荷转移(ICT)过程,在极性溶液中具有大的斯托克斯位移(Stokes)。随着钯不断被加入到水和二甲基亚砜体积比为3:7测试体系中,激发波长选在690 nm,发射波长714 nm处的荧光强度信号与钯离子浓度呈现良好的线性关系,经计算得出最低检测限为3.4×10-7 mol/L,表明探针分子对钯的检测具有高灵敏性。 由图13(b)可知,该探针不受其它金属离子干扰。最后该课题组还将探针13在HeLa细胞水平上进行了体内钯离子的近红外荧光共聚焦成像,这为研究钯在细胞中分布提供了可视化工具。
 | 图13 探针13分子识别Pd2+机理(a)以及其在水和二甲基亚砜体系中对不同金属离子的荧光强度(b)[41]Fig.13 Mechanism of the probe 13 recognition for Pd2+(a) and fluorescence intensity of probe 14 towards the presence of various metal species[41] |
华东理工大学Qian课题组[42]在2013年设计合成了一例比率型荧光探针14。 由于探针分子在水相中的溶解度差,在含有溴化十六烷基三甲铵(CTAB,表面活性剂)的PBS测试体系中加入2.0 mmol/L四氢呋喃后,强力搅拌60 s进行测试。 该探针识别钯经过5 min反应达到平衡,反应之前是415 nm蓝色荧光,高选择性识别之后是555 nm黄色荧光(见图14)。 在1×10-6~8×10-6 mol/L范围内,激发波长选在350 nm,探针14荧光强度 I550/ I418比率对钯离子的响应具有良好的线性关系( R2=0.99),经计算得出检测限为5.2×10-9 mol/L,适于痕量钯离子的检测。 设计思想是在钯催化下烯丙基醚C—O化学键断裂生成羟基,羟基靠近苯并噻唑的N,羟基的H与N在空间上满足形成氢键,基态的分子受到激发很容易发生质子转移过程(ESIPT),造成130 nm的Stokes位移。 为了拓展该荧光分子的应用范畴,Qian课题组还将其做成试纸,显示出较好的效果(图14(b))。
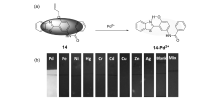 | 图14 探针14分子识别Pd2+机理(a)以及试纸对不同金属离子的检测效果(b)[42]Fig.14 Mechanism of the probe 14 recognition for Pd2+(a) and solid-state fluorescent response of probe 15 with different metal ions(b)[42] |
我们课题组[43]在2013年报道了一例基于Tsuji-Trost反应机理近红外荧光探针15。 采用花菁染料为荧光母体,利用其长波长激发得到近红外发射荧光(生物窗口650~900 nm)信号优势,有效避免了生物组织自发背景荧光干扰。 通过对花菁染料中位调控,用氮元素取代氯元素,在菁染料分子内发生电荷转移过程(ICT),实现了菁染料大的Stokes位移,降低了染料由自吸收而导致荧光淬灭的程度。 加入钯离子后,Pd2+被体系中NaBH4还原成Pd0,紧接着催化丙烯基醚C—O化学键,生成的中间体水解之后生成氨基产物,溶液颜色由绿色变为蓝色,可以到达裸眼识别效果(见图15(a))。 在比率型探针的基础上,还用PEG-400代替常用Tsuji-Trost反应钯配体的三苯基膦来提高其生物相容性。 激发波长选在640 nm处,随着钯离子加入量增多,荧光强度比率 I750/ I820在0~1.0×10-6 mol/L钯离子浓度范围内具有好的线性关系( R2=0.99),经计算检测限为3.76×10-6 mol/L,可以实现定量的检测。
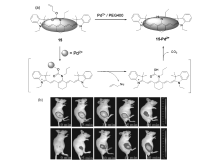 | 图15 探针15分子识别Pd2+机理(a)和活体成像(b)[43]Fig.15 Mechanism of the probe 15 recognition for Pd2+(a) and imaging in vivo(b)[43] |
不足点在于探针与钯离子孵育长达1 h才能达到平衡状态。 最后,为了探究探针分子15在活体组织中使用的可能性,我们还成功地在活鼠水平上对钯离子的分布进行了活体成像(见图15(b))。
华东理工大学Zhu课题组[44]在2014年设计合成了一例比率型荧光探针16。 通过对菁染料的 π共轭电子云密度的调控,在未识别钯离子之前,最大吸收在740 nm,荧光发射在825 nm。 在乙腈和PBS体积比1:3测试体系中加入钯离子,反应20 min后到达平衡状态,最大吸收在540 nm,荧光发射在660 nm,对钯离子响应前后Stokes位移多达270 nm(见图16),溶液的颜色由蓝绿色变为红色,可实现裸眼识别。 另外,经计算检测限为2.8×10-8 mol/L,可实现低浓度的定量检测。 为了探究该荧光分子实际应用,Zhu课题组还将其做成试纸,同样得到实用的效果。 最后,他们还用探针16在HeLa细胞水平上进行活细胞的比率型荧光成像,荧光比率值为研究活细胞内钯离子的定量测定提供了可信的数据。
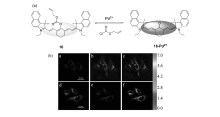 | 图16 探针16分子识别Pd2+机理和细胞成像[44]Fig.16 Mechanism of the probe 16 recognition for Pd2+ and cells imaging[44] |
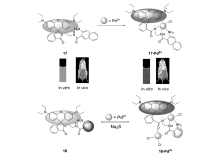
我们课题组[45]在2014年报道了一例比率型荧光分子17。 在探针分子结构设计上采用罗丹明为母体,乙二胺作为桥连的连接臂,将3-氨基-2-萘甲酸与罗丹明连接,构成合适的配位空腔。 在乙醇和水(体积比1:1)测试体系中,选420 nm的光作为激发光源,未识别钯离子之前,接收到490 nm荧光发射信号。 与Pd2+相互作用10 min之后,采用同样的光激发,收集到590 nm的荧光发射(见图17)。 荧光强度比率( I590/ I490)与钯离子在0~1.0×10-5 mol/L具有好的线性关系,检测限为4.59×10-8 mol/L,可以对环境中低浓度钯离子进行定量的检测。 另外,为了探究该探针活体水平上的应用前景,我们还利用小动物成像仪对小鼠体内的钯离子进行成像研究。 同年,我们课题组[46]将3-氨基-2-苯甲酸替代3-氨基-2-萘甲酸设计合成为一例比率型荧光探针分18。 该探针分子在未识别Pd2+之前,发射3-氨基-2-萘甲酸的408 nm蓝色荧光,加入Pd2+识别10 min之后反应达到平衡,螺环打开,发射罗丹明本身的588 nm红色荧光(见图17)。 激发波长360 nm,发射荧光强度比率 I588/ I408与钯离子浓度呈良好线性关系,经计算检测限为7.38×10-8 mol/L,这样可以定量测定溶液中低溶度Pd2+的含量。 由此可见,经过微小改变分子的局部结构,荧光探针对客体识别表现出不同的性能。 这也是荧光分子探针领域引起相关研究者关注原因之一,或许在原有结构基础上进行微小的改变,整个探针分子的性能会大幅度的提升,从而可能实现荧光探针在日常生活中应用。
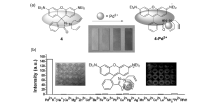
华东理工大学Zhang课题组[47]在2015年报道了一例长波长比率型荧光探针19。 当加入的钯触发反应之后(Tsuji-Trost Reaction),释放出给电子的氨基结构,另一端是两个氰基的强吸电子结构,造成分子内形成一个强的推拉电子(D-A)体系,使探针发生分子内电荷转移(ICT)过程,在极性溶剂中有大的斯托克斯位移(Stokes),避免由染料自吸收导致荧光淬灭。 待钯加入到DMSO/PBS(体积比1:1,pH=7.4)缓冲溶液中,反应大约30 min达到平衡,溶液的颜色由黄色变为粉红色,可以实现裸眼识别。 激发波长选在472 nm,在0~1×10-6 mol/L浓度范围内,探针19 I643/ I570荧光比率信号强度对钯的响应具有良好的线性关系( R2=0.97),经计算得出检测限2.42×10-8 mol/L,具有可以检测低浓度钯的潜力。 另外,该探针19表现出专一的选择性,不受环境的pH值影响、具有较快的响应速度,这些优点为该探针能够用于活体组织生物的检测提供了条件。
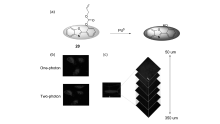
兰州大学Liu课题组[48]在2016年基于ESIPT机理设计了一例比率型双光子荧光探针分子20。 在含有10%(体积分数)乙腈的磷酸盐缓冲溶液测试体系中,钯诱导催化脱除末端的烯丙基甲酸酯识别位点,使得苯并噻唑中的N原子与邻近羟基中H在分子激发态的ESIPT(激发态分子内质子转移,excited-state intramolecular proton transfer,ESIPT)过程得以恢复,得到发射波长红移大斯托克斯位移(88 nm)的荧光发射峰。 随着钯加入量增加(0~5×10-6 mol/L),激发在325 nm,荧光强度比率 I476/ I420随之表现出良好的线性关系( R2=0.9935),表明该探针分子20可以在该体系下定量检测钯的含量。 经过计算该探针的最低检测限为1.56×10-8 mol/L,低于大多数有关钯的荧光探针,满足实际样品的检测。 作者还考察了该探针的双光子吸收方面的性质,分子20在760 nm处双光子吸收截面仅有4.13 GM,加入钯大约20 min后反应达到平衡,双光子吸收截面提高了44.1倍高达182 GM。 最后,将探针20应用到Hela活细胞激光共聚焦单光子与双光子荧光成像,还考察了用其对宫颈癌组织的深度成像,这为进一步研究钯离子在活体组织水平上参与的生理活动提供了强有力的可视化工具。
最近几年,基于有机小分子体系开发专一性识别钯离子荧光探针越来越多。 通过总结归纳已有文献报道,钯离子荧光探针的响应模式分为淬灭型、增强型和比率型。 其中,近红外发射比率型荧光探针的数量呈现逐渐增多趋势。 另外,随着双光子激光显微成像技术推广应用,今后开发双光子钯离子荧光探针的相关工作可能会逐渐出现。 为了满足初学者或者其他领域研究人员对钯离子荧光探针结构设计的需求,我们从作用机制角度总结了大多数钯离子荧光探针基本的设计原理,概述如下:
1)基于钯离子的配位能力,设计含有N、O、S和P等富电子元素相关的结构为基础,合适的配位空腔为条件,使其与钯离子配位之后溶液颜色与荧光信号有较大的变化;
2)基于Tsuji-Trost 反应机理,设计合成近红外比率型的荧光探针,钯催化端位的烯/炔丙基醚C—O化学键断裂,荧光信号随之变化并伴随着波长的改变,可以用来设计双通道检测的荧光探针;
3)基于对重元素(比如碘元素)的被催化裂解,荧光得到释放,从而可设计增强型的荧光探针。
但是,目前所开发钯离子的荧光探针也存在着较多的问题。有些激发波长和发射波长较短,不利于将其直接用于细胞活体成像,这一缺点也将限制探针在组织深度成像方面广泛而深入的应用。 双光子荧光探针逐渐被开发出来,利用其长波长(690~1000 nm)激发,不仅能够有效避免光毒性、稳定性以及组织自发荧光的干扰,而且可以得到较为理想的生物窗口的长波长发射。 我们相信,随着对钯离子荧光探针研究的不断深入,光学显微仪器的发展,开发出生物相容性好、响应速度快、灵敏度高并且能应用于检测食品、药品、环境及细胞内的钯离子含量的新型荧光探针将成为今后研究工作的热点。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|