采用计时电流法沉积纳米MnO2电极材料,利用Scharifker-Hills成核理论模型分析时间-电流( i-t)曲线判断了MnO2成核机理。 对3种不同的成核方式制得的MnO2材料进行电化学超级电容性能测试、用SEM观察了其微观形貌。 比较了不同沉积方法对沉积材料结构、电容性能的影响。 计时电流测试发现,在0.1 mol/L Mn2+溶液中,电势阶跃至0.365 V,初始成核符合瞬时成核机理,在0.01 mol/L Mn2+溶液中,电势阶跃至0.418 V,初始成核存在瞬时成核和连续成核两种不同机理,在0.5 mmol/L Mn2+溶液中,电势阶跃至0.515 V,初始成核则符合连续成核机理。 超级电容性能测试发现,瞬时成核下制得的MnO2电极材料相对于另外两种成核方式得到的电极材料具有更好的电容性能,这是因为瞬时成核更易于形成多孔、纳米片(棒)状等高比表面积的沉积物,表明制备方法影响MnO2电极材料电容性能。
An ITO supported nanostructure manganese dioxide thin film electrode, fabricated by chronoamperometry was evaluated as a potential electrode for electrochemical capacitors. The nucleation mechanism was examined by fitting the experimental data(chronoamperometry) into the Scharifker/Hills nucleation models. SEM images of the electrodeposits show that the microstructure of manganese dioxide is affected by the deposition period. The capacity of the three kinds of manganese dioxide electrode materials formed by different nucleation mechanisms was investigated by cycle voltammetry, constant current charge-discharge method and AC impedance. The results show that the nucleation follows an instantaneous nucleation mechanism in the solution of 0.1 mol/L Mn2+ under a 0.365 V step potential, and mixed instantaneous and progressive nucleation mechanism in the solution of 0.01 mol/L Mn2+ under a 0.418 V step potential. The nucleation follows a progressive nucleation mechanism in the solution of 0.5 mmol/L Mn2+ under a 0.515 V step potential. It is obvious that the instantaneous nucleation is beneficial to preparing deposit sediment which has high specific surface area. Compare with other electrolytic deposit materials, this kind of material displays a better capacitance performance, implying that the capacitance performance can be influenced via different deposit approaches.
由于传统能源的匮乏和环境污染的日益严重,人类在可用能源方面面临着两大难题:新型清洁能源的开发和应用及如何提高现有能源的使用效率。 随着新能源技术的发展,需要快速地发展关于新能源的转化、存储、使用等方面的新技术。 超级电容器作为一种新型的能源存储设备,能很好地弥补传统储能设备在能量密度以及功率密度上的不足,在许多特殊领域有不可替代的作用[1]。
常用超级电容器电极材料有碳材料、金属氧化物以及导电聚合物等[1]。 其中MnO2作为超级电容器的电极材料,已经得到了非常广泛地研究。 研究表明,MnO2的电化学性能与其合成方法、条件以及使用的环境有紧密的联系。 因此可以通过改变合成方法、控制合成条件等手段来提高MnO2电极材料的性能。 已报道的超级电容器电极材料MnO2的制备方法,包括溶胶凝胶法、水热合成法、电化学沉积法[2,3,4]。 其中,电化学沉积方法具有简单、可靠、准确、通用性强、成本低等优点,被证明在改变电极材料的结构和电化学性能方面有显著的效果[5]。 通过控制电化学沉积参数(如溶液浓度、温度、搅拌速度以及电流密度(过电势)大小等),来控制MnO2成核和生长方式(如连续成核、瞬时成核,二维生长、三维生长),最终控制MnO2的形貌及晶体结构,从而影响MnO2的超级电容性能[6]。
本实验采用计时电流法制备MnO2膜电极。 通过分析不同电势下MnO2沉积初始阶段的计时电流曲线,根据Scharifker-Hills(SH)的理论模型[7,8],归一化处理电流-时间曲线,与理论成核曲线对照,判断MnO2的成核机理。 采用循环伏安法(CV)、计时电势法(CP)以及交流阻抗法(EIS)等方法测试所制得的MnO2电极材料的电化学行为,根据公式及拟合结果计算不同电极材料的电容值,比较成核机制对制备电极材料电容性能的影响。
CHI660B型电化学工作站(上海辰华仪器有限公司),铂片辅助电极(天津艾达恒晟科技发展有限公司),ITO导电玻璃工作电极(珠海凯为光电科技有限公司),饱和KCl作盐桥的饱和甘汞电极(天津艾达恒晟科技发展有限公司),JSM-7800F型扫描电子显微镜(日本JEOL公司)。
Mn(CH3COO)2(川东化工试剂厂),Na2SO4(川东化工试剂厂),CH3COONH4(川东化工试剂厂),KCl(川东化工试剂厂),无水乙醇(川东化工试剂厂),以上试剂均为分析纯。
配制电解溶液,1号溶液:0.5 mmol/L Mn(CH3COO)2+0.1 mol/L Na2SO4+0.1 mol/L CH3COONH4;2号溶液:0.01 mol/L Mn(CH3COO)2+0.1 mol/L Na2SO4+0.1 mol/L CH3COONH4;3号溶液:0.1 mol/L Mn(CH3COO)2+0.1 mol/L Na2SO4+0.1 mol/L CH3COONH4。 再配制0.1 mol/L Na2SO4溶液用于电容性能测试。
ITO导电玻璃切割成1 cm×4 cm的长方形,在无水乙醇中超声清洗5 min,晾干,用金手指胶带封装,留出1 cm×1 cm的工作面。
在三电极体系下分别对1号、2号、3号溶液进行循环伏安测试,设置初始电势和低电势为-0.2 V、高电势为1.0 V,扫描速度0.01 V/s,圈数3圈。 根据测试的CV曲线峰电势,确定MnO2氧化沉积电势,1号溶液分别设置为0.518、0.515、0.512、0.505和0.498 V、2号溶液:0.450、0.433、0.425和0.418 V、3号溶液:0.380、0.372、0.365和0.360 V,设置初始电势为0 V、低电势为-0.1 V,进行MnO2电沉积。 制备好的MnO2电极用超纯水清洗3次晾干后在80 ℃下干燥30 min待测。 拟合实验数据,分析成核机理。
以0.1 mol/L Na2SO4溶液为电解质,在三电极体系下对已制备的MnO2电极进行电容性能测试。 CV测试以初始电势和低电势0 V、高电势0.8 V、0.02 V/s的速度扫3圈;CP测试在阴极电流和阳极电流0.0005 A、高电势0.8 V、低电势0 V的条件进行;电化学阻抗谱(EIS)测试设置初始电平0.3、振幅5 mV、高频10000 Hz、低频0.01 Hz,静置时间400 s。
电化学阳极氧化法制备MnO2电极材料,文献普遍报道的MnO2沉积反应方程式是:
Mn2++4OH-=MnO2+2H2O+2e-
溶液组成、温度、阳极电流密度(阳极过电势)等沉积参数会影响电极表面沉积物的形貌。 通过调节沉积参数,可控制MnO2电结晶过程[12]。 计时电流法通常用于研究沉积初始阶段的成核与生长机理;根据SH的理论模型,瞬时成核和连续成核的归一化电流可分别表示为[7,8]:
式中, Im和 tm分别为 i-t曲线在最大电流密度处所对应的电流值和时间。
通过测量MnO2沉积初始的 i-t曲线,经归一化处理,与瞬时成核和连续成核的SH理论曲线比较,即可判断成核机理。 本实验只改变Mn2+的浓度,支持电解质浓度不变,开路电势阶跃到不同电势下的 i-t曲线,如图1 A、2 A及3 A所示,在电势阶跃初始阶段均非常快速的出现 Im,然后电流减小并出现非零极限电流。 tm与阶跃电势有关,实验结果显示沉积电势越正, tm越短。 i-t曲线会出现峰值电流,是由于Mn2+离子在ITO电极表面放电成MnO2核并生长,使电流增大,随着MnO2核之间的相互交叠而使电流衰减直至达到一个电流增加与衰减的平衡过程;而 i-t曲线在达到最大值后下降至平台阶段,可认为是扩散控制阶段, i-t曲线可由Cottrell方程描述,其电流与 t1/2成正比[16,18]。
根据SH的理论模型, t/tm取值范围为0~5,取值间隔为0.1,然后代入方程(1)和(2)分别计算出对应的( I/Im)2值,以( I/Im)2对 t/tm做图,可分别得到瞬时成核和连续成核的归一化电流时间理论曲线。 将实测电流时间归一化曲线,叠加到理论曲线图上,判断MnO2成核生长机理。 根据图1 B、2 B和3 B,可以推断在1号溶液中MnO2成核机理更符合连续成核机理;而在2号溶液中MnO2成核在达到最大电流之前归一化曲线与连续成核更吻合,达到最大电流之后与瞬时成核更吻合,可认为其成核过程同时存在两种成核方式;3号溶液中MnO2成核机理更符合瞬时成核机理。
根据 i-t曲线,分别选择1号溶液在0.515 V,2号溶液在0.418 V,3号溶液在0.365 V制备的MnO2作为对应成核机理的典型电极进行电容性能测试,对应1号、2号和3号电极。
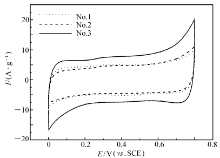
研究表明电流较大、阴阳极电流对称性好的矩形伏安图表明电极材料的电容性能好[17]。图4所示为1号、2号和3号MnO2电极在0.1 mol/L Na2SO4溶液中的循环伏安曲线,扫描速度为20 mV/s。 可以明显看出,3种电极的CV曲线均呈现矩形的特征,表明均有较好电容性能;其中3号电极CV电流明显大于1、2号电极的CV电流,而后二者电流基本接近。 参照文献[10]估算活性物质MnO2质量(此法只关注沉积反应所耗电量用于生成MnO2,排除沉积物中水分及溶液阳离子等,有很高的可信度),通过积分CV封闭曲线的面积,求算出电量值,最终计算出1、2和3号MnO2电极的比电容值分别为253、238和417 F/g。 3号MnO2电极经瞬时成核后,核数不再增加,后续沉积过程就是已生成核的长大过程,这种有限核数的生长方式更有利于生成如图5 C所示稀疏多孔的纳米片及纳米棒,而这种比表面高的沉积物通常表现出更高的电容性能[6,19]。 1号和2号MnO2电极有连续成核的过程,即在沉积过程中同时有核的长大和形成过程,核数不断增多和已形成的晶核不断长大,使得沉积物较为紧密,如图5 A、 B所示,从而导致电容性能较低[12]。
 | 图5 不同沉积方式的3种电极的SEM照片Fig.5 SEM of MnO2 electrodes with progressive( A), mixed( B) and instantaneous( C) electrodeposition nucleation mechanisms |
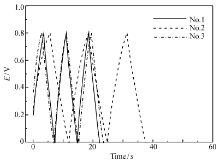
充放电实验由计时电势实验测得[20]。图6所示为MnO2电极在0.1 mol/L Na2SO4溶液中充放电能力的计时电势法测试曲线,阴阳极恒电流设定为0.5×10-3 A/cm2。 由公式 Cs= C/m和 C=IΔ t/Δ E(式中, Cs为比电容, C为电容, m为活性物质的质量, I为放电的电流值,Δ t为放电时间,Δ E为电压降),计算1号、2号和3号MnO2电极的比电容值分别为210、183和346 F/g。 由计算结果可看出,充放CP测得的电容值与CV测得电容值有偏差,但这两种方法测得的3种电极材料的电容值的相对大小的规律是一样的。
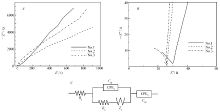
关于超级电容材料的研究大多集中在提高电极材料的功率比及频响特性,其中频响特征可由交流阻抗谱来测试[17,21,22]。 通过等效电路解析电化学阻抗谱获得电荷转移、电子电导以及离子电导电阻的数据,是表征电极材料超级电容性能的重要手段。图7 A所示为1、2、3号电极在0.1 mol/L Na2SO4溶液中阻抗Nyquist图。图7 B为局部放大图。图7 B中显示在高频区的阻抗弧是一个1/4的圆弧,反映的是双电层非法拉第充放电过程,远远快于法拉第过程;在低频区是虚部随频率快速上升的线性区,反映的是典型的电容特性,主要由电极材料的法拉第过程控制[21]。 由图7 C等效电路模型,其中 Rs为溶液电阻, Rct为赝电容过程电荷转移电阻,CPE1界面双电层充电电容, Zw为浓差极化引起的Warburg阻抗,CPE2为非理想电容[23],采用Zview软件拟合阻抗谱数据,拟合结果包括 Rct、扩散电阻 W-R、扩散时间常数 τ,以及赝电容 Cps,结果如表1所示。 Rs均小于30 Ω,并且低频区域的谱线接近垂直,3号电极尤为明显,这些特征均预示着制备出的MnO2材料是较为理想的超级电容电极材料。 根据 Cps算质量比电容[23]可得1号、2号和3号电极的比电容值分别为190、124和312 F/g;表明3号电极材料的电容较另外两种好,这与CV、CP测试结果的规律一致。
| 表1 交流阻抗数据拟合结果 Table 1 Fitting results of EIS of MnO2 electrodes with three different electrodeposition approaches |
采用计时电流法研究不同浓度Mn2+溶液中MnO2沉积行为,通过对所测的暂态 i-t曲线归一化处理,并与SH理论模型的归一化曲线比较,判断MnO2成核机理。 结果发现,在0.1 mol/L Mn2+溶液中,电势阶跃至0.365 V初始成核更符合瞬时成核;在0.01 mol/L Mn2+溶液中,电势阶跃至0.418 V初始成核存在瞬时成核和连续成核两种成核机理;在0.5 mmol/L Mn2+溶液中,电势阶跃至0.515 V初始成核更符合连续成核。 然后对这3种成核方式得到的MnO2电极材料分别采用循环伏安法、计时电势法以及交流阻抗法等测试方法进行测试。 结果发现,瞬时成核更易于形成多孔、纳米片/棒等高比表面的沉积物,这种方式制得的MnO2电极相对于另外两种电极有更好的电容性能,体现了制备方法影响MnO2电容性能的情况。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|