合成了弱配体柠檬酸三钠修饰的CdS量子点(Cit-CdS QDs), 透射电子显微镜表征结果表明, Cit-CdS QDs的粒径分布均匀(4~6 nm), 分散性好。 研究了金属离子(银(Ⅰ)离子、镉(Ⅱ)离子)、巯基化合物(巯基乙酸、半胱氨酸)以及金属离子(银(Ⅰ)离子、镉(Ⅱ)离子)与巯基化合物形成的配合物对Cit-CdS QDs荧光的影响。 发现金属离子(银离子、镉离子)与巯基化合物(巯基乙酸、半胱氨酸)形成的水溶性配合物可以显著增强Cit-CdS QDs的荧光, 配合物对Cit-CdS QDs的增强程度比单独的金属离子或巯基化合物均要高, 而且配合物修饰的CdS QDs对铜(Ⅱ)离子的响应要高于单独用金属离子或巯基化合物修饰的量子点。 建立了铜(Ⅱ)离子高灵敏度荧光检测方法, 该方法检测范围宽(1.0×10-8~1.0×10-6 mol/L), 检测限低(1.0×10-9 mol/L)且具有很好的选择性, 拓展了配合物作为量子点修饰剂的应用。
CdS quantum dots capped by citrate(Cit-CdS QDs) were synthesized in aqueous solution. TEM analysis indicates that the Cit-CdS QDs are well-dispered with the diameter of 4 to 6 nm. The influence of silver(Ⅰ), cadmium(Ⅱ), thioglycolic acid, cysteine and the complexes formed by silver(Ⅰ)/cadmium(Ⅱ) with the thiol compounds(thioglycolic acid or cysteine) on the fluorescence of Cit-CdS QDs was investigated. All above modifiers can enhance the fluorescence intensity of Cit-CdS QDs. The complexes above have much greater fluorescence enhancement effect than that of the solely metal ions or thiol compounds. In addition, the CdS QDs modified by the complexes also have much higher sensitivity for copper(Ⅱ) sensing. Based on this phenomenon, a highly sensitive and selective fluorescence probe for Cu2+ was developed with a wide range of 1.0×10-8~1.0×10-6 mol/L and a low detection limit of 1.0×10-9 mol/L. It may open up new opportunity for the synthesis and application of complex modified quantum dots in analytical chemistry.
量子点具有发射光谱窄、Stocks位移大、抗光漂白能力强以及发射波长随粒径尺寸可调谐等优良的光学性质[1,2,3]。 因此相对于常规的有机分子探针, 量子点作为荧光探针在化学传感器领域具有更为显著的优势[4,5]。 由于其具有较大的比表面积, 量子点的荧光性质对其表面状态的变化非常敏感。 一方面, 通过合适的表面修饰可以提高量子点的发光效率。 例如, Henglein等[6]发现, 碱性溶液中加入镉(Ⅱ)离子使CdS的荧光量子产率增加了50%。 这是由于CdS表面形成了Cd(OH)2壳层, 从而有效地消除了光生载流子的非辐射跃迁中心。 人们也发现, 碱性条件下, 镉(Ⅱ)离子和锰(Ⅱ)离子对于CdS和ZnS的荧光具有增强作用[7,8]。 另一方面, 量子点的表面修饰能够调控其作为荧光探针检测目标物的选择性和灵敏度, 因此, 可以通过量子点表面修饰基团的调控达到特定的分析目的。 当前的研究几乎均采用有机化合物如巯基化合物[9,10,11,12,13]、壳聚糖[14]、三乙醇胺[15]等来修饰量子点。
在本研究中, 首次采用金属离子(镉离子、银离子)与巯基化合物(巯基乙酸、半胱氨酸)形成的水溶性配合物修饰量子点。 发现这些水溶性配合物不仅能显著提高量子点的荧光, 而且配合物的修饰能使量子点对铜(Ⅱ)离子具有非常灵敏的响应。 本研究开拓了配合物作为量子点修饰剂的新应用。
Cary Eclipse型荧光分光光度计(美国瓦里安公司);TU-9001型紫外分光光度计(北京普析通用仪器有限责任公司);JEOL JEM-2100型高分辨率透射电子显微镜(日本日立公司);PHS-3 C型酸度计型(上海雷磁公司);超纯水制备装置(香港Healforce公司);移液枪(德国Eppendorf公司)。
CdCl2·2.5H2O, 巯基乙酸, 柠檬酸三钠, 半胱氨酸盐酸盐, 硝酸银, 硝酸铜, 以上试剂均为分析纯, 购自国药集团化学试剂有限公司。 Na2S·9H2O(分析纯), 购自上海凌风化学试剂有限公司。
柠檬酸三钠修饰的CdS量子点(Cit-CdS QDs)按照本实验室之前的方法[5]制备:搅拌条件下, 含有5.0×10-4 mol/L的CdCl2和2.5×10-3 mol/L的柠檬酸三钠的40 mL水溶液中通入高纯N2气除氧30 min后加入10 mL 2.0×10-4 mol/L的Na2S水溶液。 上述反应溶液在通氮气状态下继续反应30 min, 制得柠檬酸三钠修饰的水溶性的CdS量子点。
不同的表面修饰物质如金属离子-巯基化合物形成的配合物(Cd2+/Ag+-巯基乙酸配合物或者Cd2+/Ag+-半胱氨酸配合物)、巯基化合物(巯基乙酸或者半胱氨酸)、金属离子(Cd2+或者Ag+)被用于修饰CdS QDs。
1)配合物修饰的量子点的制备如下:通过溶解一定量的CdCl2以及巯基乙酸或者半胱氨酸盐酸盐于20 mL 柠檬酸缓冲(pH=7.0)溶液中制备5.0×10-3 mol/L的Cd2+-巯基乙酸(Cd-TGA)/Cd2+-半胱氨酸(Cd-Cys)配合物溶液(配合物中Cd2+与巯基乙酸或者半胱氨酸的摩尔比为1:2)。 将不同体积的上述配合物溶液加入到50 mL Cit-CdS 溶液中室温下反应2 h得到表面修饰有不同量的Cd-TGA/Cd-Cys的CdS QDs。
同样方法制得Ag+-巯基乙酸(Ag-TGA)/Ag+-半胱氨酸(Ag-Cys)修饰的CdS QDs。
2)巯基化合物(TGA/Cys)修饰的CdS QDs同样按照1)的方法制备, 即把步骤1)中的Cd2+或者Ag+去掉。
3)Ag+/Cd2+修饰的CdS QDs按如下步骤制备:将1.0 mL不同浓度的金属离子加入到Cit-CdS QDs与柠檬酸缓冲(pH=7.0)溶液的混合溶液中, 室温下反应1 h得到表面修饰有不同量的Ag+/Cd2+的CdS QDs。
0.01 mol/L的铜离子储备液由CuSO4溶解于pH=7.0的柠檬酸缓冲溶液中得到。 其它浓度的Cu2+溶液由此溶液逐级稀释得到。
1 mL不同物质修饰的CdS QDs, 1 mL 0.1 mol/L的柠檬酸缓冲溶液(pH=7.0)以及不同浓度的铜离子溶液依次加入比色管中, 反应10 min 后测定荧光强度。
图1 A为所合成的Cit-CdS QDs的发射光谱。 用370 nm的波长激发后, Cit-CdS QDs的最大发射波长位于620 nm。 柠檬酸钠是较弱的表面配体, 不能很好地钝化量子点的表面, 导致合成的CdS QDs表面具有较多的表面缺陷, 产生较宽的发射峰。 从高分辨透射电子显微镜照片(图1 B)上可以看出, 所合成的CdS QDs的粒径较为均匀, 粒径大小在4~6 nm。
柠檬酸三钠(Cit)和CdS量子点表面的结合较弱, 其它修饰物质如金属离子、巯基化合物很容易结合到量子点表面上, 量子点的光学性质对其表面状态特别敏感, 这些物质的结合使得量子点的荧光发生了变化。 如图2 A~2 D, 银离子(Ag+)、镉离子(Cd2+)、巯基乙酸(TGA)以及半胱氨酸(Cys)均能够使得Cit-CdS QDs的荧光不同程度的增强。 荧光增强是由于这些物质钝化了量子点的表面缺陷, 从而降低了非辐射跃迁的几率, 使得辐射跃迁增强。
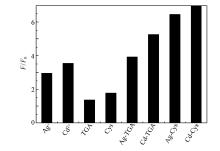
 | 图2 不同的修饰物质对Cit-CdS量子点荧光的影响Fig.2 The influence of different modifiers on the fluorescence of Cit-CdS quantum dots A.Ag+; B.Cd2+; C.TGA; D.Cys; E.Ag-TGA; F.Cd-TGA; G.Ag-Cys; H.Cd-Cys |
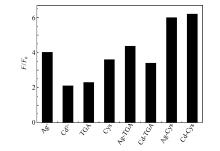 | 图3 不同修饰物质对Cit-CdS QDs的最大荧光增强程度Fig.3 The maximum fluorescence enhancement of Cit-CdS quantum dots by different surface modifiers |
一些金属离子如镉离子等能够很容易使得一些配体(如巯基化合物)的电子云极化, 从而形成稳定的配合物[16,17]。 在偏碱性环境中, 金属离子与巯基化合物倾向于形成配合比为1:2的水溶性产物。 而当溶液的pH值较低时, 金属离子与巯基化合物倾向于形成配合比为1:1的不溶性产物, 很容易从水溶液中沉淀出来[16,17]。 我们在pH值为9.0的柠檬酸缓冲溶液中加入摩尔浓度比为1:2的金属离子以及巯基化合物, 制备了镉离子-巯基乙酸(Cd-TGA)、镉离子-半胱氨酸(Cd-Cys)、银离子-巯基乙酸(Ag-TGA)以及银离子-半胱氨酸(Ag-Cys)的水溶性配合物。 实验中发现, 这些配合物的加入同样能增强量子点的荧光(图2 E~2 H), 所有的修饰物质(包括金属离子、巯基化合物、金属离子-巯基化合物形成的配合物)对量子点荧光的增强程度均与修饰物质的浓度有关。 当Ag+、Cd2+、TGA、Cys、Ag-TGA、Cd-TGA、Ag-Cys、Cd-Cys的浓度分别为1.0×10-6、2.0×10-4、8.0×10-4、1.4×10-3、1.2×10-6、6.67×10-5、3.8×10-6、2.67×10-4 mol/L时, 使得该物质修饰的量子点的荧光强度达到最大。
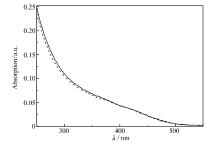
图3为不同的修饰物质对量子点荧光的最大增强程度( F/F0)。 F0以及 F分别表示Cit-CdS量子点在被其它物质修饰前后的荧光强度。 从图3可以看出, 金属离子、巯基化合物及二者形成的水溶性配合物均能使Cit-CdS量子点的荧光不同程度的增强, 而且水溶性配合物对Cit-CdS量子点荧光的增强程度要远远大于单一的金属离子或者巯基化合物对Cit-CdS量子点荧光的增强程度。图4为不同的修饰物质对Cit-CdS量子点的紫外吸收光谱的影响。 从图4可以看出, 经过不同物质修饰过的CdS量子点的紫外响应均发生了一定程度的位移, 说明这些物质已经成功修饰到了CdS表面上。 Trung等[18]认为, 发光效率主要依赖于半导体表面或粒子内部缺陷的数量, 当缺陷较多时, 绝大多数电子以非辐射的形式去活化, 发光效率明显降低。 柠檬酸钠是较弱的表面配体, 不能很好地钝化量子点的表面, 导致合成的CdS 量子点表面具有较多的表面缺陷, 荧光强度较低[19], 而量子点表面修饰的配合物能更好的钝化量子点的表面缺陷, 可以很大程度上降低量子点的表面缺陷, 增强量子点光敏性, 从而提高了CdS量子点的荧光强度[20,21,22]。
我们研究了不同物质修饰后的CdS量子点与铜离子的相互作用。 发现铜离子对不同物质修饰后的CdS量子点的荧光均有猝灭作用, 铜离子对配合物修饰的CdS量子点的荧光猝灭程度要远远大于其对单一金属离子或巯基化合物修饰CdS量子点的荧光猝灭程度(图5)。 这表明 配合物修饰的CdS量子点不仅具有较强的荧光强度, 并且对铜离子具有更加灵敏的响应。 因此, 我们用Cd-Cys修饰的CdS量子点对铜离子进行了测定。
另外, 还发现铜离子对不同物质修饰的量子点的荧光猝灭作用受到溶液pH值的影响。 当溶液的pH值为6.5~7.0时, 铜离子对所修饰的量子点的荧光猝灭程度最大。 因此, 选择在pH值为7.0的柠檬酸缓冲溶液中进行铜离子的测定。
从图6 A可以发现, 随着铜离子浓度的不断增大, Cd-Cys修饰的CdS QDs的荧光强度逐渐降低。 在铜离子的浓度为1.0×10-8~1.0×10-6 mol/L范围内, 荧光降低程度与铜离子浓度呈现线性关系(图6 B), 检测限为1.0×10-9 mol/L( S/N=3)。 铜离子对Cd-Cys修饰的CdS量子点的荧光程度符合Stern-Volume方程[4]: F0/ F=1+ Ksv[Q]=1+6.35×106[C
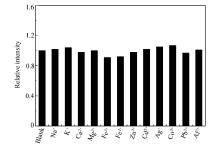 | 图7 其它金属离子(2.0×10-6 mol/L)对Cd-Cys修饰的CdS量子点荧光的影响Fig.7 The influence of other metal ions(2.0×10-6 mol/L) on the fluorescence of CdS quantum dots modified by Cd-Cys |
并不能引起Cd-Cys修饰的CdS量子点的荧光的明显变化(图7), 说明Cd-Cys修饰的CdS量子点对于铜离子的测定具有较好的选择性。利用Cd-Cys修饰的CdS QDs对实际样品中的铜离子进行了测定。 不经过任何方法处理, 直接取自来水, 采用标准加入法对水样中的Cu2+进行测定, 用外推法算得所测水样中Cu2+含量为80.5 nmol/L。 对3个不同浓度的Cu2+进行测定的回收率在97.6%~107%之间 (表1), 说明该方法能较好的用于实际样品中铜离子的测定。
| 表1 实际样品的测定结果 Table 1 Analysis results for real samples |
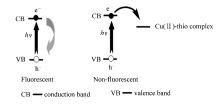
量子点的荧光猝灭机制可以通过内滤效应、非辐射复合、电子转移等[23]机理来解释。 从吸收光谱(图8)上可以看出, 加入Cu2+后的吸收光谱并未发生红移, 表明该体系中Cu2+并未结合到量子点表面, 从而未引起量子点表面态的改变[24]。 我们推测, Cu2+所引起的荧光猝灭是由于电子转移引起的[12,25]。 Touceda-Varela等[26]发现铜离子配合物如(铜(Ⅱ)-联吡啶配合物)可以有效通过电子转移机理猝灭量子点的荧光。 由于铜与硫的结合能(Cu—S, 276.0 kJ/mol)大于镉与硫的结合能(Cd—S, 208.4 kJ/mol)[27]。 因此, 铜离子能够取代镉离子与巯基化合物形成的配合物中的镉离子, 从而靠近量子点表面。 从图9 B铜(Ⅱ) -半胱氨酸配合物的循环伏安图可以看出, 铜(Ⅱ)-半胱氨酸配合物的还原电位为-0.15 V( vs.Ag/AgCl), 从图9 A的CdS量子点的阴极线性电位扫描曲线可以看出, 其导带电位是-1.25 V( vs.Ag/AgCl)。 因此, 激发态的量子点的光生电子容易转移到铜离子与巯基化合物形成的配合物上, 导致辐射跃迁的降低。铜离子的测定机理示意图如图10所示。
通过金属离子(镉离子/银离子)与巯基化合物(巯基乙酸、半胱氨酸)形成的水溶性配合物修饰CdS量子点, 能显著提高量子点的荧光强度。 尤其是镉离子-半胱氨酸配合物修饰的量子点具有最大的荧光强度。 镉离子-半胱氨酸配合物修饰的量子点对铜离子的检测表现了较高的灵敏度和较好地选择性。 该研究为量子点的表面修饰及应用提供了一种新途径。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|