利用反相悬浮聚合法, 成功制备了微米级硫氰酸根(SCN-)阴离子印迹微球。 以溶有分散剂Span-60的环已烷为分散介质, 以溶有模板阴离子SCN-、阳离子单体丙烯酰氧乙基三甲基氯化铵(DAC)及交联剂 N, N'-亚甲基双丙烯酰胺(MBA)的水溶液为分散相, 构成反相悬浮聚合体系, 在水相液滴中使DAC发生交联聚合, 成功制备了粒径约为200 μm的离子印迹微球(IIPMs)。 以同为一价阴离子的N
Micron-sized thiocyanate anion-imprinted microspheres(IIPMs) were prepared successfully with inverse suspension polymerization method. In the inverse suspension polymerization system, cyclohexane was used as dispersion medium and Span-60 was used as dispersant in the oil phase, cationic monomer of acryloxyethyltrimethyl ammonium chloride(DAC), the crosslinker N, N'-methylene bisacrylamide(MBA) and the template SCN- anion were dissolved in aqueous phase. The crosslinking copolymerization of DAC in water-in-oil droplets was carried out and SCN- IIPMs with diameter of about 200 μm were obtained. The ion recognition selectivity and binding property were investigated with monovalent anions, N
硫氰酸根离子(SCN-)广泛存在于多种工业废水中, 比如电镀、炼焦、采矿、金属冶炼、合成农药与印染等工业废水。 SCN-离子具有一定的毒性, 水介质中SCN-离子的存在不仅对人体健康造成危害, 而且会严重污染水生动植物的生态环境[1,2]。 因此, 寻求科学有效的手段, 去除水体中的SCN-离子, 对于环境保护和人体健康均具有重要的科学意义。 去除水体中SCN-离子的方法有吸附法、离子交换法、溶剂萃取法、氧化法和生物降解法等, 在这些方法中, 吸附法处理效率高, 使用方便且成本低[3,4]。 但是, 一般的固体吸附剂均有着一个共同的缺点, 即不具备吸附选择性, 而分子印迹材料(MIPs)是迄今为止识别选择性最好的固体吸附剂, 而且在一般情况下, MIPs均可以回收再循环使用。 因此, 利用MIPs从水介质中去除SCN-阴离子, 具有重要的环保价值。
分子印迹是在聚合物基质中对目标物构建识别位点的高效技术, 因此, MIPs对模板分子(离子)具有特异的识别选择性, 常被人们称为人工抗体或受体(Artificial antibodies or receptors)[5,6]。 近年来, MIPs大量用于物质的分离与纯化, 同时在环境保护与治理领域也得到广泛应用, 以MIPs为固体吸附剂, 可高效地去除水介质中各类毒性物质[7,8,9]。 制备MIPs的传统方法是包埋法, 该方法有明显的缺点:在粉碎研磨块状MIPs的过程中, 大量识别位点被破坏, 所获得的印迹聚合物微粒内部印迹空穴数目有限, 对模板分子(离子)结合性能不高;微粒内基质较厚, 孔道较深, 对模板分子的再结合扩散阻力大, 传质慢, 不易与识别位点结合[10,11]。 为有效地克服上述缺点, 进一步促进分子印迹技术的发展, 研究者们提出了几种有效解决途径, 如分子表面印迹技术, 分子印迹膜技术和直接制备微、纳米分子印迹微球(微粒)等方法[12,13,14], 大大提高了分子(离子)印迹的效率。
在微、纳米印迹微球的直接制备过程中, 分子(离子)的印迹与成球过程同步进行, 产物微球中分布有丰富的印迹空穴, 又由于微球比表面大, 孔道浅, 与印迹模板分子的可接近性好, 因此对目标物的识别速度快、结合能力强。 直接制备的微、纳米印迹微球可高效地用于固相萃取、色谱固定相、有害物质的去除和物质的分析检测等[15,16,17,18]。 直接制备微、纳米印迹微球的方法也有几种, 如沉淀聚合法、种子聚合(多步溶胀-聚合)法和悬浮聚合法[19,20,21]。 悬浮聚合法一般用于制备微米级印迹微球, 微米级印迹微球在实际使用中具有易于处理的优点。 在研究者们所采用的制备印迹微球的悬浮聚合体系中, 多为以水为分散介质的(正相)悬浮聚合体系(印迹微球是在油相中形成)[22,23], 而采用以有机溶剂为分散介质、以水溶液为分散相的反相悬浮聚合体系制备印迹微球的研究并不多见。 采用反相悬浮聚合体系制备的印迹微球有着明显的特点:非常适合在水介质中使用, 因为该印迹微球是在水相中形成的, 故在水介质中可保持印迹空穴良好的“识别记忆”特性。 基于此认识, 本研究以阳离子单体丙烯酰氧乙基三甲基氯化铵(DAC)为功能单体, 采用反相悬浮聚合法制备微米级硫氰酸根离子印迹微球(IIPMs), 深入考察研究其离子识别特性, 评价其从水介质中去除硫氰酸根离子的性能。 在不同的工业废水中, 往往溶解有各种不同的有毒有害的阴离子。本研究采用反相悬浮聚合法制备阴离子印迹微球的思路, 具有新意, 在环境保护与治理领域具有明显的参考价值。
丙烯酰氧乙基三甲基氯化铵(DAC, 上海广创景进出口有限公司), 分析纯; N, N'-亚甲基双丙烯酰胺(MBA, 上海原液生物科技有限公司), 分析纯;环己烷(天津市风船化学试剂科技有限公司), 分析纯;山梨醇酐单硬脂酸酯(Span-60, 天津市光复精细化工研究所), 分析纯;过硫酸铵(APS, 国药集团化学试剂有点公司), 分析纯;硫氰酸胺(NH4SCN, 成都化学试剂厂), 分析纯;硝酸钠(NaNO3, 北京红星化工厂), 分析纯;碘化钾(KI, 天津大茂化学试剂厂), 分析纯;其它试剂均为市售分析纯试剂。
UV-2602型紫外可见分光光度计(上海尤尼柯公司);1700型傅里叶红外光谱仪(FTIR, 美国Perkin-Elmer公司);438VP型扫描电子显微镜(SEM, 英国LEO公司);XSZ-4型带有测微尺的光学显微镜(双目生物显微镜, 太原光学仪器厂);DM6236P型非接触式转速测定器(深圳市胜利高电子科技有限公司)。
在装有搅拌, 冷凝管, 导气管的四口烧瓶中, 加入40 mL的环己烷, 再向其中加入1.8 g分散剂Span-60, 构成连续相油相。 将4.3 mL丙烯酰氧乙基三甲基氯化铵(DAC)、0.23 g N, N'-亚甲基双丙烯酰胺(MBA)和0.51 g硫氰酸胺溶于8 mL蒸馏水中构成水相。 在油相中通N2气30 min, 以排除体系内的空气, 并将其加热到55 ℃。 在水相中再加入0.025 g的引发剂过硫酸铵, 溶解后转移至一恒压滴液漏斗中, 以一定的速度缓慢滴加到在搅拌状态下的油相中, 10 min内滴加完毕, 然后将体系温度迅速升温至65 ℃。 控制搅拌速率在400 r/min附近, 在N2气保护下使悬浮聚合反应进行4 h。 反应结束后, 趁热过滤, 得到透明微球。 用环己烷多次洗涤微球, 除去物理吸附在微球表面的分散剂;然后用浓度为2 mol/L的NaCl溶液多次浸泡洗涤印迹微球, 以脱除模板离子SCN-(用硝酸铁溶液检测, 直至洗涤液为无色为止), 真空干燥至恒重, 即得硫氰酸根阴离子印迹微球IIPMs(经干燥, 微球的体积会明显收缩)。
为进行性能对比, 也在不加模板硫氰酸胺的条件下, 采用反相悬浮聚合法制备了非印迹微球(NIPMs), 即DAC的交联聚合微球CPDAC。
采用KBr压片法测定SCN-阴离子印迹微球IIPMs的红外光谱图, 表征其化学结构;使用扫描电子显微镜(SEM), 分别观察反相悬浮聚合时不加模板离子SCN-所制得的交联微球NIPMs与印迹微球IIPMs的形貌, 比较相互间差异。
1.4.1 等温结合实验 首先采用静态法考察印迹微球对SCN-的结合特性.先测定印迹微球对SCN-离子的结合动力学行为, 确定结合达到平衡的时间为3 h, 在此基础上, 进行等温结合实验。 配制浓度系列变化(1~7 mmol/L)的硫氰酸胺溶液, 将25 mL浓度不同的溶液分别置于若干具塞锥形瓶中, 加入准确称量的约0.03 g的印迹微球IIPMs, 在恒温振荡器中于25 ℃下振荡3 h, 使微球充分溶胀, 并使之对SCN-离子的结合达到平衡, 离心分离, 采用硝酸铁分光光度法测定上清液中硫氰酸根的平衡浓度, 按照式(1), 计算印迹微球IIPMs对SCN-的平衡结合量 Qe(mmol/g), 并绘制等温结合线。
式中, c0、 ce分别为结合前后溶液中硫氰酸根的浓度(mmol/L); V为吸附液体积(mL); m为印迹微球IIPMs的质量(g)。
硝酸根、碘离子与硫氰酸根离子均是是一价阴离子, 故选用N
上述3种离子测定方法简述如下:1)SCN-离子的测定:在25 mL的容量瓶中加入1 mL待测硫氰酸根溶液(浓度范围为1~7 mmol/L), 再加入5 mL浓度为0.05 g/L的硝酸铁储备液(pH值为1~2), 蒸馏水定容混匀, 在波长为 λ=450 nm处测定其吸光度, 利用已测定的工作曲线计算所测溶液中SCN-离子的浓度;2) N
1.4.2 竞争吸附实验 配制各组分浓度均为6 mmol/L的SCN-/N
式中, Kd(L/g)为某组分离子的分配系数; ce(mmol/L)为上清液中该离子的平衡浓度; Qe(mmol/g)为该离子的平衡结合量。
按式(3)计算离子印迹微球IIPMs相对于两种对比离子对SCN-离子的选择性系数 k。 k的大小标志着印迹材料对模板分子或离子的识别选择系数, 它是评价印迹材料对模板物质识别性能最重要的性能指标之一。式中, Kd(SCN-)为SCN-离子的分配系数, K'd为某一对比离子的分配系数。
1.4.3 重复使用性能的考察 在进行等温结合实验后, 用浓度为2 mol/L的NaCl溶液多次浸泡洗涤离子印迹微球IIPMs, 完全脱除模板离子SCN-(用硝酸铁溶液检验至洗液中无红色络合物形成), 真空干燥至恒重后, 再重复进行等温结合实验, 测得饱和结合量。重复进行多次, 绘制饱和结合量与使用次数之间的关系曲线, 评价印迹微球的重复使用性能。
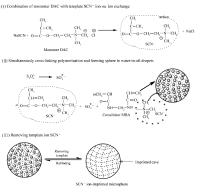
在反相悬浮体系的水相液滴中, 凭借强静电相互作用(或离子交换作用), 单体DAC与SCN-阴离子紧密地相互作用为离子对;水滴中的过硫酸盐分解产生自由基;该自由基引发DAC及交联剂MBA发生交联聚合反应, 形成交联微球, 与此同时, SCN-阴离子被包埋于交联网络中;除去模板离子后, 在聚合物微球中留下了大量的SCN-阴离子印迹空穴, 从而形成了SCN-阴离子印迹微球IIPMs。 在水相液滴中形成阴离子印迹微球IIPMs的物理化学过程及其微观结构如Scheme 1所示。
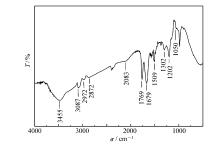
2.2.1 红外光谱图1给出了离子印迹微球IIPMs的红外光谱。 在谱图中显示出了交联共聚微球结构中单体DAC单元与交联剂MBA单元的所有特征吸收:1)1769 cm-1处的强峰吸收来自于DAC单元酯羰基的吸收, 1202 cm-1处的峰
归属于酯基中C—O键的振动吸收, 2972和2872 cm-1处的峰分别归属于聚合物主链上亚甲基及次甲基的C—H键的伸缩振动吸收, 2083 cm-1处的吸收带应归属于季铵基团中C—N—C的特征吸收, 3455 cm-1处的峰来自于季铵阳离子吸附水O—H键的伸缩振动吸收。 2)1670 cm-1处的吸收峰是MBA单元酰胺羰基的伸缩振动吸收峰(酰胺Ⅰ带), 而3087 cm-1处的吸收峰为MBA单元仲酰胺基团中N—H键的变性振动吸收(酰胺Ⅱ带), 1050 cm-1处的吸收峰应该为酰胺基团中C—N键的振动吸收。 上述谱峰数据充分说明, 在反相悬浮聚合体系中, 阳离子单体DAC与交联剂MBA发生了交联共聚合, 形成了离子印迹微球IIPMs。
2.2.2 微球形貌图2给出了交联微球NIPMs和离子印迹微球IIPMs湿态时的SEM照片。 从图2可以看出, 交联微球即非印迹微球NIPMs不仅球形度良好, 大小尺寸分布比较均匀, 粒径在200 μm附近, 而且表面十分光滑;而离子印迹微球IIPMs虽然球形度也比较好, 粒径也在200 μm附近, 但表面坑洼不平, 比较粗糙, 笔者认为, 这可能是在交联聚合过程中聚合链网络中存在模板离子引起的。
2.3.1 等温结合曲线 分别使用非印迹微球NIPMs和SCN-阴离子印迹微球IIPMs对SCN-、N
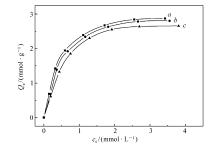 | 图3 非印迹微球NIPMs对3种阴离子的吸附等温线Fig.3 Adsorption isotherms of non-imprinted microspheres NIPMs for three anions a. SCN-; b.N |
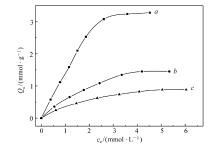 | 图4 印迹微球IIPMs对3种阴离子的的结合等温线Fig.4 Binding isotherms of imprinted microspheres IIPMs for three anio a.SCN-; b.N |
图3显示, 非印迹微球NIPMs对3种阴离子均具有高的吸附量, 且吸附容量相差不多, 饱和吸附量在2.7~2.9 mmol/g的范围, 显然吸附没有选择性。 非印迹微球NIPMs内部, 在无规交联网络中键联有大量的季铵阳离子, 微球在水介质中会发生高度的溶胀行为, 对水介质中的阴离子具有高度的可接近性, 在静电相互作用(或离子交换作用)下, 会强烈地将水介质中的阴离子吸引至溶胀微球的交联网络中, 导致高吸附容量。 SCN-、N
但是,图4显示, 经SCN-阴离子印迹而形成的印迹微球IIPMs, 对3种阴离子的等温结合曲线发生了实质性的变化: 1)印迹微球IIPMs对两种对比阴离子的结合容量大大降低, N
| 表1 3种阴离子的离子半径和几何构型 Table 1 Ionic radius data and geometrical configuration of three anions |
SCN-离子是直线型离子, N
2.3.2 选择性系数 使用非印迹微球NIPMs和印迹微球IIPMs, 对两种二元混合液分别进行了竞争吸附实验,表2与表3列出了两体系中各组分离子的分配系数及两种微球对SCN-离子的选择性系数。
| 表2 SCN-/N |
从表2的数据可以看出, 使用非印迹微球NIPMs在两种二元混合液中进行吸附实验时, 相对于N
2.4.1 单体与模板离子摩尔比的影响 在1.2节所述的制备体系中, 固定单体DAC的用量, 系列地改变模板SCN-离子的投加量, 测定所制备的印迹微球IIPMs对SCN-离子的选择性系数k(相对于N
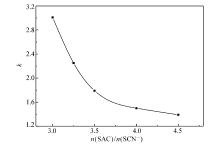 | 图5 微球IIPMs的选择性系数与DAC和SCN-离子摩尔比之间的关系曲线Fig.5 Selectivity coefficient of IIPMs as function of molar ratio of DAC to SCN- ion Molar percent of MBA:7% |
图中显示, 随着DAC和SCN-离子摩尔比的增大, 即随着模板SCN-离子的投加量的减少, 印迹微球IIPMs对SCN-离子的选择性系数在不断降低。 这是由于减少SCN-离子的投加量, 会减少微球内SCN-离子印迹空穴的数量, 导致印迹微球IIPMs对SCN-离子选择性系数的降低。 为得到选择性好的印迹微球, 应增大SCN-离子的投加量(即减小DAC和SCN-离子摩尔比 )。 但实验发现, 当DAC和SCN-离子摩尔比减小到小于3.0后, 反相悬浮体系不能成球, 故本研究选择3:1为适宜的DAC和SCN-离子的摩尔比。
2.4.2 单体与交联剂摩尔比的影响 在1.2节所述的制备体系中, 固定单体DAC的用量及SCN-离子的投加量, 系列地改变交联剂MBA的用量, 测定所制备的印迹微球IIPMs对SCN-离子的选择性系数 k(相对于N
图6显示, 随着交联剂MBA用量的增加, 微球IIPMs的选择性系数呈现先增大后减小的趋势, 当MBA的摩尔分数为7%时, 微球IIPMs具有最大的选择性系数。 交联剂MBA用量的多少与印迹空穴的尺寸大小密切相关, 因而与印迹空穴与模板离子的相互匹配性密切相关, 故会显著影响印迹微球的选择性系数。 本研究选择7%摩尔分数为交联剂MBA的适宜用量。
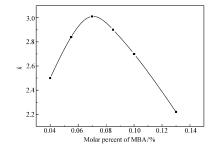 | 图6 微球IIPMs的选择性系数与MBA用量之间的关系曲线Fig.6 Selectivity coefficient of IIPMs as function of used amount of MBA n(DAC): n(SCN-)=3:1 |
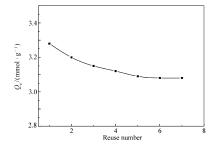
在进行等温结合实验后, 将印迹微球IIPMs内的模板SCN-离子清除干净, 真空干燥后, 再重复进行等温结合实验,图7给出饱和结合量与使用次数之间的关系曲线。
从图7可以看出, 在印迹微球IIPMs重复使用前4次过程中, 对SCN-离子的饱和结合量有较明显的下降(3.28→3.12 mmol/g), 第5次后, 饱和结合量稳定地维持在3.10 mmol/g(181 mg/g)的水平, 表明该阴离子印迹微球具有良好的重复使用性能。事实上, 本研究制备的印迹微球IIPMs对SCN-离子的吸附容量远高于其它吸附剂, 比如用表面活性剂改性的生物质对SCN-离子的吸附容量仅为8.6 mg/g[4];含有ZnCl2的活性碳对SCN-离子的吸附容量仅为16.2 mg/g[2];焙烧氢氧化镁铝对SCN-离子的吸附容量则为96.7 mg/g[3]。 其原因如上所述, 印迹微球IIPMs在水介质中高度溶胀, 不但对水介质中的阴离子具有高度的可接近性, 而且在SCN-离子印迹空穴的专一识别与结合性能的驱动下, 水介质中的SCN-离子会高效地被结合于印迹微球内部。
以阳离子单体DAC为功能单体, 环已烷为分散介质, 以Span-60为分散剂, 采用反相悬浮聚合法, 成功制备了粒径在200 μm左右的SCN-阴离子印迹微球IIPMs。 该离子印迹微球在水介质中高度溶胀, 球中的印迹空穴与SCN-阴离子在尺寸大小与空间构型高度匹配, 对SCN-阴离子显示出特异的识别选择性和优良的结合性能, 且循环使用性能良好, 可作为功能微球, 从水介质中高效地去除SCN-阴离子。 本文的研究结果在离子印迹微球的制备方面具有明显的科学意义, 在环境保护与治理领域具有潜在的应用价值。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|