以壬基酚、环氧氯丙烷、二甲胺和3-氯-2-羟基丙磺酸钠为原料, 在催化剂的作用下经醚化、叔胺化、季铵化, 合成了壬基酚甜菜碱两性表面活性剂(NSZ), 并确定了最佳的反应条件。 壬基酚氯醇醚的最佳合成条件:物料比 n(壬基酚): n(环氧氯丙烷)=1:4, 催化剂四丁基溴化铵用量为壬基酚用量的4%(摩尔比), 反应时间为4 h, 反应温度为95 ℃。 壬基酚叔胺的最佳合成条件:物料比为 n(壬基酚氯醇醚): n(二甲胺): n(氢氧化钠)=1:2.5:1.1, 反应时间为4 h, 反应温度为60 ℃。 NSZ的最佳合成条件:以异丙醇/水为溶剂且其体积比为2:1, 反应温度为85 ℃, 反应时间24 h, n(3-氯-2羟基丙磺酸钠): n(壬基酚叔胺)=1.2:1, 反应体系的pH值为8~9。 通过测定NSZ在高温高矿化度条件下的界面性能、乳化性能和热稳定性, 证明了NSZ具有良好的耐温抗盐性能。
Under the action of catalyst, the nonylphenol betaine amphoteric surfactant(NSZ) was synthesized from nonylphenol, epichlorohydrin, dimethylamine and 3-chloro-2-hydroxy propyl sulfonic acid sodium by etherification, amination, and quaternization, and the optimum reaction conditions were determined. The optimum synthesis conditions of nonylphenol chlorohydrin ether are:the material ratio n(nonylphenol): n(epichlorohydrin) was 1:4, the total amount of the catalyst tetrabutyl ammonium bromide was 4%(molar fraction) relative to nonylphenol, the reaction time was 4 h and the reaction temperature was 95 ℃. The optimum synthesis conditions of nonylphenol tertiary amine are:the material ratio n(nonylphenol chloro ether): n(dimethylamine): n(NaOH) was 1:2.5:1.1, the reaction time was 4 h and the reaction temperature was 60 ℃. The optimum synthesis conditions of NSZ are:the volume ratio of isopropanol to water was 2:1, the reaction temperature was 85 ℃, the reaction time was 24 h, the material ratio n(3- chloro-2-hydroxy-propanesulfonate): n(nonylphenol tertiary) was 1.2:1, the pH of the reaction system was 8~9. The interface properties, emulsifying properties and thermal stability of NSZ were measured under the condition of high temperature and high salinity, the results showed that NSZ had a good tolerance to temperature and salt.
两性表面活性剂虽然开发较晚, 但是在很多领域均具有重要的地位。 两性表面活性剂具有低毒性和对皮肤、眼睛的低刺激性[1], 极好的耐硬水性和耐高浓度电解质性[2], 良好的生物降解性, 对织物有优异的柔软平滑性、抗静电性、杀菌性和抑霉性。 因其良好的乳化性和分散性, 几乎可以和所有类型的表面活性剂配伍[3], 并可吸附在带负电荷或带正电荷的物质表面上而不生成憎水薄层, 因此有很好的润湿性和发泡性。 两性表面活性剂上述优点使其成为一类极具开发价值的绿色表面活性剂[4,5]。
目前, 国内针对驱油用的两性表面活性剂已有较多的研究。 高明等[6]合成了驱油用磺基甜菜碱两性表面活性剂SLB-13, 并将SLB-13与聚合物进行复配。 该复配形成的二元体系在非均质、低渗透人造岩心上取得了很好的驱油效果。 马涛等[7]将磷酸酯基的甜菜碱型表面活性剂与分子结构中具有乙烯基吡咯烷酮和2-甲基-2-丙烯酰胺基-丙磺酸基团的聚合物进行复配, 制成了无碱二元复配体系。 实验证明该体系具有很好的抗温耐盐性能。 崔正刚等[8]合成了一种双长链烷基甜菜碱两性表面活性剂。 在表面活性剂质量浓度为0.01%~0.5%, 聚丙烯酰胺浓度为0.1%, 不加碱、45 ℃时, 大庆原油/地层水界面张力降到了10-3 mN/m数量级。 刘春德[9]合成了一种双苯双醚型两性表面活性剂, 这种表面活性剂的三元复合驱油体系与大庆原油可以达到10-3~10-5 mN/m的超低界面张力, 可使原油采收率提高25%(OOIP)以上。 孙焕泉等[10]研发出了一种用于高温高矿化度油藏化学驱三次采油的粘弹性表面活性剂混合溶液, 该溶液主要由两种不同结构的两性离子表面活性剂组成。 该粘弹性溶液在高温、高矿化度条件下具有较高的粘度。 例如, 浓度为0.3%时, 表观粘度达到29 mPa·s。 赵濉等[11]合成了具有居贝特结构的烷基聚乙烯醚两性表面活性剂。 该表面活性剂的溶液具有优异的发泡性、泡沫稳定性、耐温耐盐性和良好的润湿性。 孙安顺等[12]合成了 N, N-二烷基丙酰胺脂肪烷基甜菜碱两性表面活性剂, 并将其与聚合物组成二元复合体系。 该体系可以与大庆原油达到10-3 mN/m数量级的超低界面张力。 姜颜波[13]合成了新型Guerbet两性离子表面活性剂 N-(3-支链十六烷基聚氧乙烯醚(3)-2-羟丙基)- N, N-二甲基羧酸甜菜碱(C16GPE3B)。 通过对C16GPE3B的表面张力和油水动态界面张力的测定, 证明C16GPE3B具有非常优异的驱油能力。
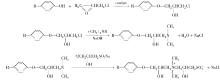
本文以壬基酚为主要原料设计并合成了壬基酚甜菜碱两性表面活性剂。 与传统的合成方法相比, 此方法具有反应时间短, 产率高, 合成步骤简单等优点。主要合成路线如Scheme 1所示。
壬基酚(枣庄市纳特生物材料有限公司), 工业品;环氧氯丙烷(上海美福化工有限责任公司), 分析纯;四丁基溴化铵(天津鹏坤化工有限公司), 分析纯;40%二甲胺水溶液(天津市大茂化学试剂厂), 化学纯;氢氧化钠(沈阳市新光试剂厂), 分析纯;异丙醇(天津市大茂化学试剂厂), 化学纯;3-氯-2-羟基丙磺酸钠(武汉百耐特化工有限公司), 化学纯。
DF-101S型集热式恒温加热磁力搅拌器(巩义市英峪京华仪器厂);TX500型旋滴型界面张力仪(美国盛维公司);Bruker-Tensor 27型傅里叶变换红外分光光度仪(上海杜美化工科技有限公司)。
1.2.1 壬基酚氯醇醚的合成 在1000 mL四口烧瓶中加入220 g(1 mol)壬基酚, 368 g(4 mol)环氧氯丙烷和少量的催化剂。 装上冷凝回流管, 搅拌升温到85 ℃反应1 h。 再把温度升高到95 ℃, 反应3 h, 减压蒸出过量的环氧氯丙烷。 通过硅胶层析柱分离得到深黄色粘稠液体壬基酚氯醇醚, 产率为95%。
1.2.2 壬基酚叔胺的合成 在1000 mL四口烧瓶中加入40%的二甲胺水溶液340 g。 装上冷凝回流管, 搅拌升温到40 ℃, 1.5 h内滴加壬基酚氯醇醚(溶在200 mL无水乙醇中)。 同时用30%NaOH溶液控制反应体系pH值为7~8。 将温度升高至60 ℃恒温4 h, 静止分层后将产物水洗至中性, 减压蒸馏除去溶剂得到壬基酚叔胺粗品。 称取0.3 g壬基酚叔胺粗品用标准的盐酸溶液滴定, 测得壬基酚叔胺的含量为80%。
1.2.3 N, N, N, N-二甲基-对(2-羟基)丙氧基烷基苯基-(2-羟基)丙基硫酸铵(壬基酚甜菜碱两性表面活性剂, NSZ)的合成 在2000 mL四口瓶中加入235 g(1.2 mol)3-氯-2-羟基丙磺酸和400 mL去离子水, 加热搅拌使其完全溶解。 将壬基酚叔胺粗品溶于800 mL异丙醇中, 通过恒压滴液漏斗缓慢滴加到四口烧瓶中, 然后温度升至85 ℃恒温24 h。 在反应过程中用恒压滴液漏斗滴加NaOH水溶液控制反应体系pH值为8~9。 用石油醚液相萃取, 旋转蒸发除去石油醚、异丙醇和水, 得黄色粘稠状产品, 用乙酸乙酯多次洗涤后, 抽滤, 干燥即得最终产品。 用磷钨酸法测得 N, N, N, N-二甲基-对(2-羟基)丙氧基烷基苯基-(2-羟基)丙基硫酸铵的有效物含量为75%。
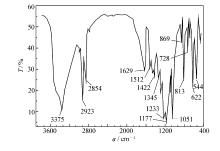
在图1中, 3375 cm-1处为O—H的伸缩振动吸收峰, 2923 cm-1处为饱和烷烃C—H的伸缩振动吸收峰, 2854 cm-1是—CH2的反对称伸缩振动吸收峰, 1629 cm-1处为C=C伸缩振动吸收峰, 而1512 cm-1中等强度吸收峰是苯环骨架的伸缩振动吸收峰, 1051 cm-1处是磺基—S
2.2.1 壬基酚与环氧氯丙烷的开环醚化反应 环氧氯丙烷的环氧基在四丁基溴化铵的催化作用下开环, 再与壬基酚的酚羟基发生醚化反应。生成中间体氯醇醚。 反应过程中壬基酚与环氧氯丙烷原料比、催化剂用量、反应温度和反应时间对开环醚化产率影响显著。
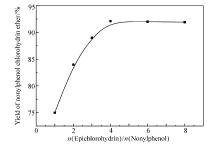
按照化学计量可知, 生成壬基酚氯醇醚所需要的 n(壬基酚): n(环氧氯丙烷)=1:1。 但为使壬基酚完全反应, 环氧氯丙烷必须要过量。 环氧氯丙烷既是反应物也起到溶剂的作用, 所以用量一定要适当。 反应时间4 h, 反应温度95 ℃, 催化剂用量为4%下的实验结果如图2所示, 可以看出 n(壬基酚): n(环氧氯丙烷)最佳比为1:4。
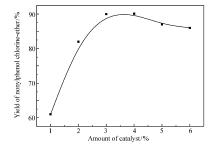
催化剂用量也是反应的关键, 用量太少会降低反应速率, 影响产率, 用量过大会产生环氧氯丙烷自身聚合等副反应。 n(壬基酚): n(环氧氯丙烷)=1:4, 反应时间4 h, 反应温度95 ℃下的实验结果如图3所示。 从图3可以看出, 四丁基溴化铵的用量<4%时, 壬基酚氯醇醚的产率随着催化剂用量的增加而增加。 当其用量超过4%时, 壬基酚氯醇醚的产率随着催化剂用量的增加而减小。所以催化剂用量应为壬基酚用量的4%。
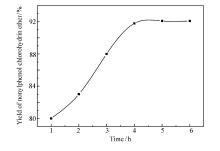
n(壬基酚): n(环氧氯丙烷)=1:4, 催化剂用量为4%, 反应温度95 ℃下反应时间对壬基酚氯醇醚产率的影响结果如图4所示, 随着反应时间的增加, 壬基酚氯醇醚的产率提高, 反应时间超过4 h后产率没有明显的提高, 故选择反应时间为4 h。
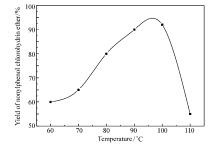
环氧基的开环反应为放热反应, 容易发生副反应。 四丁基溴化铵属于季铵盐, 热稳定性较差, 很容易发生降解反应, 因此需要控制合适的温度。 n(壬基酚): n(环氧氯丙烷)=1:4, 催化剂用量为4%, 反应时间为4 h下反应温度对壬基酚氯醇醚产率的影响结果如图5所示, 可知当温度低于95 ℃时, 产物产率随反应温度升高而增加。 但当温度高于95 ℃时产率急剧下降, 这是由于反应温度过高四丁基溴化铵已经降解, 起不到催化作用。 所以反应最佳条件应该为95 ℃。
2.2.2 壬基酚氯醇醚的叔胺化反应 氯醇醚与二甲胺反应一步生成叔胺, 反应过程中加入强碱NaOH可以提高反应速率, 得到高产率的叔胺。 实验考察了温度、时间、二甲胺用量和NaOH用量对叔胺产率的影响。
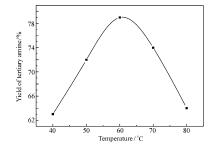
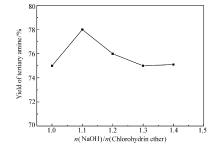
二甲胺水溶液沸点很低, 反应温度过高会导致二甲胺挥发损失较大和叔胺产率下降, 所以选择合适的温度是胺化反应的关键。 n(NaOH): n(氯醇醚)=1.1:1, 反应时间4 h, n(二甲胺): n(氯醇醚)=2.5:1下的实验结果如图6可知, 反应的最佳条件为60 ℃。
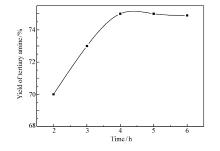
n(NaOH): n(氯醇醚)=1.1:1, 反应温度60 ℃, n(二甲胺): n(氯醇醚)=2.5:1下的实验结果如图7所示, 产物收率随着反应时间的加长而增长, 但是增长幅度越来越小, 反应时间超过4 h产率基本上没有变化。 故反应时间控制在4 h左右最为合适。
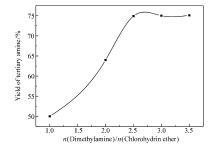
由于二甲胺易挥发且沸点低, 反应过程中损失大, 所以二甲胺要过量。 n(NaOH): n(氯醇醚)=1.1:1, 反应时间4 h, 反应温度60 ℃, 不同 n(二甲胺): n(氯醇醚)比下的实验结果如图8所示, 二甲胺与氯醇醚的摩尔比高于2.5时产率不再增加。 所以最佳物料比为 n(二甲胺): n(氯醇醚)=2.5:1。
NaOH用来中和胺化反应生成的HCl, 如果用量太少HCl中和不完全, 将会影响反应速率, 过多会导致氯醇醚的水解。 所以NaOH应该适量并且要用恒压滴液漏斗缓慢地滴加到反应体系中。 反应时间4 h, 反应温度60 ℃, n(二甲胺): n(氯醇醚)=2.5:1, 不同NaOH用量下的实验结果如图9所示, n(NaOH): n(氯醇醚)=1.1:1最为合适。
2.2.3 壬基酚叔胺与3-氯-2羟基丙磺酸钠的季铵化反应 反应体系的pH值对季铵化的产率影响显著。 当pH<8时, 壬基酚叔胺的反应活性较差, 不利于反应的进行。 当pH>9时, 产物的收率也开始降低。 这是由于季铵化反应与3-氯-2羟基丙磺酸钠的水解都是亲核取代反应, 3-氯-2-羟基丙磺酸钠水解生成2-羟基丙磺酸钠, 2-羟基丙磺酸钠不能发生季铵化反应, 因此体系的pH值会影响季铵化反应的收率。所以反应体系的pH值最好控制在8~9之间。
3-氯-2羟基丙磺酸钠与壬基酚叔胺的季铵化反应为亲核取代反应, 介电常数大的极性溶剂的溶剂化效应有利于亲核取代反应的发生。故溶剂对季铵化反应影响显著。 溶剂对反应的影响如表1所示。
| 表1 溶剂对季铵化反应产率的影响 Table 1 Influence of solvent on the quarternization reaction yield |
由表1可以看出, 以 V(异丙醇): V(水)=2:1的混合溶剂的季铵化产率最高。 这是由于3-氯-2羟基丙磺酸钠在异丙醇中的溶解度很小且水对叔胺的溶解也有限, 单一的溶剂不能使反应以均相状态进行, 影响反应产率, 所以在制备NSZ时, 采用了合适比例的异丙醇/水混合溶剂, 使季铵化反应得以均相状态进行, 可得到收率较高的NSZ。
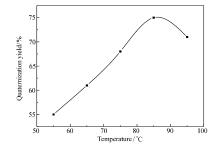
反应时间24 h, 反应体系的pH值控制在8~9, n(3-氯-2羟基丙磺酸钠): n(壬基酚叔胺)=1.2:1下的实验结果如图10所示, 随着反应温度的升高NSZ的收率增加, 但当反应温度超过85 ℃时产率开始下降。 这是因为超过85 ℃时, 3-氯-2-羟基丙磺酸钠的水解反应加剧, 因此产率下降。
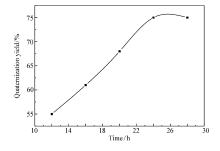
反应温度为85 ℃, 反应体系pH值为8~9, n(3-氯-2羟基丙磺酸钠): n(壬基酚叔胺)=1.2:1, 不同时间下的实验结果如图11所示, 季铵化产率随着反应时间的延长而增加, 反应时间超过24 h后收率无明显变化, 所以季铵化反应的最佳时间为24 h。
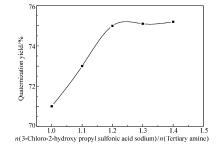
反应温度为85 ℃, 反应体系pH值为8~9, 反应时间为24 h, 不同3-氯-2-羟基丙磺酸钠与壬基酚叔胺的物料比下的实验结果如图12所示, 随着3-氯-2-羟基丙磺酸钠与壬基酚叔胺的物料比的增加, 季铵化产物的产率也随之增加, 当 n(3-氯-2-羟基丙磺酸钠): n(壬基酚叔胺)>1.2之后产率无明显的增加。
综上所述, 以 V(异丙醇): V(水)=2:1为溶剂, 反应温度为85 ℃, 反应时间24 h, n(3-氯-2-羟基丙磺酸钠): n(壬基酚叔胺)=1.2:1, 反应体系的pH值为8~9为季铵化的最佳合成条件。
2.3.1 界面性能 矿化度对NSZ界面张力的影响:以蒸馏水和矿化水(矿化度为32308、48462和64616 mg/L)为溶剂, NSZ的浓度为1 g/L(在胜利油田采收率室对表面活性剂含量的要求范围), 用旋转滴界面张力仪在85 ℃、转速为5000 r/min的条件下测定不同矿化度溶液与胜利二区原油的界面张力如图13所示。 随着矿化度的增加界面张力有微小的增加但是仍然能达到超低界面张力(10-4 mN/m)。说明NSZ具有良好的抗温耐盐性能。
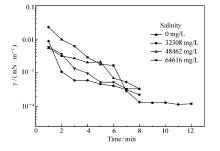 | 图13 不同矿化度对NSZ(1 g/L)油水界面张力曲线Fig.13 NSZ(1 g/L) oil-water interfacial tension curve under different degree of mineralization |
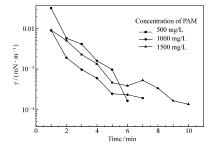 | 图14 不同聚合物浓度对NSZ(1 g/L)油水界面张力曲线Fig.14 NSZ(1 g/L)oil-water interfacial tension curve under different PAM concentrationThe degree of mineralization was 32308 mg/L |
聚丙烯酰胺浓度对NSZ界面张力的影响:以矿化水(矿化度为32308 mg/L)为溶剂, NSZ浓度为1 g/L, 在85 ℃、转速为5000 r/min的条件下测定不同聚丙烯酰胺浓度(分子量为1600万, 浓度为0.05%、0.1%、0.15%)的表面活性剂溶液与胜利二区原油的界面张力。 如图14所示, 不同聚丙烯酰胺浓度的表面活性剂溶液与胜利二区原油的界面张力仍然可以达到超低界面张力(10-4 mN/m), 说明NSZ与聚丙烯酰胺有很好的配伍性。
2.3.2 乳化性能 在100 mL具塞量筒中, 分别加入40 mL液蜡(液态石蜡为油相)和40 mL含有聚丙烯酰胺的NSZ水溶液, 按紧玻璃塞上下猛烈震动5次, 静置1 min, 如此重复震动-静置5次, 记录最后一次分出10 mL水的时间。如此重复3次, 最终取平均值, 由分出10 mL水的时间长短来判断乳化性能的好坏, 分水时间越长则乳化性能越好[14]。
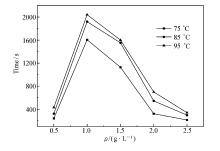
以矿化水(矿化度为32308 mg/L)为溶剂, 加入分子量为1600万的聚丙烯酰胺使其浓度为0.05%, 配制一系列不同浓度的NSZ水溶液。 测定75、85和95 ℃下溶液分出10 mL水的时间, 实验结果如图15所示。 NSZ在高温高矿化度条件下具有良好的乳化性能。 在NSZ的浓度为1 g/L时乳化性能最好, 并且随着温度升高乳化性能有所增强。
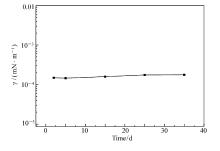
2.3.3 热稳定性 以矿化水(矿化度为32308 mg/L)为溶剂, 配制浓度为1 g/L的NSZ水溶液, 测定其在85 ℃下2、5、15、25和35 d时与原油的界面张力, 结果如图16所示。 实验结果表明, NSZ水溶液在85 ℃条件下长时间放置依然可以与胜利二区原油形成超低的界面张力。
壬基酚氯醇醚的最佳合成条件:物料比 n(壬基酚): n(环氧氯丙烷)=1:4, 催化剂四丁基溴化铵用量为壬基酚用量的4%(摩尔比), 反应时间为4 h, 反应温度为95 ℃。 壬基酚叔胺的最佳合成条件:物料比为 n(壬基酚氯醇醚): n(二甲胺): n(氢氧化钠)=1:2.5:1.1, 反应时间为4 h, 反应温度为60 ℃。 NSZ的最佳合成条件:以 V(异丙醇): V(水)2:1为溶剂, 反应温度为85 ℃, 反应时间24 h, n(3-氯-2羟基丙磺酸钠): n(壬基酚叔胺)=1.2:1, 反应体系的pH值为8~9。 聚丙烯酰胺与NSZ的溶液在85 ℃、矿化度达到64616 mg/L时界面张力仍然能达到超低界面张力(10-4 mN/m), 并且与聚丙烯酰胺有很好的配伍性能。 NSZ与聚丙烯酰胺二元体系在高温高矿化度条件下具有很好的乳化性能。NSZ水溶液在85 ℃下放置35 d与胜利二区原油的界面张力仍然可以达到超低界面张力(10-4 mN/m)。 由NSZ的界面性能、乳化性能和热稳定性能来看NSZ具有很好的耐温抗盐性能, 极有可能被用作高温高矿化度油藏原油采收率的驱油剂。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|