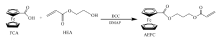
二茂铁类燃速催化剂在使用过程中存在的主要问题是在推进剂贮存过程中易产生迁移和挥发问题。 针对这些不足,对二茂铁衍生物进行改性,在二茂铁的茂环上引入极性基团以增大分子极性。 以二茂铁甲酸(FCA)和2-羟乙基丙烯酸酯(HEA)为反应物,以二环己基碳二亚胺(DCC)为脱水剂,以对二甲氨基吡啶(DMAP)为催化剂,在二氯甲烷(DCM)中合成二茂铁甲酸(2-丙烯酰氧乙基)酯(AEFC),优化各反应条件,确定最佳投料摩尔比为 n(FCA): n(HEA): n(DMAP): n(DCC)=20:28:20:24,反应温度为0 ℃,DCC溶液滴加时间为60~75 min,反应时间为15 h,搅拌速率为1000 r/min,在此条件下得到的AEFC的产率为75.1%,纯度为98%。
The main problems in the use and storage of ferrocene derivatives as burning rate catalysts are the migration and volatility of catalysts. A solution for the problems is to introduce polar groups on ferrocene. This paper reported the synthesis of 2-acryloyloxyethyl ferrocenecarboxylate(AEFC) from ferrocenecarboxylic acid(FCA) and 2-hydroxyethyl acrylate (HEA) with N, N'-dicyclohexylcarbodiimide(DCC) as the dehydration agent in the presence of 4-dimethylaminopyridine(DMAP). Under optimized reaction conditions, the synthesis was conducted with FCA, HEA, DMAP, and DCC in a molar ratio of 20:28:20:24 at 0 ℃ and addition of DCC solution in 60~75 min to give AEFC in 75.1% yield and 98% purity.
目前,复合推进剂中最常用的燃速催化剂为过渡金属氧化物及二茂铁类衍生物,其中二茂铁类衍生物由于具有很高的催化效率,而成为广泛使用的复合推进剂燃速催化剂[1,2,3]。 二茂铁及其衍生物是一类应用较广、提高推进剂燃速幅度较大的燃速催化剂,在航天工业中已经发挥了巨大的作用。 二茂铁类衍生物用作固体推进剂的燃速催化剂起源于50年代,但由于其本身是固体,目前所应用的二茂铁类燃速催化剂在使用过程中存在的主要问题是推进剂在贮存过程中的迁移和挥发问题[4,5,6,7]。 针对这些不足,国内外研究人员积极开展了对二茂铁衍生物的改性研究,改性的基本思路是在分子设计上考虑适当增长茂环上取代基的碳链或引入极性基团以增大分子极性,或者将含二茂铁的结构单元经过不同的反应接枝到聚合物分子链上,同时应保持催化剂分子中较高的含铁量[4,8]。
在茂环上引入—COOR、—OH、—COOH等极性基团以增大分子极性,或者引入双键,可以合成含有二茂铁基团的聚合物,但同时需保持较高的含铁量。 综合以上因素,本实验选择2-羟乙基丙烯酸酯(HEA)作为原料。 将HEA直接接在二茂铁茂环上有一定困难,利用HEA上的羟基,在茂环上先接上羧基生成二茂铁甲酸(FCA),然后再以FCA和HEA为原料进行酯化反应,得到一个含有二茂铁基、酯基、双键的单体二茂铁甲酸(2-丙烯酰氧乙基)酯(AEFC)。 AEFC本身可以用作燃速催化剂,其均聚物聚二茂铁甲酸(2-丙烯酰氧乙基)酯(PAEFC)也是良好的燃速催化剂,含有AEFC的接枝共聚物也可用作燃速催化剂。 酯化反应可选的方法较多,如酰氯酯化法、酸酐酯化法、 N, N'-二环己基碳二亚胺(DCC)脱水酯化法等,以及最近的酶催化交换法[9,10]。 其中,酰氯酯化法应用最多,但存在原料酰氯需要现制现用、副产物HCl去除麻烦、整体合成路线长等问题[11]。 相比之下,DCC脱水缩合法合成AEFC,反应条件温和,产率通常较高[12,13,14]。 4-二甲氨基吡啶(DMAP)可以同DCC一起构成DCC/DMAP催化体系用于酯化反应中,其中DMAP充当缩合促进剂或催化剂,本文研究该体系用于催化酯化反应合成AEFC的最佳合成工艺。
FCA、DMAP和DCC,分析纯,国药集团化学试剂有限公司;2-羟乙基丙烯酸酯(HEA),分析纯,上海笛柏化学品技术有限公司,纯化[15]后使用;二氯甲烷(DCM)用CaH2干燥过夜后蒸馏纯化[16],其它溶剂为分析纯试剂,直接使用。
AVANCF-400 MHz型超导傅里叶数字化核磁共振谱仪(德国Bruker公司),溶剂为氘代氯仿(CDCl3)。LC-20AD型高效液相色谱仪(日本岛津仪器有限公司),紫外检测器,检测波长为310 nm,C-18柱,流动相为甲醇和水的混合物,柱温为25 °C,进样量为10 μL,流速为1 mL/min。薄层色谱的固定相为硅胶GF254,展开剂为 V(正己烷): V(乙酸乙酯)=10:1混合溶剂,薄层板长度为8 cm。 比移值是指薄层色谱法中原点到斑点中心的距离与原点到溶剂前沿的距离的比值,又称 Rf值。
将4.60 g(20 mmol)的FCA、3.25 g(28 mmol)的HEA、2.44g(20 mmol)的DMAP、250 mL DCM加到500 mL的三口烧瓶中,并将其放入冰浴中搅拌并充N2气。 30 min后将4.95 g(24 mmol)DCC溶解于40 mL DCM中,在60 min内滴加到上述混合液中。 最后在室温下搅拌15 h。 将反应后的混合液经过滤除去生成的不溶物 N, N'-二环己基脲,浓缩滤液,用饱和的碳酸氢钠溶液洗涤去除剩余的FCA,然后用水洗去残留的碳酸氢钠,加无水硫酸镁进行干燥,将干燥后的溶液浓缩、最后用48~75 μm硅胶柱层析分离,淋洗剂为 V(正己烷): V(乙酸乙酯)=10:1混合溶剂,旋转蒸发去除溶剂后得4.93 g橙黄色固体,产率为75.1%(以FCA为基准计算),纯度为98%,熔点为53~55 ℃[5,16]。1H NMR(CDCl3,400 MHz), δ:4.20(s,5H,C5H5),4.40(s,2H,—C5H4),4.48(s,4H,—OCH2—CH2O—),4.80(s,2H,—C5H4),5.88(d, J=10.4 Hz,1H, 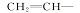
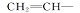
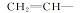
AEFC的合成反应式如Scheme 1所示,等化学计量的FCA和HEA在DCC/DMAP的作用下脱水生成AEFC,DCC在脱水成酯过程中形成 N, N'-二环己基脲。 DMAP[18]可以催化DCC作为脱水剂的酯化反应,在以下合成方法的优化过程中,先把DMAP的用量控制在1%~10%。
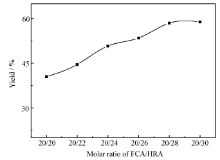
2.1.1 FCA和HEA的最佳配比 通过使一种反应物过量是提高产率常用的方法,结合本实验的实际情况,选择HEA过量。 实验过程按照1.2节所述方法,只改变HEA物质的量比,即 n(FCA): n(HEA): n(DMAP): n(DCC)=20: X:2:20,滴加时间为60 min,反应时间为24 h,反应温度为0 ℃,转速为1000 r/min。 实验结果如图1所示,随着HEA用量不断增加,产率(以FCA为基准计算)逐渐增加,当HEA的用量增加到FCA的1.4倍时产率基本达到最大,再增加HEA的用量产率无明显增加,由此可知,当 n(FCA): n(HEA)=20:28时为最佳比例。
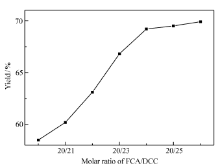 | 图2 FCA与DCC的摩尔比对产率的影响Fig.2 Influence of molar ratio of FCA and DCC on the yield of AEFC n(FCA): n(HEA): n(DMAP): n(DCC)=20:28:2: Y( Y:variable); others seeFig.1 |
2.1.2 FCA和DCC的最佳配比 实验过程按照1.2节所述,只改变DCC的用量,即 n(FCA): n(HEA): n(DMAP): n(DCC)=20:28:2: Y,DCC用量对产率影响如图2所示,当其它条件不变时,随着DCC用量的增加,产率(以FCA为基准计算)逐渐增大,当FCA与DCC的摩尔比20:24时产率达到69.2%,若再增大DCC的用量产率增加不明显。 因此,FCA和DCC的最佳配比为20:24。
2.1.3 DCC的最佳加料时间 如果将DCC一次性加入,反应较快不易控制而产生很多副产物导致产率极低,所以采用滴加的方法。 实验过程按照1.2节所述,只改变DCC溶液的滴加时间,其对产率影响如图3所示,随着滴加时间的增加,产率(以FCA为基准计算)逐渐增大,60 min时产率可达到69.2%,再延长滴加时间产率有一定增长,但增长不大。因为滴加DCC可以在很大程度上提高DCC的利用率,不会因大量DCC的聚集而引起大量副产物的出现。考虑到操作方便等因素,在60~75 min内滴加完即可。
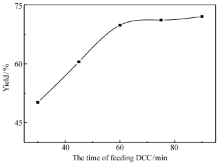 | 图3 DCC的滴加时间对产率的影响Fig.3 Influence of feeding time of DCC on the yield of AEFC n(FCA): n(HEA): n(DMAP): n(DCC)=20:28:2:24; others seeFig.1 |
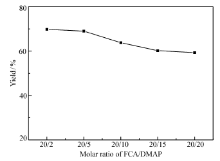 | 图4 FCA与DMAP的摩尔比对产率的影响Fig.4 Influence of different molar ratio of FCA and DMAP on the yield of AEFC n(FCA): n(HEA): n(DMAP): n(DCC)=20:28: Z:24( Z:vaariable); others seeFig.1 |
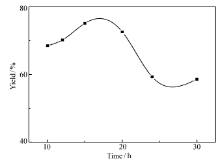 | 图5 反应时间对产率的影响Fig.5 Influence of different reaction time on the yield of AEFC n(FCA): n(HEA): n(DMAP): n(DCC)=20:28:20:24; others seeFig.1 |
2.1.4 FCA和DMAP的最佳配比 DMAP广泛用于催化醇和胺的酰胺化和酯化等反应。 实验过程按照1.2节所述,只改变DMAP的量,即 n(FCA): n(HEA): n(DMAP): n(DCC)=20:28: Z:24,实验结果如图4所示,随着DMAP用量的增加,产率(以FCA为基准计算)呈减小趋势,但是整体上变化不大。 当FCA与DMAP摩尔比从20:2增加到20:20时,产率仅减小13.9%。 DMAP的用量对反应时间有较大的影响,当FCA与DMAP摩尔为20:2时反应经24 h后产率仍不到50%,而当FCA与DMAP摩尔比为20:20时,只需15 h就可到达75.1%。 所以本文比较了不同反应时间对产率的影响,由于FCA与DMAP摩尔为20:20时效率较高,据此选择 n(FCA): n(HEA): n(DMAP): n(DCC)=20:28:20:24,其它条件不变,只改变反应时间,结果如图5所示,随着反应时间的增加,产率(以FCA为基准计算)逐渐增加,反应时间为15 h时产率可达到最高75.1%,但是随着反应时间的再增加产率则逐渐下降,原因是随着反应的进行,有一部分目标产物转化成了副产物。
2.1.5 反应温度的影响 从2.1.3节的讨论可知,DCC的反应活性较高,使得该反应较剧烈而不易控制,所以将DCC逐滴滴加。 为了使反应能够顺利的进行,提高产率,本文研究了反应温度对实验的影响,实验过程按照1.2节所述,只改变反应温度,这里的反应温度是指从开始滴加DCC到DCC滴加结束这段时间。 实验结果如图7所示,当温度低于0 ℃时产率(以FCA为基准计算)均较高,当温度高于0 ℃时产率下降很明显,因为温度较低时反应可以很好地控制,从而使得反应能够顺利地进行,而温度较高时,反应过于剧烈,同时有大量的副产物生成,且不利于向正反应方向进行。 但是-5和0 ℃产率相比差距并不大。
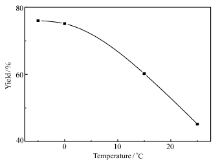 | 图6 反应温度对产率的影响Fig.6 Influence of reaction temperature on the yield of AEFC n(FCA): n(HEA): n(DMAP): n(DCC)=20:28:20:24; reaction time: 15 h; others seeFig.1 |
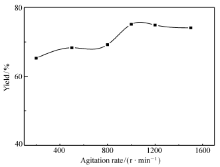 | 图7 搅拌速率对产率的影响Fig.7 Influence of agitation rate on the yield of AEFCReaction conditions seeFig.6 |
2.1.6 搅拌速率的影响 实验过程按照1.2节所述,只改变搅拌速率,搅拌速率对产率的影响如图7所示,随着搅拌速率的增加,产率(以FCA为基准计算)也逐渐增加,但是当转速超过1000 r/min时产率增加的不是很明显。 综上可得转速为1000 r/min为最佳转速。
以FCA和HEA为反应物,以DCC为脱水剂,以DMAP为催化剂,以DCM为溶剂,用DCC/DMAP法催化合成AEFC。 通过实验确定了最佳反应条件: n(FCA): n(HEA): n(DMAP): n(DCC)=20:28:20:24,反应温度为0 ℃,DCC溶液滴加时间为60~75 min,反应时间为15 h,搅拌速率为1000 r/min。在此反应条件下得到的AEFC的产率为75.1%,纯度为98%。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|