利用“一步法”合成并表征了4种碱性金属修饰的金属有机骨架材料MOF-5(记作M-MOF-5,M=Li,Na,K,Mg)。 并应用理想溶液吸附理论(IAST)对样品吸附选择性进行计算比较。 结果表明,碱性金属掺入可以降低MOF-5材料骨架结构的“互穿”程度,同时,在常温常压下,M-MOF-5对CO2/CH4的吸附选择性相对MOF-5(选择性为3.79)有着显著提高,尤其是Li-MOF-5(选择性为7.39)。 此外,Li-MOF-5的CO2捕获能力相对MOF-5也有提高。
Alkali-metal modified metal organic frameworks MOF-5(denoted by M-MOF-5, M=Li, Na, K, Mg) were prepared by ‘one-step’ synthesis. The theoretical calculation(IAST, ideal adsorbed solution theory) was performed to compare the adsorption selectivity of materials. It is found that alkali-metal incorporated MOF-5 can reduce the interpenetration level of MOF-5 framework. The experiment results also show that M-MOF-5 can significantly improve the CO2/CH4 adsorption selectivity compared to MOF-5(3.79), especially Li-MOF-5(7.39) at ambient conditions. Furthermore, the CO2 capacity of Li-MOF-5 is also enhanced.
能源需求的快速增长和环境友好型新能源的开发,促进了可再生能源(如沼气)的发展。 甲烷(CH4)是沼气的主要成分,可以作为车辆的绿色能源。 然而,在使用沼气作为能源时,必须先纯化沼气,分离除去其中的主要杂质二氧化碳气体(CO2)。 目前沼气的脱CO2处理,主要是用胺溶液通过化学吸收的方法实现的[1]。 而该方法能源消耗过高,同时胺溶液会腐蚀钢管道和阀门,因此亟需寻找其它替代方法以降低成本。 近来大量分子筛和碳基材料作为固体吸附剂被用以分离CO2/CH4混合气体。 而金属有机骨架材料(MOFs)作为一类新型多孔材料,具有极高的比表面积,在气体分离领域具有潜在的应用前景[2,3]。
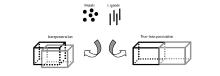
MOF-5由于具有高的热稳定性和气体吸附性而受到广泛关注[4,5]。 研究表明,MOF-5普遍存在框架的“相互穿插”现象(或称“互穿”现象)[6](方案1)。 普遍认为其形成原因是在MOF-5的初级骨架形成后,由于部分的Zn离子进入初级骨架的孔穴中,并有机会在三维空间与配体配位,形成“互穿”。 “互穿”结构会降低空隙空间的可利用性,往往导致材料比表面积下降,但是同时,“互穿”产生了防
止骨架塌陷的排斥力,从而显著提高框架的稳定性。 碱性阳离子掺杂的MOFs材料在环境条件储氢方面的应用引起了研究者的极大兴趣[7]。 为了提高MOFs材料的吸附性能,向MOFs中掺入轻金属(如锂等)是一种行之有效的方法[8]。
本文制备了碱性金属锂、钠、钾、镁掺杂的MOF-5材料(记作M-MOF-5,M=Li,Na,K,Mg),研究了其对CO2/CH4混合气体的吸附选择性,探究“一步法”合成中碱金属对MOF-5材料“互穿”结构的影响。
D8 Advance型X射线衍射仪(德国Bruker公司),Cu靶,管流40 mA,管压40 kV;VERTEX型傅里叶红外光谱仪(德国Bruker公司);Optima4300DV型电感耦合等离子发射光谱仪(美国PerkinElmer公司);STA449F3型同步热分析仪(德国Netzsch公司);ASAP2020型比表面积及孔隙分析仪(美国Micromeritics公司)。 每次取60100 mg样品进行气体吸附等温线测量。 用于测试的CO2、CH4和N2气的纯度大于99.999%。 测试前,样品在523 K、真空条件下脱气6 h(初始活化)。 微孔比表面积选取相对压强 p/p0在0.050.5之间,由Brunauer-Emmett-Teller(BET)和Langmuir法计算得出。
六水合硝酸锌(Zn(NO3)2·6H2O,分析纯,国药集团化学试剂有限公司);对苯二甲酸(H2BDC,99%,上海晶纯生化科技股份有限公司(Aladdin));硝酸锂(LiNO3,99+%,上海晶纯生化科技股份有限公司(Aladdin));硝酸钠(NaNO3,99%,国药集团化学试剂有限公司);硝酸钾(KNO3,99%,国药集团化学试剂有限公司);硝酸镁(Mg(NO3)2·6H2O,99%,上海晶纯生化科技股份有限公司(Aladdin)); N, N'-二甲基甲酰胺(DMF,99.5%,上海晶纯生化科技股份有限公司(Aladdin))。
采用溶剂热法合成样品MOF-5和M-MOF-5。 将0.440 g Zn(NO3)2·6H2O(1.5 mmol),0.184 g H2BDC(2.67 mmol)溶于DMF和少量水(0.18 mL)组成的混合溶液中。 待反应物混合均匀后,转移到特氟龙反应釜中,在393 K下反应48 h。 得到的晶体用DMF洗涤并在室温下真空干燥6 h,随后升温至523K继续干燥6 h。 M-MOF-5(M=Li,Na,K,Mg)的合成方法与之类似,只需在混合溶液时加入0.045 mmol对应的金属硝酸盐。 由于MOF-5材料极易水解使得骨架坍塌,因此所得产品存储在干燥的环境中。
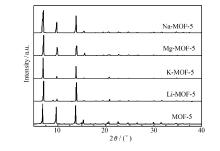
MOF-5和M-MOF-5系列材料的XRD图谱中尖锐的衍射峰位置完全匹配(图2所示),表明碱性离子的掺入没有引起MOF-5材料晶相的变化。 同时,从图2可以看出,各材料对应衍射峰的相对峰强有所变化。 事实上,若将9.7°和6.8°衍射峰强度比值记作 R1,13.8°和6.8°衍射峰强度比值记作 R2(见表1),Hafizovic等[6]的研究表明MOF-5中 R1值与结构孔穴中物质有关(含锌化合物,如Zn2+与BDC的配合物,但未形成3D骨架结构或溶剂分子);Chen等[9]研究发现MOF-5中较高的 R1值和 R2值表明较高的“互穿”度。 由表1可知,M-MOF-5的 R1和 R2值分别低于MOF-5的 R1和 R2值。 其中, R1值从MOF-5(0.84)依次下降至Na-MOF-5(0.49)>Mg-MOF-5(0.42)>Li-MOF-5(0.13)>K-MOF-5(0.12),同时 R2值也较MOF-5有所下降。 这些值的降低表明了M-MOF-5骨架结构“互穿”度的降低。 而这可以解释为,在MOF-5晶体生长过程中碱性离子能进入到初级骨架的孔穴中,换言之,降低了锌离子进入初级骨架的几率,防止了“互穿”结构形成,因为即使碱性离子在孔穴中也不能在三维结构上配位生长。 总之,结果表明碱性离子的掺入可以减少MOF-5晶体生长过程中孔穴内含锌化合物的残留,一定程度上抑制“互穿”结构的形成,提高了其比表面积。 此外,电感耦合等离子发射光谱(ICP)结果显示,各样品中锌离子质量分数约为24%,Li、Na、K和Mg质量分数依次分别为0.013%、0.065%、0.091%和0.252%,证明样品中确有碱性金属存在。
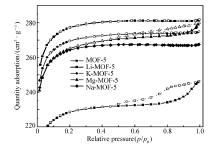
采用氮气等温吸附脱附曲线研究了MOFs材料的孔结构。 如图3所示,相对MOF-5而言,M-MOF-5氮气吸附量明显增加,而且吸附量Li-MOF-5>K-MOF-5>Mg-MOF-5>Na-MOF-5。 此外,MOF-5在相对压强0.8~0.99区间范围内出现的吸附滞后环,表明结构中含有介孔,而Li-MOF-5、Na-MOF-5、K-MOF-5的等温吸附曲线中滞后环消失。 由其比表面积对比(表1)可知,碱性金属的掺入使骨架移位,从而产生更高的孔隙率和更大的比表面积。
MOF-5和M-MOF-5在25°C、压强0.1 MPa的条件下,对CO2和CH4单组分气体吸附数值见表1。 其中,Li-MOF-5具有最高的CO2吸附量。
随后我们研究了材料对CO2/CH4混合气体的吸附选择性。 利用理想吸附溶液理论(Ideal Adsorbed Solution Theory,简称IAST)来计算吸附选择性,即采用材料的单组分气体吸附等温线来模拟计算双组份混合气体的吸附[10]。 其定义式为:
SA/B=
式中, SA/B表示吸附选择性系数, XA和 XB表示组分A和B在吸附相中的摩尔分数, YA和 YB表示组分A和B在主体相中的摩尔分数。 如表1所示,温度273 K、压强0.1 MPa,M-MOF-5比MOF-5表现出更高的选择性,其吸附选择性顺序为MOF-5<K-MOF-5<Na-MOF-5<Li-MOF-5<Mg-MOF-5。 据此我们可以推断,碱性金属掺入能够提高MOF-5对CO2/CH4混合气体的选择性。 这与已报道的模拟结果相符[11]。综合来说,在M-MOF-5中Li-MOF-5具有最高CO2吸附性能和极高CO2/CH4吸附选择性。 因此,在分离CO2/CH4中是最佳选择。
| 表1 MOF-5和M-MOF-5的表面性质,吸附选择性和骨架“互穿”程度 Table 1 Surface property, adsorption selectivity and framework interpenetrated level of MOF-5 and M-MOF-5 |
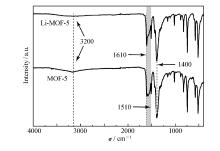
图4为Li-MOF-5和MOF-5的红外光谱图。 3200 cm-1处的吸收峰是羧基上—OH基团的伸缩振动吸收峰。 而Li-MOF-5中该处的吸收峰消失,这是由于锂与羧基的—OH反应使得羟基峰消失;1610和1400 cm-1是单齿配位羧基反对称伸缩振动和对称伸缩振动峰,1510 cm-1是双齿螯合羧基伸缩振动峰,观察到1510~1610 cm-1区间内峰形存在差异,也可以反映出锂离子与羧基配位后对其伸缩振动的影响,傅里叶红外光谱表明,锂离子存在于Li-MOF-5的结构之中并与羧基配位,增强了该吸附位点的电势,提高了该位点与客体气体分子的相互作用从而提高吸附量。
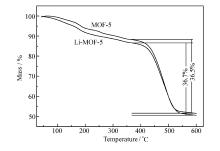
MOF-5和Li-MOF-5的热重分析见图5。 在20~300 ℃区间溶剂和水引起的热损失不同(质量分数约10%~14%)。 365~600 ℃之间的热损失来自于配体BDC的分解,且热损失量几乎相同(质量分数约36.5%)。
实验结果和IAST的计算表明,“一步法”碱性金属(Li,Na,K,Mg)修饰能影响MOF-5的骨架结构,即降低骨架结构的“互穿”程度。 较低“互穿”程度能提高MOF-5的比表面积。其中,Li-MOF-5具有最高比表面积1097 cm3/g,其后依次为K-MOF-5、Na-MOF-5、Mg-MOF-5,均高于MOF-5材料的738 cm3/g。 同时,对于常温常压下CO2(40%)/CH4(60%)吸附选择性,Mg-MOF-5(9.20)>Li-MOF-5(7.39)>Na-MOF-5(6.62)>K-MOF-5(6.56)>MOF-5(3.79)。 而且,Li-MOF-5的CO2捕获能力高于其它M-MOF-5。 综上,Li-MOF-5是这4种碱性金属中最佳选择(最高比表面积,最高CO2捕获量,极高CO2/CH4吸附选择性)。可以推测,这种性能的提升归因于在合成过程中,锂离子的适量引入能够减少其孔穴中的含锌化合物,降低其结构的“互穿”度,从而得到较高比表面积的骨架材料。 与此同时,锂离子的引入能促进MOF-5骨架表面和客体分子间的相互作用(气-固表面相互作用),提高CO2/CH4混合气体的吸附选择性。 吸附选择性的提高对其分离气体(尤其是从沼气中分离出高纯甲烷)有着重要意义。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|