采用静态失重、动电位极化、交流阻抗等技术方法研究了1-苯胺甲基苯并咪唑(PAB)对盐酸介质中N80钢的缓蚀性能,并讨论了PAB在N80钢表面的吸附行为。 结果表明,缓蚀率随着PAB浓度增大而升高,随着温度升高而下降。 极化曲线测试表明PAB是一种混合控制型缓蚀剂。 PAB在N80钢表面的吸附是一个自发、放热、熵增的过程,其行为符合Langmuir吸附等温式。 同时采用量子化学方法对PAB的缓蚀机理做了进一步分析。
The inhibition effect and adsorption behavior of 1-phenylaminomethylbenzimidazole(PAB) for N80 steel in HCl solution were investigated by mass-loss test, potentiodynamic polarization and electrochemical impedance spectroscopy(EIS). The inhibition efficiency increased with higher concentration of PAB and decreased with elevated temperature. Polarization curve reveals that PAB is a mix-type inhibitor. The adsorption between PAB and N80 steel surface is a spontaneous, exothermic and entropy increasing process fitting Langmuir isotherm. The relationship between the molecular structure of PAB and the inhibition efficiency was investigated using quantum chemical calculations.
酸化是油田常用的一项提高油井采收率的措施,但酸液的注入将对地面管路及井筒管壁产生严重的腐蚀,而且溶蚀的Fe3+进入地层会对地层产生永久损害[1]。 研究表明,在酸液中添加缓蚀剂是一种效果好、成本低的防护措施。 在众多的缓蚀剂中,曼尼希碱类缓蚀剂因有较好的缓蚀性能而广受关注。 目前研究较多的主要是C—H酸曼尼希碱的缓蚀性能[2,3,4],而对N—H酸曼尼希碱的缓蚀性能研究得较少。
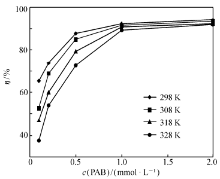 | Scheme 1 Molecular structure of 1-phenylaminomethylbenzimidazole(PAB)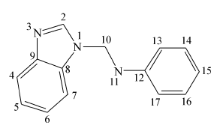 苯并咪唑是一种含有2个氮原子的苯并杂环化合物,其衍生物主要包括咪唑环N原子上的1位取代产物和C原子上的2位取代产物[5]。 近来,有研究表明,以烷基、巯基、氨基、吡啶基和苯胺基等取代的2位苯并咪唑衍生物对金属有一定的缓蚀性能[6,7,8],但对1位取代的苯并咪唑衍生物的缓蚀作用的研究尚不多见。 本文参照文献[9-10]合成了一种1位取代的苯并咪唑- N曼尼希碱:1-苯胺甲基苯并咪唑(PAB,见Scheme 1),采用失重法、动电位极化法和交流阻抗法评价了PAB对盐酸介质中N80钢的缓蚀作用,探讨了PAB在N80钢表面的吸附行为,最后通过量子化学计算分析了它的缓蚀作用机理。 苯并咪唑是一种含有2个氮原子的苯并杂环化合物,其衍生物主要包括咪唑环N原子上的1位取代产物和C原子上的2位取代产物[5]。 近来,有研究表明,以烷基、巯基、氨基、吡啶基和苯胺基等取代的2位苯并咪唑衍生物对金属有一定的缓蚀性能[6,7,8],但对1位取代的苯并咪唑衍生物的缓蚀作用的研究尚不多见。 本文参照文献[9-10]合成了一种1位取代的苯并咪唑- N曼尼希碱:1-苯胺甲基苯并咪唑(PAB,见Scheme 1),采用失重法、动电位极化法和交流阻抗法评价了PAB对盐酸介质中N80钢的缓蚀作用,探讨了PAB在N80钢表面的吸附行为,最后通过量子化学计算分析了它的缓蚀作用机理。1 实验部分 1.1 试剂和仪器盐酸(AR,武汉市中天化工有限公司),无水乙醇(AR,天津市北联精细化学有限公司),丙酮(AR,武汉市中天化工有限公司),N80钢片(江苏江都建华仪器厂),砂纸(400目、800、1200目,湖北玉立砂带有限公司),AB胶。CHI660E型电化学工作站(上海辰华仪器有限公司),恒温水浴锅(江苏金坛国盛仪表厂)。 1.2 研究方法1.2.1 失重法 按SY 5405-1996《酸化用缓蚀剂性能试验方法及评价指标》中的要求,配制15%的盐酸,将N80钢片依次用400、800、1200目砂纸打磨,再依次用乙醇、丙酮洗净,干燥、称重。 将N80钢片垂直浸入含有不同浓度PAB的酸液中,以未添加任何缓蚀剂的酸液作为空白,恒温4 h后取出,擦净,再经纯水、乙醇清洗,干燥至恒重,然后按式(1)和式(2)分别计算腐蚀速率和缓蚀率。v= 2 结果与讨论 2.1 失重试验失重法测试结果见图1。 从图1可见,在同一温度下,PAB在15%盐酸中对N80钢的缓蚀率随着缓蚀剂浓度的升高而增大,但是当PAB浓度达到1 mmol/L时,再提高PAB的浓度,缓蚀率的增幅明显放缓。 如在298 K时,当缓蚀剂浓度为0.1 mmol/L时,缓蚀率为65.4%,当缓蚀剂浓度增加到1和2 mmol/L时,缓蚀率分别为92.2%和93.9%。 因此,可以认为当PAB浓度为1 mmol/L时,N80钢表面的PAB已接近饱和吸附。 而当PAB的浓度一定时,温度的上升将会削弱其缓蚀作用,特别是当PAB的浓较低时,这种削弱作用更为明显。 如PAB浓度为0.1 mmol/L时,308和328 K下的缓蚀率分别为65.4%和37.3%,二者相差28个百分点;而当PAB浓度为2 mmol/L时,缓蚀率分别为93.9%和87.7%,其差值缩小至6个百分点。 由此可见,增大缓蚀剂的浓度可减小温度上升对缓蚀率的影响。 |
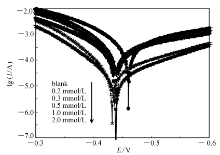
298 K时,N80钢在含不同浓度PAB的15%盐酸溶液中的极化曲线见图2,拟合得到的相关参数列于表1。 从表1可以看出,增大PAB的浓度,腐蚀电流下降,缓蚀剂的阴极和阳极作用系数( fc和 fa)均小于1且逐渐变小,表明PAB对腐蚀过程中的电极反应产生了抑制作用,将会减弱腐蚀反应的速率。 而且随着PAB浓度的增大,这种抑制作用逐渐变强。但是当PAB浓度达到1 mmol/L时,再提高浓度,腐蚀电流的变化不大,表明当浓度为1 mmol/L时,PAB已较为充分地抑制了N80钢片的电极反应,这与失重法中缓蚀率随PAB浓度的变化趋势(图1)是吻合的。 在所研究的浓度范围内,阳极作用系数( fa)均小于阴极作用系数( fc),表明PAB对阳极反应的抑制作用大于阴极反应,而且腐蚀电位有正移的倾向,均表明PAB是一种以抑制阳极为主的混合控制型缓蚀剂。 从表1还可看出,阴极塔菲尔斜率 bc和阳极塔菲尔斜率 ba均有所降低,表明PAB的加入在一定程度上改变了阴极和阳极反应过程。 有研究表明,苯并咪唑及其衍生物在酸性介质中以质子化形式存在,其与金属表面之间存在供质子吸附[13]。 因此,在碳钢表面质子化的PAB吸附膜可能对酸液中带正电的氢离子产生斥力,使之难以接近碳钢表面,从而影响了阴极的析氢反应的发生。 这可能是阴极塔菲尔斜率变小的原因。 而阳极塔菲尔斜率下降的原因可能是PAB中的N原子可与亚铁离子形成配合物,导致了阳极溶解过程的改变[14]。
| 表1 不同浓度PAB下的极化曲线参数(298 K) Table 1 Polarization parameters in 15%HCl with various concentrations of PAB(298 K) |
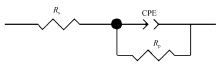
298 K时,N80钢在不同浓度PAB的15%盐酸溶液中的阻抗谱见图3。 从图3 A可见,在不同浓度PAB的酸液中,Nyquist曲线均呈现出单一的容抗弧,而且随着PAB浓度的升高,容抗弧的直径增大,表明腐蚀作用的阻力在增加。 从图3 B可见,不同浓度PAB时的相位角未见明显双峰出现,表明电极过程仍可视为单个时间常数的瞬态过程[15],因此可用图4所示的电路图来对阻抗谱进行拟合,其中, Rs为溶液电阻,CPE为常相位角元件,由CPE-T(相当于双电层电容)和CPE-P(弥散指数)组成, Rp为极化电阻,拟合结果见表2。 从表2可见,随着酸液中PAB浓度的升高,CPE-T减小,表明PAB取代了水分子吸附于N80钢表面。 这是因为水分子介电常数比PAB大,导致PAB吸附于N80钢表面的界面电容要明显小于水分子吸附于N80钢表面的电容值[16]。 Rp随PAB浓度的上升而增大,表明随着PAB的增大,腐蚀过程中电极反应的阻力也相应增大,导致缓蚀作用增强。 但当PAB浓度达到1 mmol/L时,再提高其浓度, Rp的增幅较小,表明当PAB浓度为1 mmol/L时,已能较充分地阻滞电极反应的发生,从而将会起到较好的缓蚀效果,这与失重法(图1)和极化曲线(表1)的相关结果是相符的。另外,从表1和表2还可看出,由极化曲线法和交流阻抗法所得的缓蚀率( ηp和 ηE)较为一致,但均小于失重法(图1)所得到的缓蚀率( ηw),原因可能是电化学方法得到的是瞬时结果,而失重法得到的是较长时间内的平均结果。
| 表2 15%盐酸中不同浓度PAB条件下的交流阻抗拟合参数 Table 2 Impedance parameters in 15%HCl with various concentrations of PAB |
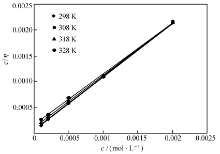
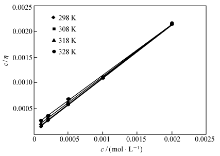
由极化曲线结果(表1,图2)知,加入PAB后腐蚀电位未发生明显变化,表明缓蚀剂在电极表面为几何覆盖效应[17]。 这种类型的缓蚀剂在金属电极表面上的吸附覆盖率与溶液中缓蚀剂的浓度之间的关系可用吸附等温式来表示。 在几何覆盖效应情况下,吸附覆盖率正比于缓蚀率。 假设PAB在N80钢表面的吸附服从Langmuir吸附等温式[18],则应有:
c inh/η=c inh+1/K ads(7)
式中, cinh为缓蚀剂浓度, η为缓蚀率, Kads为平衡吸附常数。 以 cinh/ η对 cinh作图,得到了图5所示的吸附等温线,线性拟合的复相关系数均大于0.99,表明用Langmuir吸附等温式来关联PAB的浓度与缓蚀率是合理的。 根据所拟合直线方程的截距可求出吸附平衡常数( Kads)。 又可据式(8)可求出吸附能(Δ
Δ
lnK ads=- Δ
式中,R =8 .314 J/( mol· K),T为试验热力学温度( K),K ads为吸附平衡常数,55 .5为1升水的物质的量( mol)。 ln K ads与1 /T的关系如图6所示。 最后据式(8)可计算出吸附熵 Δ
Δ
由式(7) ~(10)计算所得到的K adsΔ
| 表3 PAB在N80钢表面的吸附热力学参数 Table 3 Thermodynamic parameters of adsorption of PAB on N80 steel surface at different temperatures |
从表3可见,随着温度的升高, Kads呈下降趋势,表明温度的升高不利于PAB的吸附。 Δ
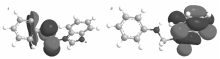
通过量子化学计算,PAB分子的HOMO能量为-9.998 eV,LUMO能量为-1.249 eV,图7为计算所得的PAB的HOMO和LUMO表面。 从图7可见,PAB分子HOMO主要分布在苯胺基团上,说明这一区域的电子云密度最大,有较强的供电子能力,可与Fe的3 d空轨道形成配位键;LUMO主要分布于苯并咪唑环上,说明这一区域可接受Fe成键轨道的电子形成反馈键。 而且PAB分子HOMO与LUMO的这种非重叠分布还有利于分子以平行的方式吸附于Fe表面,从而增大对Fe表面的覆盖面积,提高缓蚀性能。
为了进一步确定分子的反应活性位点,表4给出了PAB分子的主要原子的Fukui指数值。 该值既可测定分子的反应活性,还可以确定活性位点的亲电和亲核性。 fi(r)-和 fi(r)+分别为亲电攻击指数和亲核攻击指数,分别表示分子中原子i给/得电子能力的强弱,其值越大,给/得电子能力越强[22]。 从表4可见,PAB分子中苯胺基团上的N11原子的 fi(r)-最大,表明这个原子具有最强的供电子能力,由于共轭作用,苯环上的C13、C15和C17也有较大 fi(r)-值,因此,这些原子形成了一个多中心的供电子区域,可向Fe原子提供电子形成配位键;咪唑环上C2原子的 fi(r)+最大,其余依次为C5、C8、N1和C7,这些原子形成了一个多中心的得电子区域,可接受Fe表面的电子形成反馈键。
| 表4 PAB分子的Fukui指数 Table 4 Fukui index values for PAB molecule |