将金鸡纳生物碱衍生物用于催化蒽酮和 β-硝基芳基乙烯的不对称Michael加成反应。 考察了溶剂、温度及催化剂用量对反应催化性能的影响。 结果表明,最佳条件为5%(摩尔分数)催化剂1b、甲苯为溶剂、0 ℃反应,得到了91%~99%的化学产率和最高达95% ee的对映体选择性。
Cinchona alkaloid derivatives as organocatalysts were applied in asymmetric Michael addition reaction of anthrone with various trans-β-nitroolefins. Solvent, temperature and catalyst loading were screened. The optimized conditions are using toluene as the solvent with a 5%(molar fraction) loading of catalyst 1b at room temperature. The products are obtained in 91%~99% yield with up to 95% ee.
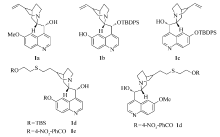
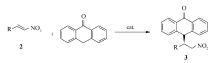
Michael加成反应在有机合成中是一种高效、原子经济性的形成C—C键的重要方法[1]。 近年来,许多手性有机小分子催化剂被应用于各类底物的不对称Michael加成反应[2,3,4,5,6,7,8]。 硝基烯烃为受体的Michael加成反应是制备硝基烷烃,并进一步合成胺、羰基化合物、氰等化合物的重要方法。 醛、酮、丙二酸酯、丙二氰等化合物是Michael加成反应中常见的亲核试剂[9,10,11]。 而蒽酮化合物作为亲核试剂用于不对称Michael加成反应的文献报道则较少[12,13,14,15]。 2007年,Shi等[14]首次报道了有机催化的蒽酮与硝基烯烃的不对称Michael 加成反应,得到了80%~99% ee的对映体选择性。 2010年He等[15]报道了伯胺硫脲类催化蒽酮与 β-硝基苯乙烯的不对称Michael加成反应,得到了65%~86%的对映体选择性。 我们设计合成了金鸡纳生物碱及其衍生物1a~1f(图1)作为有机催化剂,用于蒽酮与 β-硝基烯烃的不对称Michael 加成反应。
Bruker Avance-500型核磁共振谱仪(德国Bruker公司),均以CDCl3为溶剂, TMS为基准物质;LC-20A型高效液相色谱仪(日本岛津公司),Daicel Chiralpak AD-H、Chiralcel AS-H及Chiralcel OD-H型手性色谱柱(日本大赛璐公司),奎宁为Acros试剂;奎尼丁为Fluka试剂,其他试剂均为市售分析纯产品。 β-硝基烯烃根据文献[16]方法合成,催化剂1b~1f根据文献[17]方法合成。
于5 mL圆底烧瓶中依次加入硝基芳基苯乙烯(0.2 mmol),催化剂1b(0.01 mmol),蒽酮(46.6 mg,0.24 mmol), 甲苯(3.0 mL),室温搅拌反应12~18 h, TLC监测,反应结束后,经硅胶柱层析分离, V(正己烷)∶ V(乙酸乙酯)(体积比9:1)洗脱,得到产品3a~3l。
10-(2-硝基-1-苯基乙基)-10 H-蒽-9-酮(3a):1H NMR(500 MHz,CDCl3), δ: 8.07(d, J=8.0 Hz,1H),7.98(d, J=8.0 Hz,1H),7.67~7.59(m,2H),7.53~7.46(m,2H),7.45~7.40(m,2H),7.17~7.13(m,1H),6.95(t, J=7.5 Hz,2H),6.05(d, J=8.0 Hz,2H),4.89(dd, J=9.0,13.0 Hz,1H),4.60(dd, J=7.0,13.0 Hz,1H),4.55(d, J=3.5 Hz,1H),4.08~4.04(m,1H);HPLC(Daicel Chiralpak AD-H, V(hex)∶ V( iPrOH)=95∶5,0.5 mL/min,254 nm), tR:55.2 min(minor),58.5 min(major)。
10-[1-(2-氟苯基)-2-硝基乙基]-10 H-蒽-9-酮(3b):1H NMR(500 MHz,CDCl3), δ:8.13(d, J=7.5 Hz,1H),8.07(d, J=7.5 Hz,1H),7.66~7.61(m,1H),7.57~7.49(m,3H),7.48~7.44(m,1H),7.26~7.18(m,2H),6.88~6.78(m,2H),6.07(t, J=7.5 Hz,1H),4.74(dd, J=8.0,13.5 Hz,1H),4.60(d, J=9.0,1H),4.54(dd, J=8.0,13.5 Hz,1H),4.39~4.35(m,1H);HPLC(Daicel Chiralpak AD-H, V(hex)∶ V( iPrOH)=95∶5,0.5 mL/min,254 nm), tR:49.1 min(minor),68.6 min(major)。
10-[1-(2-氯苯基)-2-硝基乙基]-10 H-蒽-9-酮(3c):1H NMR(500 MHz,CDCl3), δ:8.18(d, J=7.5 Hz,1H),8.15(d, J=7.5 Hz,1H),7.70~7.64(m,2H),7.54~7.51(m,1H),7.47~7.43(m,1H),7.42~7.35(m,2H),7.23~7.19(m,1H),7.02(t, J=7.5 Hz,1H),6.80(d, J=7.0 Hz,1H),6.23(d, J=8.0 Hz,1H),4.72(bs,1H),4.66(d, J=3.5 Hz,1H),4.44~4.38(m,2H);HPLC(Daicel Chiralpak AD-H, V(hex)∶ V( iPrOH)=95∶5,0.5 mL/min,254 nm),tR:40.2 min(minor),59.0 min(major)。
10-[1-(2-溴苯基)-2-硝基乙基]-10 H-蒽-9-酮(3d):1H NMR(500 MHz,CDCl3), δ:8.22~8.18(m,2H),7.80(bs,1H),7.71~7.68(m,1H),7.61(d, J=6.5 Hz,1H),7.55(t, J=7.5 Hz,1H),7.49~7.45(m,1H),7.38(t, J=7.5 Hz,1H),7.17~7.13(m,1H),7.07(t, J=7.5 Hz,1H),6.72~6.71(m,1H),6.25(dd, J=1.5,8.0 Hz,1H),4.73(bs,1H),4.72(s,1H),4.36(d, J=6.0 Hz,2H);HPLC(Daicel Chiralpak AD-H, V(hex)∶ V( iPrOH)=95∶5,0.5 mL/min,254 nm), tR:42.9 min(minor),59.8 min(major)。
10-(呋喃基-2-硝基乙基)-10 H-蒽-9-酮(3e):1H NMR(500 MHz,CDCl3), δ:8.18(t, J=8.0 Hz,1H),7.67~7.63(m,1H),7.56~7.45(m,4H),7.22(s,1H),7.04((d, J=7.5 Hz,1H),6.21~6.19(m,1H),5.55(d, J=3.5 Hz,1H),4.66(d, J=3.5 Hz,1H),4.49(dd, J=7.0,13.5 Hz,1H),4.38~4.33(m,1H),4.23~4.19(m,1H);HPLC(Daicel Chiralpak AD-H, V(hex)∶ V( iPrOH)=95∶5,0.5 mL/min,254 nm), tR:37.2 min(major),41.5 min(minor)。
第4期张天一等:有机催化蒽酮与 β-硝基烯烃的不对称Michael加成反应应 用 化 学 第32卷 10-[1-(3-氟苯基)-2-硝基乙基]-10 H-蒽-9-酮(3f):1H NMR(500 MHz,CDCl3), δ:8.09(d, J=7.5 Hz,1H),8.02(d, J=7.5 Hz,1H),7.69~7.59(m,2H),7.55~7.40(m,4H),6.98~6.82(m,2H),5.88(d, J=7.5 Hz,1H),5.80~5.76(m,1H),4.86(dd, J=8.5,13.5 Hz,1H),4.59(dd, J=8.5,13.5 Hz,1H),4.55(d, J=3.5 Hz,1H),4.08~4.02(m,1H);HPLC(Chiralcel AS-H, V(hex)∶ V( iPrOH)=90∶10,0.8 mL/min,254 nm), tR:22.2 min(major),29.5 min(minor)。
10-[1-(3-氯苯基)-2-硝基乙基]-10 H-蒽-9-酮(3g):1H NMR(500 MHz,CDCl3), δ:8.11(d, J=7.5 Hz,1H),8.02(d, J=7.5 Hz,1H),7.69~7.60(m,2H),7.56~7.44(m,3H),7.41(d, J=8.0 Hz,1H),7.15~7.13(m,1H),6.89(t, J=8.0 Hz,1H),6.01(s,1H),5.96(d, J=7.5 Hz,1H),4.85(dd, J=8.5,13.5 Hz,1H),4.59~4.54(m,2H),4.05~4.00(m,1H);HPLC(Daicel Chiralpak AD-H, V(hex)∶ V( iPrOH)=95∶5,0.5 mL/min,254 nm), tR:53.6 min(minor),59.9 min(major)。
10-[1-(4-氟苯基)-2-硝基乙基]-10 H-蒽-9-酮(3h):1H NMR(500 MHz,CDCl3), δ:8.08(d, J=7.5 Hz,1H),8.00(d, J=7.5 Hz,1H),7.67~7.60(m,2H),7.53~7.42(m,4H),6.64(d, J=7.5 Hz,2H),6.02~5.99(m,2H),4.87(dd, J=9.0,13.0 Hz,1H),4.59~4.52(m,2H),4.06~4.02(m,1H);HPLC(Daicel Chiralpak AD-H, V(hex)∶ V( iPrOH)=95∶5,0.5 mL/min,254 nm), tR:58.2 min(major),68.0 min(minor)。
10-[1-(4-氯苯基)-2-硝基乙基]-10H-蒽-9-酮(3i):1H NMR(500 MHz,CDCl3), δ:8.11(d, J=8.0 Hz,1H),8.03(d, J=8.0 Hz,1H),7.68~7.59(m,2H),7.54~7.44(m,3H),7.40(d, J=7.5 Hz,1H),6.95(d, J=8.5 Hz,2H),6.02(d, J=8.0 Hz,2H),4.85(dd, J=8.5,13.0 Hz,1H),4.57~4.52(m,2H),4.06~4.02(m,1H); HPLC(Daicel Chiralpak AD-H, V(hex)∶ V( iPrOH)=95∶5,0.5 mL/min,254 nm),tR: 51.8 min(major),54.4 min(minor)。
10-[1-(4-甲基苯基)-2-硝基乙基]-10 H-蒽-9-酮(3j):1H NMR(500 MHz,CDCl3), δ:8.08(d, J=7.5 Hz,1H),8.00(d, J=7.5 Hz,1H),7.67~7.58(m,2H),7.53~7.49(m,2H),7.45~7.38(m,2H),6.76(d, J=8.0 Hz,2H),5.96(d, J=8.0 Hz,2H),4.84(dd, J=9.0,13.0 Hz,1H),4.57~4.52(m,2H),4.05~4.00(m,1H),2.22(s,3H);HPLC(Daicel Chiralpak AD-H, V(hex)∶ V( iPrOH)=95∶5,0.5 mL/min,254 nm), tR:28.0 min(minor),29.9 min(major)。
10-[1-(4-甲氧基苯基)-2-硝基乙基]-10 H-蒽-9-酮(3k):1H NMR(500 MHz,CDCl3), δ:8.07(d, J=8.0 Hz,1H),7.99(d, J=7.5 Hz,1H),7.66~7.65(m,2H),7.50~7.38(m,4H),6.47(d, J=8.5 Hz,2H),5.95(d, J=8.5 Hz,2H),4.83(dd, J=9.0,13.0 Hz,1H),4.55(dd, J=8.0,13.0 Hz,1H),4.49(d, J=3.5 Hz,1H),4.03~3.97(m,1H),3.68(s,3H);HPLC(Chiralcel OD-H, V(hex)∶ V( iPrOH)=70∶30,1.0 mL/min,254 nm), tR:20.3 min(minor),27.2 min(major)。
10-(1-硝基甲基-丁基)-10 H-蒽-9-酮(3l):1H NMR(500 MHz,CDCl3), δ:8.27~8.31(m,2H),7.62~7.67(m,2H),7.43~7.55(m,4H),4.37(dd, J=8.5,13.0 Hz,1H),4.33(d, J=3.5 Hz,1H),4.19(dd, J=6.5,13.0 Hz,1H),2.75~2.80(m,1H),1.03~1.25(m,3H),0.70(t, J=7.0 Hz,3H),0.56~0.67(m,1H);HPLC(Chiralpak AD-H, V(hex)∶ V( iPrOH)=98∶2,0.8 mL/min,254 nm), tR:24.1 min(minor),26.3 min(major)。
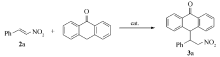
将催化剂1a~1f用于 β-硝基苯乙烯(2a)与蒽酮的不对称Michael加成反应中(Scheme 2),考察各种催化剂的催化性能。 并考察温度、溶剂及催化剂用量对反应立体选择性的影响,结果见表1。
| 表1 反式硝基苯乙烯与蒽酮的不对称Michael加成反应条件筛选 a Table 1 Screening of conditions for the asymmetric Michael addition reaction a |
由表1结果可以看出:1)6种催化剂均能以很高的产率(80%~98%)催化 β-硝基苯乙烯和蒽酮的不对称Michael加成反应。 其中奎宁衍生物催化剂1b表现出最好的催化性能(98% yield,94% ee,entry 10)。 测定其比旋光值[ α
将筛选出的最优催化条件应用于不同 β硝基烯烃的不对称Michael加成反应中,考察催化剂体系的普适性,结果见表2。
表2 蒽酮和不同硝基烯烃的不对称Michael加成反应 a Table 2 Asymmetric Michael addition reactions of anthrone with various trans-β-nitroolefins a 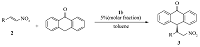 |
实验结果表明,筛选出的催化剂体系对不同取代 β-硝基烯烃与蒽酮的不对称Michael加成反应表现出优秀的普适性,对于芳环上不同取代基、不同取代位置的底物以及烷基取代的硝基烯烃,均能够以很高产率(91%~99%)得到相应的产品,并表现出优良的立体选择性(90%~95% ee)。
将金鸡纳生物碱衍生物催化剂用于蒽酮与硝基烯烃的不对称Michael加成反应,考察了溶剂、温度及催化剂用量等因素对反应立体选择性的影响,得到最佳的催化体系为:5%(摩尔分数)的催化剂1b,甲苯,室温反应。 将其应用于不同取代 β硝基烯烃和蒽酮的不对称Michael加成反应,表现出良好的普适性,得到很好的化学产率和高达95%的立体选择性。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|