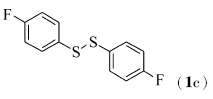
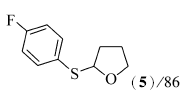
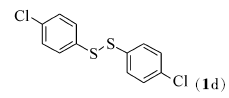
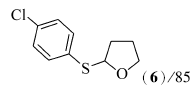
研究了醋酸酮催化二硫醚与四氢呋喃以氧化偶联反应构建C—S键。 结果表明,在醋酸酮(10%摩尔分数)、二硫醚(0.5 mmol)、四氢呋喃(2 mL)和双氧水(35%,2倍化学计量),反应温度120 ℃条件下,二硫醚与四氢呋喃能够顺利地发生氧化偶联反应,生成相应的C—S键化合物,合成硫醚类化合物产率中等到良好。 该反应以双氧水为氧化剂,具有环境友好等特性。
A new Cu(OAc)2-catalyzed oxidative coupling of disulfides with tetrahydrofuran for the synthesis of etherified sulfides has been developed. In the presence of Cu(OAc)2(10% molar fraction) and H2O2(35%, 2 equiv), a variety of disulfides(0.5 mmol) were treated with tetrahydrofuran(2 mL) at 120 ℃ to afford the corresponding etherified sulfides in moderate to high yields. This method employs 35% aqueous H2O2 as the green oxidant, and provides an efficient way for the formation of the C—S bonds.
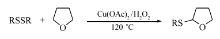
功能化的有机硫化物是许多具有生理活性的天然产物、药物和农药的基本骨架,它们在体内的新陈代谢及酶催化过程中起着重要作用,在新药的研发中也常常作为先导药物进行研究[1,2],探索高效、绿色构建C—S键的方法一直是人们关注的焦点。 氧化偶联反应是由氧化剂将C—H键氧化断裂,直接导入官能团构建C—C、C—O、C—S和C—N键等[2,3,4,5,6,7,8,9,10,11,12,13,14,15,16],根据技术手段,氧化偶联反应机制可分为无金属参与、金属参与以及光催化等方法。 C—H键直接官能团化可以避免使用官能团化的反应底物,提高原料利用率,减少废物的排放。 近10年来,应用C sp3—H键氧化偶联反应在构建C—C键方面取得了重要的进展,但应用类似方法构建C—杂原子键的研究相对较少[9,10,11],且反应所加入的氧化剂大多为有机过氧化物,反应后副产物和反应残留多,容易对环境造成不利影响。 最近,Li等[3]研究报道了在无金属条件下,分子筛促进TBHP(叔丁基过氧化氢)氧化酰胺氮原子邻位C sp3—H键直接硫化构建C—S键。 Han等[4]研究报道了环烷烃C sp3—H被DTBP(过氧化二叔丁基)氧化脱氢,在无金属条件下与二硫化物建了C—S键。 Lei等[5]也研究报道了碘单质促进的DTBP氧化烷烃C sp3—H键与硫醇构建C—S键。 在金属参与的C sp3—H键氧化偶联反应中,常使用过渡金属如钯、锆、钛、钽、铑、钌、铱、铜等为催化剂。 我们小组利用TBHP将四氢呋喃氧原子邻位C sp3—H键氧化脱氢,在催化量碳酸钠的作用下与二硫化物反应构建了C—S键[12]。 在本文中,继续研究以过氧化氢为氧化剂,以价廉的醋酸铜催化四氢呋喃氧原子邻位的C sp3—H键氧化断裂,与二硫醚直接构建C—S键,合成了硫醚类化合物,提高反应的经济性及绿色性(Scheme 1)。
ZF-2型三用紫外分析仪(上海安亭电子仪器制造厂);510p型傅里叶变换红外光谱仪(美国Nicolet公司);Bruker-300MHz型核磁仪(瑞士Bruker公司),内标为TMS,溶剂为CDCl3;GC-MS QP2010 Plus型质谱仪(日本岛津公司)。 所用试剂均为分析纯。
在25 mL的Schlenk反应瓶中,加入二硫醚1(0.5 mmol),四氢呋喃(2 mL),双氧水(35%,2倍化学计量)和醋酸铜(10%摩尔分数),混合物在120 ℃左右的Ar气气氛中反应,用TLC板跟踪反应进度。 反应结束后,将反应混合物冷却至室温,用乙酸乙酯(5 mL)萃取,饱和食盐水洗涤(1 mL×3),水相经乙酸乙酯萃取(2mL×3),有机相合并,再经无水硫酸钠干燥,减压蒸干溶剂,混合物经柱层析( V(己烷): V(乙酸乙酯)=15:1)分离提纯得目标产物。
2-苯巯基四氢呋喃(3)[13]:淡黄色油状物;1H NMR(500 MHz,CDCl3), δ:7.43(d, J=8.0 Hz,2H),7.17~7.25(m,3H),5.60~5.57(m,1H),3.95~3.99(m,1H),3.87~3.90(m,1H),2.30~2.33(m,1H),1.89~1.98(m,2H),1.79~1.85(m,1H);13C NMR(125 MHz,CDCl3), δ:135.8,131.0,128.9,126.8,87.3,67.2,32.6,24.9;MS(EI,70 eV) m/z(%):180(M+,100)。
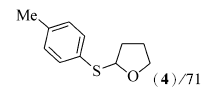
2-(4-甲苯巯基)四氢呋喃(4)[12]:淡黄色油状物;1H NMR(500 MHz,CDCl3), δ: 7.34(d, J=8.0 Hz,2H),7.02(d, J=8.0 Hz,2H),5.48~5.51(m,1H),3.91~3.96(m,1H),3.85~3.88(m,1H),2.21~2.27(m,4H),1.78~1.94(m,3H);13C NMR(125 MHz,CDCl3), δ:137.1,131.9,131.7,129.5,87.5,67.1,32.6,24.8,21.1;MS(EI,70 eV) m/z(%):194(M+,100)。
2-(4-氟苯巯基)四氢呋喃(5)[12]:无色油状物;1H NMR(500 MHz,CDCl3), δ:7.41~7.45(m,2H),6.93(t, J=8.0 Hz,2H),5.44~5.58(m,1H),3.92~3.96(m,1H),3.85~3.89(m,1H),2.25~2.29(m,1H),1.80~1.93(m,3H);13C NMR(125 MHz,CDCl3), δ:162.5(d, J=245.5 Hz,1C),133.8(d, J=8.0 Hz,2C),130.5(d, J=3.4 Hz,1C),115.8(d, J=21.6 Hz,2C),87.8,67.2,32.5,24.8;MS(EI,70 eV) m/z(%):198(M+,100)。
2-(4-氯苯巯基)四氢呋喃(6)[14]:淡黄色油状物;1H NMR(500 MHz,CDCl3), δ:7.35(d, J=8.0 Hz,2H),7.19(d, J=8.0 Hz,2H),5.51~5.54(m,1H),3.88~3.97(m,2H),2.29~2.31(m,1H),1.80~1.96(m,3H);13C NMR(125 MHz,CDCl3), δ:134.3,133.0,132.5,128.9,87.3,67.3,32.6,24.7;MS(EI,70 eV) m/z(%):216(M++2,35),214(M+,100)。
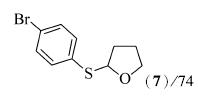
2-(4-溴苯巯基)四氢呋喃(7)[12]:淡黄色油状物;1H NMR(500 MHz,CDCl3), δ:7.29~7.34(m,4H),5.52~5.55(m,1H),3.86~3.96(m,2H),2.27~2.30(m,1H),1.80~1.95(m,3H);13C NMR(125 MHz,CDCl3), δ:135.0,132.6,131.8,120.9,87.2,67.2,32.6,24.7;MS(EI,70 eV) m/z(%):260(M++2,15),258(M+,16),71(100)。
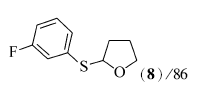
2-(3-氟苯巯基)四氢呋喃(8)[12]:淡黄色油状物;1H NMR(500 MHz,CDCl3), δ:7.16~7.20(m,3H),6.80~6.85(m,1H),5.60~5.64(m,1H),3.90~3.97(m,2H),2.28~2.36(m,1H),1.80~1.95(m,3H);13C NMR(125 MHz,CDCl3), δ:162.6(d, J=246.0 Hz,1C),138.2(d, J=8.0 Hz,1C),129.9(d, J=8.4 Hz,1C),125.9(d, J=3.0 Hz,1C),117.2(d, J=22.7 Hz,1C),113.6(d, J=21.0 Hz,1C),86.8,67.3,32.6,24.8;MS(EI,70 eV) m/z(%):198(M+,100)。
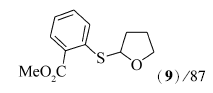
2-四氢呋喃-2-硫苯甲酸甲酯(9)[12]:淡黄色油状物;1H NMR(500 MHz,CDCl3), δ:7.84(d, J=8.5 Hz,1H),7.78(d, J=8.0 Hz,1H),7.38(t, J=7.5 Hz,1H),7.10(t, J=8.5 Hz,1H),5.66~5.69(m,1H),3.91~3.95(m,2H),3.82(s,3H),2.33~2.39(m,1H),1.98~2.02(m,2H),1.80~1.85(m,1H);13C NMR(125 MHz,CDCl3), δ:167.0,140.9,132.3,130.7,128.3,128.0,124.6,84.5,67.5,51.9,32.3,25.0;MS(EI,70 eV) m/z(%):238(M+,100)。
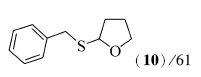
2-苄巯基四氢呋喃(10)[12]:淡黄色油状物;1H NMR(500 MHz,CDCl3), δ:7.13~7.28(m,6H),5.14~5.16(m,1H),3.80~3.90(m,3H),3.68(d, J=13.6 Hz,1H),2.09~2.14(m,1H),1.91~1.93(m,1H),1.71~1.79(m,2H);13C NMR(125 MHz,CDCl3), δ:138.5,128.9,128.4,126.7,83.0,66.8,35.0,32.0,24.8;MS(EI,70 eV) m/z(%):194(M+,100)。
以二苯二硫醚(1a)与四氢呋喃(THF,2)的反应为例,研究以双氧水为氧化剂,醋酸酮催化的化合物1a与化合物2氧化偶联反应生成目标产物3的情况,实验结果见表1。 实验结果表明,双氧水与醋酸酮的用量、反应温度等因素均对该反应有一定的影响。
表1 二苯二硫醚(1a)与四氢呋喃(2)在不同条件下的氧化偶联反应 Table 1 Oxidative coupling of 1,2-diphenyldisulfane(1a) with tetrahydrofuran(2) under different conditions a |
首先以35%的双氧水(2倍化学计量)为氧化剂,在不加任何催化剂的条件下,化合物1a(0.5 mmol)与化合物2(2 mL)在100 ℃下反应24 h,结果目标产物3的产率只有21%(Entry 1)。 当向反应中添加碘化亚酮、氯化亚铜、氯化铜、乙酰丙酮亚铁、三氯化铁或醋酸铜等催化剂,均能够促进该反应的进行(Entries 2~7),尤其是醋酸铜表现出很好的催化活性,收率达到75%。 当醋酸铜的用量增加到摩尔分数10%时,产物3的产率提高到81%(Entry 8)。 以过氧化二叔丁基(DTBP)代替双氧水作为反应的氧化剂,反应产率有所降低(Entry 9)。 此外,双氧水的用量对反应有一定的影响,当双氧水的用量降低,即以1.5倍化学计量于化合物1a的用量时,产物3的产率下降至46%(Entry 10),增加双氧水的用量,产率无明显变化(Entry 11)。 控制反应温度由100 ℃逐步升高,当温度在120 ℃时反应产率最高达91%(Entries 12~13)。
以上实验结果表明,以双氧水为氧化剂,醋酸铜为催化剂,化合物1a与化合物2发生氧化偶联反应生成目标产物3的较佳反应条件是:化合物1a(0.5 mmol)、化合物2(2 mL)、双氧水(35%,2倍化学计量)和醋酸铜(10%摩尔分数),反应温度120 ℃,Ar气气氛中反应。
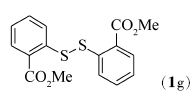
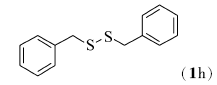
在上述较佳条件下,对其它二硫醚(1a~1h)与四氢呋喃(2)的氧化偶联反应进行研究,反应结果见表2。 在双氧水及醋酸铜的作用下,大多数二硫醚包括芳香族二硫醚(1b~1g)或脂肪族二硫醚(1h)均能与四氢呋喃顺利地发生氧化偶联反应并得到相应的中等和高产率的目标产物4~10。
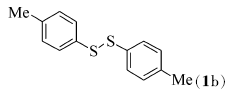
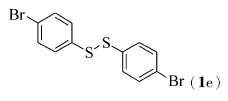
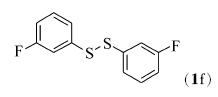
在双氧水(35%,2倍化学计量)、醋酸铜(10%摩尔分数)以及反应温度120 ℃下,对于芳香族的二硫醚,当芳环上含有供电子基团时,如对甲苯基二硫醚(1b)与化合物2能顺利地发生氧化偶联反应,目标产物4的产率为71%(Entry 1);当芳环上含有吸电子基团如F、Cl、Br或CO2Me等基团时,而且在芳环的不同取代位置上,均能够较好地发生反应,目标产物5~9的产率分别是86%、85%、74%、86%和87%(Entries 2~6)。 脂肪族二硫醚如二苄基二硫醚(1h)与化合物2也能较好地发生氧化偶联反应(Entry 7),目标产物的产率为71%。
表2 醋酸铜催化的二硫醚与四氢呋喃的氧化偶联反应 Table 2 Cu(OAc)2-catalyzed oxidative coupling reaction of disulfides(1) with tetrahydrofuran(2) a |
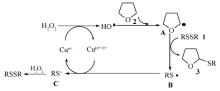
基于先前的报道和上述实验结果,氧化偶联反应机制是通过氧化C sp3—H键形成自由基过渡态,然后完成化学转换。 醋酸酮催化二硫醚与四氢呋喃的氧化偶联反应可能的反应机理如Scheme 2所示[15,16]。 首先,在醋酸酮促进下,双氧水很容易发生过氧键断裂生成活性自由基HO·,HO·诱导化合物2氧邻位 sp3的C—H键生成碳自由基中间体A,碳自由基中间体A再与二硫醚1反应生成目标产物3以及自由基RS·(B),自由基B在高价态铜的作用下,通过单电子转移生成RS+(C)和低价态铜,低价铜继续下一次的催化循环,在双氧水的氧化下,RS+(C)很容易转化为二硫醚RSSR。
我们发展了一种催化二硫醚与四氢呋喃通过氧化偶联反应直接构建C—S键化合物的新方法。 该方法以价廉的醋酸铜为催化剂,双氧水为氧化剂,通过氧化偶联反应构建C—S键,合成硫醚类化合物,反应具有经济性及绿色性。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|