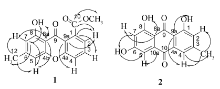
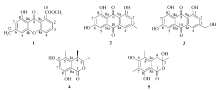
研究了红树林植物尖瓣海莲叶内生真菌 Penicillium sp.B21次级代谢产物。 用硅胶柱层析、制备薄层层析和重结晶等方法,从该菌发酵液的乙酸乙酯萃取相中首次分离获得5个单体化合物,运用现代波谱技术、单晶X射线衍射以及文献数据对照,鉴定其结构分别为8-羟基-6甲基-1-甲氧羰基酮(1)、大黄素(2)、 ω-羟基大黄素(3)、(3 R,4 S)-6,8-二羟基-3,4,5-三甲基-3,4-二氢异香豆素(4)和3,6,8-三羟基-3,5,7-三甲基-3,4-二氢异香豆素(5)。 首次获得了sclerotinin B单晶结构。
The secondary metabolites of the medicinal mangrove endophytic fungus Penicillium sp.B21 were investigated. Five compounds were firstly isolated from the ethyl acetate extract of the fermentation mixture using silica gel column chromatography, preparative thin-layer chromatography and recrystallization. The structures of these compounds were identified as janthinone(1), emodin(2), citreorosein(3), decarboxydihydrocitrinone(4) and sclerotinin B(5), by comprehensive spectroscopic characterizations, X-ray single crystal diffraction as well as comparison with reported data. The single crystal structure of compound 5 was firstly obtained.
植物内生菌(endophyte)是指一类在其部分或全部生活史中存活于健康植物组织内部,而不使宿主植物表现出明显感染症状的微生物[1]。 红树林植物内生真菌次级代谢产物具有结构多样性和显著的生物活性等特征,红树林植物内生真菌已成为寻找具有生物活性的先导化合物的重要资源。 国内外研究人员对很多红树林植物包括尖瓣海莲( Bruguiera sexangula var. rhynchopetala)进行了化学成分研究[2,3]。 但截至目前尖瓣海莲内生真菌次级代谢产物的研究未见报道。 本文选择海南红树植物尖瓣海莲叶内生真菌青霉菌 Penicillium sp.B21作为目标菌株,从其发酵液乙酸乙酯萃取相中分离得到5个化合物(Scheme 1)。
X4型显微熔点仪(北京光电仪器厂),温度未校正;Bruker400M型核磁共振仪(瑞士Bruker公司);G6300型液-质联用仪(美国Agilent科技公司),Gemini A Ultra型X射线单晶衍射仪(美国Agilent科技公司)。 石油醚、乙酸乙酯、氯仿、甲醇等为工业试剂,使用前重蒸;葡萄糖(CR),粗海盐(微生物养殖用);薄层层析硅胶GF254和柱层析硅胶(青岛海洋化工厂)。
菌株于2013年8月分离自海南东寨港红树林自然保护区的尖瓣海莲叶,经形态学和分子生物学鉴定该菌株为青霉属真菌,该菌种现保存于热带药用植物化学教育部重点实验室。 无菌状态下取尖瓣海莲样品,用无菌水冲洗3遍,0.01升汞浸泡 1 min,无菌水冲洗3遍,75%酒精浸泡30 s,无菌水冲洗3遍。 将组织切块,置于PDA(马铃薯200 g、葡萄糖20 g、琼脂15 g、陈海水1000 mL、pH=7.2)培养基中,28 ℃恒温倒置培养。 待菌丝长出后,挑取尖端菌丝转接至新的培养基上,几次纯化后得到共附生真菌并转接到试管斜面上保存备用。 发酵培养基为PDA培养基,添加葡萄糖25 g/L,粗海盐36 g/L,1000 mL三角瓶内装400 mL培养液,经121 ℃(0.1 MPa)高温灭菌25 min后,在超净工作台上接种100 L,28 ℃静置培养40 d。
将所得发酵液过滤得发酵液和菌丝体。 发酵液用乙酸乙酯充分萃提,菌丝体用甲醇充分浸提。 合并萃取液,使用旋转蒸发仪浓缩后硅胶柱色谱分离。 以石油醚-乙酸乙酯(体积比10:1,5:1,3:1,1:1,1:3),乙酸乙酯-甲醇(体积比10:1,5:1,3:1,1:1,1:3)梯度洗脱,收集各组分,再经反复柱层析、薄层层析、重结晶等方法纯化得到化合物1(550 mg)、化合物2(300 mg)、化合物3(350 mg)、化合物4(55 mg)、化合物5(90 mg)。
化合物1:无色块状晶体(甲醇),mp 197.9~198.2 ℃。 EI-MS( m/z):284(100%);1H NMR(400 MHz,CDCl3), δ:12.15(s,1H,8-OH),7.74(dd, J=8.5,7.3 Hz,1H,H-3),7.52(dd, J=8.5,1.0 Hz,1H,H-4),7.28(dd, J=7.3,1.0 Hz,1H,H-2),6.75(d, J=6.69 Hz,1H,H-5),6.63(d, J=6.69 Hz,1H,H-7),4.03(s,3H,H-11),2.43(s,3H,H-12);13C NMR(100 MHz,CDCl3), δ:180.5(C-9),169.7(C-10),161.5(C-8),155.9(C-4a),155.7(C-4b),149.4(C-6),134.8(C-3),133.6(C-1),122.5(C-2),119.4(C-4),117.6(C-9a),111.7(C-7),107.4(C-5),106.9(C-8a),53.2(C-11),22.7(C-12)。
化合物2:桔红色针状晶体(甲醇),mp 258.0~258.5 ℃。 EI-MS( m/z):270(100%);1H NMR(400 MHz,Acetone-d6), δ:12.0,11.9,11.3(s,1H,each,OH),7.4(s,1H,H-4),7.1(d, J=2 Hz,1H,H-5),6.9(s,1H,H-2),6.5(d, J=2 Hz,1H,H-7),2.3(s,3H,CH3);13C NMR(100 MHz,Acetone-d6), δ:190.3(C-9),181.6(C-10),167.5(C-8),165.6(C-1),162.3(C-6),148.3(C-3),135.6(C-10a),133.4(C-4a),123.9(C-4),120.5(C-2),113.7(C-9a),109.8(C-5),108.8(C-8a),108.0(C-7),21.1(CH3)。
化合物3:橙色针状晶体(丙酮),mp 151~152 ℃。 EI-MS( m/z):286(100%);1H NMR(400 MHz,Acetone-d6), δ:12.1(s,2H,OH),10.1 (s,1H,OH),7.65(s,1H,H-5),7.26(s,1H,H-7),7.13(d, J=4 Hz,1H,H-4),6.60(d, J=4 Hz,1H,H-2),5.58(s,1H,CH2OH),4.61(s,2H,CH2OH);13C NMR(100 MHz,Acetone-d6), δ:189.7(C-9),181.5(C-10),165.8(C-6),164.5(C-8),161.5(C-1),152.8(C-3),135.2(C-10a),132.9(C-4a),120.8(C-4),117.1(C-2),114.1(C-9a),108.9(C-5),107.9(C-8a),62.0(CH2OH)。
化合物4:无色针状晶体(甲醇),mp 217~218 ℃。 EI-MS( m/z):222(100%);1H NMR(400 MHz,Acetone-d6), δ:11.31(s,1H,8-OH),9.38(brs,1H,6-OH),6.21(m,1H,H-7),4.59(m,1H,H-3),3.02(m,1H,H-4),1.96(s,3H,Me-5),1.15(m,6H,Me-3,Me-4);13C NMR(100 MHz,aceton-d6), δ:169.4(C-1),163.7(C-6),163.3(C-8),144.1(C-4a),114.8(C-5),101.4(C-7),100.1(C-8a),80.7(C-3),35.2(C-4),20.1(Me-3),19.9(Me-4),10.1(Me-5)。
化合物5:无色块状晶体(甲醇),mp 192.9~193.2 ℃。 EI-MS( m/z):238(100%);1H NMR(400 MHz,Acetone-d6), δ:11.77(brs,1H,8-OH),9.56(brs,1H,6-OH),7.49(brs,1H,6-OH),3.10(m,2H,H-4),2.13(s,3H,Me-10),2.07(s,3H,Me-9),1.70(s,3H,Me-11);13C NMR(100 MHz,aceton-d6), δ:170.1(C-1),160.3(C-8),159.2(C-6),134.4(C-4a),114.1(C-5),108.1(C-7),102.4(C-3),99.7(C-8a),35.7(C-4),27.4(C-11),11.3(C-9),8.7(C-10)。
对化合物1在氯仿/甲醇中培养1星期,得到无色长方体型晶体,取一片0.4 mm×0.2 mm×0.2 mm的晶体进行单晶衍射分析。 化合物5在甲醇中培养得到无色块状晶体。 利用Agilent Technologies Gemini A Ultra X射线单晶衍射仪,用石墨单色化的Mo- Kδ( λ=0.154184 nm)为衍射源,293 K下采集单晶衍射数据。 用SHELXL-97程序直接法解出晶体结构,数轮差值Fourier拟合确定非氢原子坐标,对全部非氢原子坐标及各向异性参数进行全矩阵最小二乘法修正,氢原子位置按照理论模型计算。
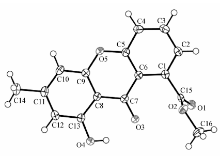
化合物1:从氢谱可以看到, δ 9.0以上为酚-OH的信号区, δ 12.15提示有1个缔合的酚羟基;有1个1,2,3-三取代的苯环[ δ 7.28(dd, J=7.3,1.0 Hz,1H,),7.52(dd, J=8.5,1.0 Hz,1H),7.74(dd, J=8.5,7.3 Hz,1H)],一个甲氧基[ δ 4.03(s,3H)],以及一个甲基[ δ 2.43(s,3H)]。 结合碳谱, δ 180.5为一个氢键缔合羰基的信号, δ 155.9、155.7为典型的连氧芳碳的位移值,猜测该化合物具有酮的母核结构[4]。 经二维谱图分析以及已报道数据比对[5],确定该化合物的结构为Janthinone。 单晶X射线衍射分析进一步确证该化合物的结构。
化合物2:该化合物的碳谱有两个羰基峰[ δ 190.3、181.6],此外还有12个芳碳信号,提示具有蒽醌母核结构。 从氢谱可以看出,低场有两个与羰基缔合的酚羟基[ δ 12.05(s,1H),11.94(s,1H)],提示两个羟基是1,8-二羟基。 还能明显看出苯环上的氢是间位取代( J=2.2 Hz),结合二维谱图以及已报道的文献[6],可以判断该化合物为大黄素。
化合物3:该化合物的碳谱有两个羰基峰[ δ 189.7、181.5],此外还有12个芳碳信号,提示具有蒽醌母核结构。 δ 62.0为一个连氧碳。 δ 12.1(s,2H)提示1,8-位有两个酚羟基; δ 7.13(d, J=2.3 Hz,1H),6.59(d, J=2.3,1H)为同一苯环上间位的H, δ 5.58的一个宽峰为醇羟基峰。 结合二维谱图以及已报道的文献[7],可以判断该化合物为 ω-羟基大黄素。
化合物4:从氢谱可以看出, δ 11.3为一个缔合的酚羟基, δ 9.38为一个自由的酚羟基。 低场区有一个单峰[ δ 6.21(s,1H)],提示有一个五取代的苯环, δ 4.59、3.02为次甲基峰,其中前者与氧相连。 从碳谱可以看出, δ 169.4为一个酯羰基, δ 163.7~100.1为芳碳信号, δ 80.7和35.2为两个次甲基碳,前者与氧相连,此外还有3个端甲基信号, δ 20.0、19.9和10.1。 结合二维谱图以及已报道的文献[8],可以判断该化合物为decarboxydihydrocitrinone。
化合物5:氢谱显示有2个苄基氢 δ 3.10 (m,2H,H-4),1个甲基 δ 1.70(s,3H,Me-11),2个芳甲基 δ 2.13(s,3H,Me-10)和 δ 2.07(s,3H,Me-9),碳谱显示有1个酯羰基 δ 170.1(C-1)以及1个苯环。 结合已报道的文献[9],可判断该化合物为Sclerotinin B。 单晶X射线衍射分析进一步确证该化合物的结构。
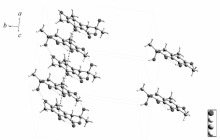
化合物1的晶体结构如图2所示。 晶体空间群为I2/a,晶胞参数 a=1.32775(4) nm, b=1.04031(2) nm, c=1.96513(5) nm, α=90°, β=104.907(3)°, γ=90°;分子式为C16H12O5,相对分子质量 Mr=284.26,晶胞体积 V=2.62259(12) nm3,晶胞内分子数 Z=8, Dx =1.400 g/cm3, μ=0.905 mm-1, F(000)=1184, R=0.0406, wR2=0.1102(2345)。
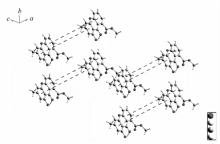
通过platon分析结果表明,分子中3个环几乎在一平面上,平面之间具有强烈的pi-pi堆积相互作用( α=3.58°, β=22°, γ=22°,平面之间的垂直距离为0.329nm);同时存在一个分子内氢键(9-羰基氧原子与8-羟基氢原子,H—O键长为0.189 nm,O—H—O键长为0.263 nm)。 晶胞堆积图如图3所示。
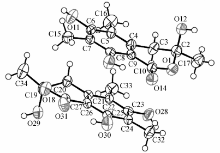
化合物5的晶体结构如图4所示。 晶体空间群为P 21/c,晶胞参数 a=0.74894(4) nm, b=1.73259(10) nm, c=1.77508(10) nm, α=90°, β=96.237(5)°, γ=90°;分子式为C16H14O5,相对分子质量 Mr=238.23,晶胞体积 V=2.2897(2) nm3,晶胞内分子数 Z=4, Dx=1.382 g/cm3, μ=0.0108 mm-1, F(000)=1008.0, R=0.1486, wR2=0.4833(4680)。
通过platon分析结果表明,该化合物形成一个分子内氢键,(1-羰基氧原子与8-羟基氢原子,H—O键长为0.189nm,O—H—O键长为0.260nm);此外2个分子还形成2个分子间氢键,即6-羟基氧(氢)原子分别与相邻分子的3-羟基氢(氧)原子形成氢键(H—O键长为0.204 nm,O—H—O键长为0.280 nm)。 由于氢键的饱和性,该晶体中存在两两成对的分子,导致晶体中非对称单元中存在3个相同的分子。 分子中苯环之间的pi-pi堆积作用( α=2.6°, β=20.8°, γ=20.2°,平面之间的垂直距离为0.353 nm)将分子串起来像个“葫芦串”。 晶胞堆积图如图5所示。 该晶体结构为首次获得,其晶体学数据已上传于剑桥晶体数据中心(CCDC号:1047539)。
传统药用植物和特殊生境中的植物的内生真菌是重要的生物资源[10]。 本文选择海南红树植物尖瓣海莲叶内生真菌青霉菌 Penicillium sp. B21作为目标菌株,从其发酵液乙酸乙酯萃取相中分离得到8-羟基-6甲基-1-甲氧羰基酮(1)、大黄素(2)、 ω-羟基大黄素(3)、(3 R,4 S)-6,8-二羟基-3,4,5-三甲基-3,4-二氢异香豆素(4)和3,6,8-三羟基-3,5,7-三甲基-3,4-二氢异香豆素(5)。 所有化合物均为首次从尖瓣海莲叶内生真菌得到,并首次获得sclerotinin B单晶结构。 其中大黄素是一种蒽醌类化合物,具有免疫调节、抗菌、抗炎和抗肿瘤等多方面的药理作用,目前主要是从蓼科植物虎杖中提取。 通过生物发酵的办法,可高效廉价的得到大黄素单体,具有广阔的应用前景,值得进一步研究。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|