将核壳微凝胶包埋在两性基质中,制备了复合水凝胶(CAH)。 研究发现,利用微凝胶与聚合物链之间的物理缠结作用,可以使复合凝胶具有致密的网络结构,力学性能显著提高;复合凝胶对pH和离子强度敏感,呈现出典型的两性聚电解质凝胶的溶胀行为。 同时微凝胶的存在和特殊的复合结构,可赋予CAH两性凝胶基质所不具有的响应性,并实现在高温下快速响应。
The composite polyampholyte hydrogels(CAH) were prepared by inserting core-shell microgel particles into a bulk polyampholyte matrix. CAH gels with uniform and tight network structure have excellent mechanical performance due to the entanglement between microgels and network chains, and exhibit an antipolyelectrolyte effect and pH-sensitivity. And ionic strength drastically affects their swelling behaviors. Meanwhile, CAH gels show rapid shrinking rate and transmittance switch in response to the temperature change as a result of the incorporation of microgel particles.
智能水凝胶[1, 2]可在外界刺激下产生体积或形态的变化, 利用这一特性及其良好的生物相容性, 可应用于组织工程[3]、药物控制释放[4]、化学传感器[5]及生物分离[6]等方面。 其中同时含有阴、阳离子基团的两性水凝胶[7], 因其特殊的反聚电解质效应[8, 9]及抗衡离子挤出效应[10, 11]而备受关注。 但其力学强度低、韧性差等缺点限制了在实际生活中的应用。
复合材料不仅可以改进原材料性能, 实现增韧、增强效应, 还可能引进新的基团赋予材料新功能。 如Thé venot等[12]制备了疏水聚乙烯粒子与聚丙烯酰胺的复合水凝胶, 增强了凝胶强度。 微凝胶因为较高的比表面积而具有更快的响应速率, 同时与宏观凝胶基质具有良好的相容性, 更适用于复合水凝胶的制备。 本文首先合成了以聚(N-异丙基丙烯酰胺)为核, 聚乙烯胺为壳的温敏微凝胶, 进而将微凝胶物理掺杂在两性凝胶基质中制备复合水凝胶, 以期在改善水凝胶力学性能的同时, 赋予水凝胶新的温度响应性。
聚乙烯胺(PVAm, 相对分子质量为3× 104); 特丁基过氧化氢(TBHP, 70%水溶液, Aldrich); N-异丙基丙烯酰胺(NIPAAm, Acros, 正己烷/甲苯混合溶剂重结晶); N, N'-亚甲基双丙烯酰胺(MBA, Alfa Aesar); 丙烯酰胺(AAm, 北京化工厂); 丙烯酸(AAc, 北京益利精细化学品有限公司); 丙烯酰氧乙基三甲基氯化铵(DAC, 80%水溶液, 日本三洋化工); 偶氮二异丁咪唑啉盐酸盐(VA-044, 北京化工厂)。
WSM-10KN型电子万能试验机(长春智能仪器设备有限公司), 10 KN传感器, 圆柱形样品原始高度22 mm, 直径14 mm, 压缩速度为2 mm/min; UV-2401PC型变温紫外光谱仪(日本岛津公司), 样品长度20 mm, 宽度8 mm, 厚度为2 mm, 测试温度变化范围为20~45 ℃, 变温速度为1 ℃/min; Model XL30 ESEM型场发射扫描电子显微镜(荷兰Philips公司), 样品测试前真空冷冻干燥, 表面喷金, 操作电压为10~15 kV; VERTEX-70型红外光谱仪(德国Bruker公司), 采用粉末KBr压片共研磨法, 扫描次数32, 分辨率2 cm-1; AV-400型核磁共振仪(德国Bruker公司), 核壳微凝胶样品离心提纯干燥后, 置于D2O中重新溶胀分散测定1H NMR谱图; CGS-3型激光光散射仪(德国ALV公司), 光波长658.0 nm, 散射角为90° , 分别在25和45 ℃各测定一次。
核壳微凝胶采用无皂乳液聚合[13]制备。 向烧杯中依次加入纯化的1.20 g NIPAAm, 3.20 g MBA(0.5%水溶液), 0.30 g PVAm, 加水溶解。 反应体系总质量为30 g, 固含量为5%, 溶液的pH值调节至7~8。 聚合反应在装有回流冷凝管、机械搅拌装置和氮气导管的100 mL三口烧瓶中进行。 通N2气除氧30 min后, 加入0.60 g TBHP(0.1%水溶液)作为引发剂, 反应在250 rad/s、70 ℃加热油浴中进行6 h。 反应停止后, 自然冷却至室温得到乳白色乳液。
AAc首先在冰水浴中用NaOH(30%溶液)中和配成质量分数20%的水溶液。 分别称取1.00 g AAm、0.82 g AAcNa(20%溶液)和0.42 g DAC(80%溶液), 反应溶液(共10 g)中共聚单体的质量分数为15%, 摩尔比为8: 1: 1。 按一定比例加入核壳微凝胶乳液(5%溶液), 微凝胶占单体质量分数分别为5%、10%、15%、20%和25%。 最后将一定量的MBA(0.5%溶液)加入上述溶液中, 搅拌混合, 得到稳定、均匀的反应液。 将溶液转移到试管中, 脱气并充入N2气保护后, 加入0.30 g VA-044(1%溶液)在50 ℃下引发聚合, 反应24 h。 将所得水凝胶切成薄片, 在蒸馏水中浸泡7 d, 每天换1次水, 以除去溶胶部分。 将水凝胶在烘箱中50 ℃干燥恒重。 CAH(a, b)中a、b分别代表MBA、微凝胶与共聚单体质量比。
将称重的干凝胶浸泡于25 ℃水中, 每隔一定时间取出, 用滤纸擦干表面的游离水, 称重直至质量不再改变, 达到平衡状态为止。 平衡溶胀倍率(ESR):
ESR/%=[(me-m0)/m0]× 100(1)
式中, m0为干凝胶初始质量, me为溶胀平衡时水凝胶的质量。
使用NaCl配制不同浓度的盐水溶液。 采用HCl或NaOH配制不同pH值的溶液, 加入0.9%的NaCl去除离子强度的影响。 去溶胀实验:将在室温下平衡溶胀的凝胶样品置入45 ℃的去离子水中, 每隔一定时间取出测定质量, 溶胀倍率Mt与室温下ESR百分比值随时间变化的曲线为去溶胀曲线。
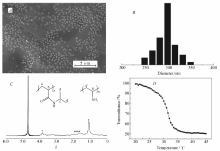
在本实验体系中, TBHP与PVAm上的伯胺基团形成氧化还原对, 70 ℃下产生大分子自由基, 引发NIPAAm单体接枝聚合。 形成以PVAm为主链, PNIPAAm为侧链的接枝聚合物。 其中PNIPAAm处于疏水状态, 反应过程中, 两亲性的接枝聚合物起到稳定剂的作用, 同时在交联剂MBA存在下, 自组装形成以PNIPAAm为核, PVAm为壳的微凝胶。 动态光散射(DLS)测试:在25 ℃下, 微凝胶粒径为429 nm, 多分散系数PDI为0.04; 在45 ℃下, PNIPAAm处于疏水状态, 微凝胶收缩, 粒径为289 nm, 多分散系数PDI为0.10。 图1A为微凝胶样品的SEM照片, 微凝胶呈现球形粒子; 对图中的粒子进行统计计算, 如图1B所示, 微凝胶的平均粒径为300 nm左右, 具有良好的单分散性。 由于电子显微镜样品是在微凝胶完全干燥后测试, 因此所得样品粒径要小于DLS实验结果。 图1C为提纯后微凝胶的1H NMR谱图, 化学位移归属为:δ 1.1和3.9分别对应NIPAAm异丙基上的甲基和亚甲基; δ 1.2~2.4为主链上— CH2— 和— CH— 的化学位移。 微凝胶组成中PVAm和PNIPAAm的质量比(AWR)可由下式计算:
AWR=(2× A1/A2-1)× 43.07/113.18(2)
式中, A1为主链质子峰的积分面积, A2为甲基质子峰的积分面积。 计算结果表明AWR为1: 5.81。 图1D考察了温度对微凝胶乳液体系透光率的影响, 当温度较低时, 乳液具有较高的光学透过率, 当温度升高, 在31~33 ℃之间, 透过率突然减小, 之后趋于平稳。 可知微凝胶的相转变温度(LCST)为32 ℃。
图2A为CAH的红外光谱图。 复合凝胶对应的1735、1664和1557 cm-1分别为酯基、酰胺基和羧基上羰基特征吸收峰, 表明其由AAm、AAcNa和DAC 3种结构单元组成; 1370~1385 cm-1为异丙基的特征吸收峰, 表明微凝胶掺入基质中。
图2B、C分别是CAH和两性凝胶基质的SEM照片。 从图中可以看出, CAH内部呈现较均匀的网络结构, 相比于基质, 其内部孔径更小、更致密。 造成这种现象的原因可能是:微凝胶均匀分散在溶液中; 由于扩散, 共聚单体不可避免地存在于微凝胶内部, 在链增长过程中, 聚合物链穿过微凝胶, 与其内部网络相互缠绕。 最终在复合凝胶网络中, 填充的微凝胶粒子起到了物理交联的作用[14, 15]。 所以在相同MBA含量的情况下, CAH具有更致密的网络结构。
微凝胶、MBA含量对CAH力学性能的影响如图3所示。 在压缩测试中, 两性水凝胶基质(AH, MBA含量为0.1%)的断裂形变仅为68%, 断裂强度为0.14 MPa。 与此相比, CAH的断裂形变均高于80%, 适当的微凝胶、MBA含量可使其压缩强度维持在1 MPa以上。 CAH韧性及强度的提高可归因于微凝胶对两性基质的增强效应, 以及聚合物链与微凝胶网络的相互缠绕。 当外界应力达到一定值时, 交联密度更高的微凝胶可率先发生断裂来耗散多余的能量[16], 从而避免了整个网络上裂纹的产生及延展, 阻止了宏观凝胶的断裂。
从图3A可看出, 相同MBA含量(0.1%)CAH的断裂形变及断裂强度随填充微凝胶含量的增加而逐步减小。 微凝胶含量在3%~8%之间变化时, CAH的断裂强度在5 MPa左右变动。 当微凝胶含量为5%时, 复合凝胶具有最优力学性能, 断裂强度5.17 MPa, 断裂形变96%。 这是由于在制备过程中, 相比其它部位, 微凝胶的周围更容易形成致密的网络结构[17], 随着微凝胶含量的增加, 这种现象愈加明显而导致整个网络的均匀性下降, 从而力学性能降低。
图3B考察了固定微凝胶含量为10%, MBA含量对CAH力学性能的影响。 断裂强度在MBA含量为0.1%时出现峰值。 当MBA用量较低时, 体系不能形成完善的交联网络, 部分聚合物可溶解, 因而具有较低的模量和强度; 随着MBA用量增加, 凝胶交联密度增大, 具有较高的模量; 当MBA用量过高时, 交联点分布变得更加不均匀, 因此凝胶强度降低、变脆。
CAH网络中同时带有正、负离子基团, 因而对不同pH值水溶液具有特殊的应答性。 图4A为CAH样品ESR与pH值的关系曲线。 在5< pH< 8时, 其溶胀倍率最小; 而当pH< 5或pH> 8时, 其溶胀倍率都增大。 在等电点附近, 网络中正、负电荷吸引形成离子交联结构, 同时凝胶内部的渗透压也较小, 因而凝胶具有较小的ESR。
图4B为将CAH样品分别置于不同浓度的NaCl溶液中的平衡溶胀倍率曲线。 从图4B可以看出, 随着离子强度的增加, ESR不断减小; 而在较高离子强度溶液中, ESR开始增大, CAH表现出反聚电解质凝胶溶胀特点。 这是由网络中静电作用和凝胶内外渗透压差共同决定的。 在高离子强度时, 凝胶网络上的电荷完全被溶液中的反离子所屏蔽, 减弱了阴阳离子静电引力, 离子交联解离, 导致ESR增大。
图5A为溶胀后的CAH样品的透光率随温度的变化曲线。 从图5A可以看出, 在低温时, 凝胶具有较高的透光性; 当温度升高至30 ℃时, 透光率开始急剧下降, 凝胶变为不透明的乳白色; 当降温冷却时, 凝胶恢复透明性。 这说明CAH具有快速的温度响应特性, 其相转变温度与微凝胶的基本相同, 说明物理交联没有对微凝胶温敏性产生显著影响。 图5B为CAH在45 ℃去离子水中的去溶胀曲线。 复合水凝胶都有一定程度的脱水, MBA含量高的样品失水率较低, 微凝胶含量高的样品具有更快的去溶胀速率, 类似的现象也存在于透光率实验中。 造成这种现象的可能原因是:当温度高于LCST时, 微凝胶开始收缩, 与凝胶基质发生分离, 形成溶剂孔道; 同时因为链缠绕、物理交联作用, 微凝胶的收缩牵引网络中聚合物链的移动, 最终将多余的水分排出[14, 18]。 而MBA含量高的样品, 交联密度大, 网络链移动性差, 所以失水率较低。
通过无皂乳液聚合制备了单分散性的温敏核壳微凝胶, 将其引入至两性水凝胶基质合成具有高机械强度的复合水凝胶。 微凝胶均匀分布在网络中, 与聚合物链物理缠绕、相互作用, 对基质起到增韧作用。 调节MBA含量、微凝胶含量, 可以调控复合水凝胶的压缩强度、断裂形变及溶胀性能。 复合水凝胶对pH敏感, 在等电点附近具有最小的ESR; 具有一定的耐盐性, 表现出反聚电解质凝胶溶胀行为; 同时具有快速的温度响应性质。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|