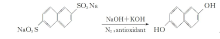以便宜的2,6-萘二磺酸钠为原料,通过一步混合碱高温碱熔法合成高纯度2,6-二羟基萘。 N2气保护下,添加苯酚或抗氧剂1010防止过度氧化焦油的产生,能显著提高2,6-二羟基萘收率。 较佳反应条件为:2,6-萘二磺酸钠与混合碱的质量比1∶3,混合碱中氢氧化钠和氢氧化钾质量比2∶1,使用0.5 g苯酚或抗氧剂1010,反应温度345 ℃,反应时间2 h,碱熔收率达到86.3%。 经过甲醇-水混合溶剂精制,2,6-二羟基萘纯度能达到99%。
High purity 2,6-dihydroxynaphthalene was synthesized by one-pot alkali fusion using cheap disodium 2,6-naphthalenedisulfonate as the starting material. Under nitrogen atmosphere, in order to avoid overoxidation and obtain high yield of 2,6-dihydroxynaphthalene, phenol or antioxidant 1010 was added. Under the optimal technological conditions, the mass ratio of disodium 2,6-naphthalenedisulfonate and alkali 1∶3, the mass ratio of sodium hydroxide and potassium hydroxide 2∶1 in mixed alkali, the reaction temperature 345 ℃, the yield of 2,6-dihydroxynaphthalene in the alkali fusion is 86.3%. It is confirmed that the purity of 2,6-dihydroxynaphthalene is up to 99% after being refined by a methanol-water mixed solvent.
2, 6-二羟基萘为灰白色至白色片叶状晶体。 熔点215~220 ℃, 在纤维、薄膜、电子元件、包装容器以及染料医药等领域具有广泛的应用, 是制备各种聚酯材料和液晶聚酯树脂的重要中间体[1, 2, 3, 4, 5]。 国内关于2, 6-二羟基萘生产及合成研究的报道均很少, 只有某公司相关的专利[6]报道。 该报道与国外早期有些关于磺化碱熔法制备2, 6-二羟基萘的报道相似, 合成路线均是在高温330 ℃下, 将2, 6-萘二磺酸在氢氧化钾或氢氧化钠中碱熔, 反应3 h, 2, 6-萘二磺酸转化率为99%。 在该工艺中, 普遍使用有机物作为溶剂, 例如氢化联苯[7]为溶剂, 转化率为46%, 选择性为58%; 添加苯酚, 以二苄基甲苯[8]为溶剂, 反应1.5 h, 2, 6-二羟基萘收率约为80%; 添加油基磺酸钠、硫酸钾, 以矿物油(脂肪或脂环烃混合物)为溶剂, 反应3.5 h, 原料转化率为99%, 2, 6-二羟基萘选择性为85%[9]。 上述报道中均未提到产品具体纯度, 采用有机物做溶剂, 如二苄基甲苯、氢化联苯等, 理论上可以套用, 但是反应过程中产物中焦油成分溶于有机溶剂, 有机溶剂经过一次反应后, 污黑粘腻, 难以分离, 致使反应成本高, 有机溶剂难套用, 加重环境负担。 还有一种合成路线[10], 先合成薛弗氏酸(即2-萘酚-6-磺酸), 在一定条件下由薛弗氏酸合成2, 6-二羟基萘。也可由2-萘酚合成薛弗氏酸, 进一步反应合成2, 6-二羟基萘。 路线分两步完成, 路线增长, 易造成物料浪费及收率较低问题。 还有一种方法[11], 在甲醇-水的介质中, 水解2, 6-二乙酰氧基萘, 得到高纯度的2, 6-二羟基萘, 但该工艺原料不易得到, 过程复杂, 未见有关工业化报道。
该产品市场前景广阔, 主要供出口, 国外订单达到每吨80万元。 某公司用萘经过一定条件磺化生产2, 7-萘二磺酸钠时, 由于平行反应产生的主要副产物是2, 6-萘二磺酸钠, 多年的生产致使2, 6-萘二磺酸钠大吨量堆积。 本文利用2, 6-萘二磺酸钠为原料制备2, 6-二羟基萘, 廉价易得。 使用氢氧化钠和氢氧化钾混合碱, 提高碱熔剂的活性同时降低原料成本, 本文放弃有机物作为溶剂, 降低成本, 缩减工艺, 降低环境负担, 通N2气并且添加苯酚或抗氧剂1010, 防止过氧化现象。 因此, 2, 6-二羟基萘的工艺合成研究不仅具有科研价值, 而且使2, 6-萘二磺酸钠变废为宝, 符合绿色化学的经济环保理念。
2, 6-萘二磺酸钠、氢氧化钠(纯度96%)、氢氧化钾(纯度96%)、抗氧剂1010、苯酚、粉末状活性炭、乙醇、甲醇等均为工业品(盐城市云峰化工有限公司)。
利用岛津LC-10AT型高效液相色谱(日本岛津制作所)检测产物中主产物及各个物质的组成, 使用面积归一法定量。检测条件:C18色谱柱(150 mm× 4.6 mm, 4.6 μ m), 流动相为乙腈和0.1%醋酸水溶液的混合物(体积比30∶ 70), 流速为1.0 mL/min, 进样量为10 μ L, SPD-10A VP Plus型紫外-可见检测器(日本岛津), 检测波长226 nm, 柱温35 ℃。 利用WRS-2型微机熔点仪(上海易测仪器设备有限公司)测定产品熔点。
在反应釜中加入30 g 96%氢氧化钠和15 g 98%氢氧化钾及10 mL蒸馏水, 搅拌加热至160 ℃左右, 逐渐加入33.2 g 2, 6-萘二磺酸钠(质量分数50%)及一定量的抗氧剂。 通N2气, 升温至反应温度, 常压下进行碱熔反应。 一定时间后, 降温至220 ℃, 出料至150 mL冰水中稀释。 降温后, 用硫酸中和至微酸性, 析出白色沉淀, 过滤, 滤饼用100 mL沸水溶解。 加入2 g活性炭搅拌脱色10 min, 热过滤, 滤液冷却15 ℃以下, 过滤, 真空干燥。 用高效液相色谱测定2, 6-二羟基萘的纯度, 计算收率。
碱熔收率/%=
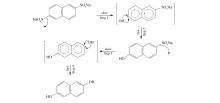
反应过程如Scheme 1所示。
为了进一步降低熔点, 加入一定量的水。 加入水另一优点在于, 反应前期, 加热温度高于100 ℃以后, 水会逐渐蒸发, 蒸发水汽会在反应釜上方去除大部分空气, 达到抗氧化的目的。 但是用水量不可过多, 水增加会使碱浓度降低, 不利于碱熔反应, 碱浓度越高越有利于碱熔进行[12]。
常压碱熔高温反应会发生繁多复杂的氧化副反应。 为避免副产物产生, 提高产品纯度, 本实验采用了反应前期使用水产生蒸汽隔绝空气, 并且反应中加入抗氧剂, 反应整个过程通N2气等一系列措施来降低及避免氧化副反应的进行, 否则焦油产生量很大。
有文献[13]中使用溶剂法制备其它二羟基萘, 例如导热油、氢化联苯等溶剂, 或者二苄基甲苯矿物油为溶剂。 本文重复溶剂法工艺表明, 由于反应生成焦油较多, 油水不易分层, 收率很低。 另外溶剂回收套用存在难度, 导致溶剂成本很高, 处理复杂, 产生大量污染。 因此, 溶剂法较难工业化。
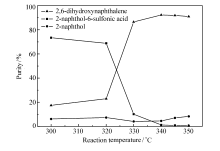
反应温度对产品的生成纯度影响最大。 反应产物除了目标产物2, 6-二羟基萘外, 主要有薛弗氏酸、2-萘酚、萘酚二聚物等, 当反应温度低于320 ℃时2, 6-二羟基萘生成量很少, 主要生成薛弗氏酸; 当反应温度为320330 ℃时, 2-萘酚生成较多; 反应温度逐渐升高时, 2, 6-二羟基萘产量逐渐升高, 当温度到350 ℃时, 2, 6-二羟基萘纯度开始降低, 副产物萘酚二聚物开始增加, 焦油大量生成, 过度氧化现象明显。 比较图2中各个结果可知, 温度控制在340350 ℃最好。
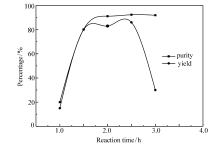
反应时间对产品纯度及收率的影响尤为重要。 当反应温度为340345 ℃时, 反应时间对产品纯度和收率的影响如图3所示。 产品纯度随着反应时间的增加显著增高, 当反应时间大于2 h时, 产品纯度的增加趋于平稳。 而产品收率更受制于反应时间的长短。 从图3可知, 反应时间为22.5 h时, 收率最高。 当反应温度大于2.5 h时收率急剧下降。 高温条件下反应, 反应时间越长越易产生繁杂的过氧化现象。 随着反应的进行, 碱浓度越来越低, 影响2, 6-二羟基萘的生成。 所以反应时间不易过长, 最佳反应时间段为22.5 h。
抗氧剂是阻止氧气氧化不良影响的物质。 本实验在其它条件不变的情况下, 尝试保险粉、氢醌、苯酚、抗氧剂1010等多种类型的抗氧化添加剂, 保险粉、氢醌对反应效果改善非常有限, 最终遴选出效果较好的苯酚和抗氧剂1010。 实验结果如图4、图5所示。
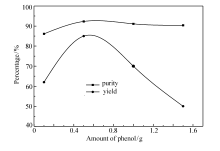 | 图4 不同用量苯酚对产品收率和纯度的影响Fig.4 Effect of different amount of phenol on the purity and yield of the product |
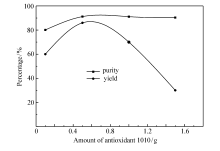 | 图5 不同用量抗氧剂1010对产品收率和纯度的影响Fig.5 Effect of different amount of antioxidant 1010 on the purity and yield of the product |
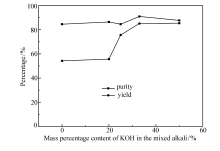
依据图4、图5可知, 苯酚和抗氧剂1010等添加剂的加入量直接影响产品的收率和纯度。 在0.5 g之前, 苯酚和抗氧剂1010加入量越多, 产品收率越高, 相对产品纯度也逐渐升高, 添加剂苯酚和受阻酚类抗氧剂1010起到有效的抗氧化保护作用。 当抗氧剂加入量大于0.5 g时, 随着苯酚和抗氧剂1010逐渐增加, 产品纯度没有明显变化, 但是产品收率显著降低。 当抗氧剂加入过多时形成自由基不仅未起到抗氧化的效果反而有助氧化等副反应的进行。 因此, 苯酚和抗氧剂1010的用量最优值为0.5 g。
萘环上磺酸基转化为羟基的反应是芳环上亲核取代反应。 本实验中亲核试剂为OH-, 离去基团为磺酸基, 芳环上亲核取代反应的慢步骤为磺酸基离去, 生成碳正离子; 然后亲核试剂快速进攻碳正离子; 第三步, 第二个磺酸基离去, 此步骤为关键性阶段, 需要较高活化能, 要求温度更高; 最后, 亲核试剂进攻碳正离子, 得到2, 6-二羟基萘。 要想优化反应条件, 实现低能快速路径, 提高转化率和收率, 寻找高效的离去反应催化剂成了必然的选择。 本实验中尝试添加水增加反应溶剂的质子性。 2, 6-萘二磺酸钠碱熔法制备2, 6-二羟基萘的可能反应机理见Scheme 2。
以NaOH、KOH和水为碱熔剂, 常压混合碱碱熔法一步反应由2, 6-萘二磺酸钠制取高纯度2, 6-二羟基萘, 反应时间短, 22.5 h, 较佳反应温度为340350 ℃。 通N2气, 添加适量苯酚或抗氧剂1010, 可提高产品纯度和收率, 碱熔收率为86.3%, 经过甲醇-水混合溶剂(体积比例为1∶ 2.5)精制提纯, 2, 6-二羟基萘纯度能达到99%, 熔点为214215 ℃。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|