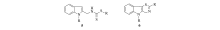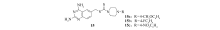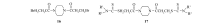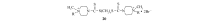氨基二硫代甲酸酯类化合物由于其独特的分子结构,使其具有明显的抗肿瘤、抗菌、抗氧化以及杀虫等多种生物活性,已经成为近年来药物化学领域研究的重点。 本文评述了近年来文献报道的氨基二硫代甲酸酯类化合物以及它们的主要生物活性,并对其今后的发展方向、应用前景做出展望。
Dithiocarbamate compounds have become the focus of pharmaceutical chemistry in recent years due to their unique molecular structure with a variety of biological properties, such as anti-tumor, antibacterium, antioxidation and insecticidal activity. This article reviews recent progresses in the biological activities of dithiocarbamate compounds and gives prospects for their development and application.
氨基二硫代甲酸酯类化合物(dithiocarbamates, DTCs)作为一类广泛存在的有机分子, 具有多种官能团和杂原子, 使其具有较强的金属键合能力, 能够有效地螯合重金属和清除体内NO自由基[1], 还可以作为单功能性诱导物, 选择性增强二相酶活性, 对生物系统产生深远的影响[2, 3]。 因此, 不同的DTCs衍生物表现出诸多生物学和药学等方面的特性, 例如不仅具有优秀的抗炎[4]、抗菌[5, 6]、抗氧化[7]、抑制心脏过度肥大[8]等活性, 最近还被报道为有效的抗癌药物和细胞凋亡的抑制剂。 由于该类化合物高效、低毒等特点目前已成为药物化学领域研究的热点。 本文评述了近年来文献报道的氨基二硫代甲酸酯类化合物及其主要生物活性, 包括抗肿瘤、抗菌、抗结核杆菌以及对放射性药物的组织缺氧成像能力等, 并对其今后的发展方向做出展望。
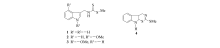
广泛存在于花椰菜、甘蓝菜、萝卜和白菜等十字花科蔬菜中的吲哚氨基二硫代甲酸酯类化合物, 已经证明能够有效地抑制肺癌、结肠癌、乳腺癌的形成, 是该类食物防癌抗癌作用的关键成分。 主要代表性的化合物包括:Brassinin(1, 吲哚碱类氨基二硫代甲酸酯)、1-Methoxybrassinin(2, 1-甲氧基吲哚碱类氨基二硫代甲酸酯), 4-Methoxybrassinin(3, 4-甲氧基吲哚碱类氨基二硫代甲酸酯)和Cyclobrassinin(4, 吲哚碱类环状氨基二硫代甲酸酯)(Scheme 1)[9]。 其中化合物1和4, 能够有效地阻止乳腺癌和白血病的前期形成, 调节动物模型中的化疗预防活动, 是一种有效地化学防癌抗癌化合物[10, 11]。 该类化合物之所以具有防癌、抗癌活性, 一方面, 它们不仅可以降低致癌物质的活性, 降低癌症的发生率, 还可以增强机体对致癌物质的抵抗能力; 另一方面它们能够有效地诱导第二相解毒酶, 提高酶的活性, 阻断许多致癌物(例如亚硝胺等)的肿瘤诱导作用, 减缓肿瘤细胞的生长速度。
最近一些研究表明, 吲哚胺酶— — 2, 3-二氧酶 (indole amine 2, 3-dioxygenase, IDO)在抑制肿瘤免疫反应中表现出一定的作用。 因此, 人们开始专注于识别新的、潜在的IDO抑制剂作为癌症治疗的新方法。 为了寻找新的IDO抑制剂, 不同的吲哚碱基分子被筛选, 有趣的是, 发现天然产物Brassinin(1, Scheme 1)具有中等的抑制活性[12]。 这些发现, 进一步促使将它们作为先导化合物制备各种其类似物并进行抗肿瘤活性研究。
Pé ter课题组在成功合成Brassinin、Cyclobrassinin和它们衍生物的基础上, 2006年报道了Brassinin的位置异构体Isobrassinin(5)和Cyclobrassinin异构体Isocyclobrassinin(6, Scheme 2)的合成, 并评价了它们对宫颈癌、乳腺癌和肺癌等肿瘤细胞的抑制作用, 发现当R=Me和Bz时, 化合物5对肿瘤细胞抑制作用要远远高于Brassinin; 当R=Ph时, 同等浓度条件下, 化合物6对宫颈癌和乳腺癌具有非常优秀的抑制作用, 被证明也是一类新型的抗肿瘤细胞增殖剂[13]。
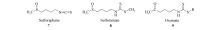
同样从十字花科植物中发现的脂肪族异硫氰酸酯— — Sulforaphane(7, 萝卜硫素, Scheme 3)[14]与吲哚碱的氨基二硫代甲酸酯— — Brassinin(1, Scheme 1)均能选择性地增强二相酶活性, 被证明具有很好的化学防癌作用。 Gerhä user等将化合物Sulforaphane的甲基亚砜正丁烷部分与Brassinin的氨基二硫代甲酸酯部分相拼合, 设计合成了Sulforamate(8, Scheme 3)[15]。 药理实验表明, Sulforamate的活性较Sulforaphane提高了两倍而毒性却降低了2/3, 是一种非常具有潜在研究价值的化学防癌化合物[16]。
Hirschelman课题组研究发现, 将Sulforamate结构中甲基亚砜替换为甲基酮基, 即Oxomate(9), 也是一种潜在的二级酶诱导剂, 可用做化学防癌药物使用[17, 18, 19]。
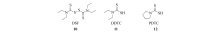
双硫仑(Disulfiram, DSF, 10, Scheme 4)作为一种不可逆转的醛基脱氢酶抑制剂, 是被FDA批准用作治疗酒精中毒的两个药物之一, 临床试验也验证了DSF的生物活性, 并发现该化合物没有毒性[20]。 最近Dou等研究表明, DSF与铜的配合物, 能够通过抑制蛋白酶活性诱导乳腺癌细胞等肿瘤细胞凋亡[21]。 同时, 临床也验证二乙基二硫代氨基甲酸(diethyldithiocarbamate, DDTC(11, Scheme 4)被用于HIV-1感染的病人, 能够延迟AIDS的发病过程[22]。 研究结果表明, 该类化合物除了能够使致癌物质活性降低, 增加二相解毒酶— — 谷胱甘肽S-转移酶和UDP葡萄糖醛酸转移酶的含量外, DDTC还能够作为烷化剂, 清除体内形成的致癌物质或者类似致癌物质。
吡咯烷二硫代氨基甲酸(pyrrolidine dithiocarbamate, PDTC)(12, Scheme 4)作为一种稳定的氨基二硫代甲酸酯的吡咯烷衍生物, 是一种可以通透细胞膜的NF-κ B活化抑制剂, 可以在多种细胞中抑制NF-κ B的激活。 在细胞毒研究中, PDTC常被用作抗氧化剂和金属离子螯合剂, 可以诱导大鼠平滑肌细胞发生凋亡, 也可以抑制白血病细胞HL-60发生凋亡[23]。 另有文献报道[24], PDTC的毒性直接与可利用的金属离子, 例如铜、锌等相关。 除此之外, 有文献报道[25], PDTC除了可以抑制紫外线诱导细胞凋亡, 也能够减少由细胞毒性药物诱导细胞凋亡的范围。
2005年, Cao等[26, 27]设计合成了一系列在2-甲基-4(3H)-喹唑啉酮的6位连有不同氨基二硫代甲酸酯侧链的化合物13(Scheme 5), 并发现当化合物13中胺基为不同的哌嗪基时, 对白血病K562细胞株具有较好的抑制作用, 其中4-对氟苯基哌嗪基取代的化合物13a活性最强(IC50=0.5 μ mol/L)。
为了进一步研究含喹唑啉酮结构的氨基二硫代甲酸酯类化合物, 2010年, Cao等[28]在化合物13的结构基础上, 将原来的喹啉酮的二硫代甲酸酯部分进行结构改造, 合成一系列化合物14(Scheme 5), 但抗肿瘤活性研究结果表明, 除了R为乙炔基(14a, Scheme 5)外, 其余大部分化合物的抗肿瘤活性较化合物13明显降低。
2013年, Cao等[29]根据化合物13的构效关系特点, 用2, 4-二氨基喹唑啉替代化合物13中2-甲基-4(3H)-喹唑啉酮单元, 合成了一系列4-苯基哌嗪基取代的化合物15(Scheme 6), 发现该类化合物对人肺癌(A549)、乳腺癌(MCF-7)、宫颈癌(HeLa)和结肠腺癌(HT29, HCT-116)肿瘤细胞均具有优秀的细胞毒活性(IC50=1.4711.83 μ mol/L), 特别是当R为对甲氧基苯基、对氟苯基、对硝基苯基(15a, 15b, 15c, Scheme 6)时, 对被测的5种肿瘤细胞的抑制活性最强(16a IC50=1.582.27 μ mol/L; 16b IC50=1.843.27 μ mol/L; 16c IC50=1.474.6 8 μ mol/L)。
1, 4-二(3-溴丙酰基)哌嗪16(Scheme 7)是一种烷化剂类抗血液病药, 它对血小板增多症, 红细胞增多症和慢性粒细胞白血病有明显治疗作用, 但由于毒性较大已被淘汰。 Guo等[30]对化合物16进行结构改造, 合成了1, 4-二[3-(氨基硫代甲酰硫基)丙酰基]哌嗪类化合物17(Scheme 7), 并进行抗癌活性对比实验, 以期获得低毒高效的药用化合物。 体外抗肿瘤实验结果表明该类化合物对白血病细胞具有很好的选择性, 与仲胺相比, 多数伯胺形成的化合物具有更强的抗白血病活性。
同时该课题组还合成了另一类哌嗪基二硫代甲酸酯类化合物— — 4-甲基哌嗪-1-二硫代甲酸-(3-氰基-3, 3-二苯基)丙酯盐酸盐(18, TM208, Scheme 8), 该化合物虽然没有明显的体外抗肿瘤活性, 但体内抗肿瘤活性很强, 体内实验结果显示, 连续灌胃给药后, 化合物18对小鼠移植性肿瘤S180、H22、异种移植肿瘤BGC生长均有明显的抑制作用, 且几乎无毒性[31, 32, 33]。 因此, 该课题组[34, 35]以化合物18为先导化合物, 又合成了一系列N-连有不同取代基的衍生物(19, Scheme 8), 发现当R=H时, 化合物活性明显好于先导化合物18, 但是在氮原子上引入大体积取代基, 会严重影响的它们的抗肿瘤活性。 作为一类结构新颖、抗肿瘤作用强、毒性反应小的氨基二硫代甲酸酯类化合物, 该类化合物有望成为一种新的抗肿瘤药物。
除此之外, 该课题组[36]还合成一些别的哌嗪基二硫代甲酸酯类化合物, 例如, 哌嗪盐化合物20(Scheme 9), 并发现该类化合物具有显著镇痛作用。
沙利度胺(21, Scheme 10), 1950年已经被注册用于治疗失眠和呕吐, 目前仍被用于麻风病、类风湿关节炎和移植物抗宿主病(GVHD)等引起的疼痛炎症。 为了寻找具有抗肿瘤活性的新化合物, Zahran等[37]合成了一系列含沙利度胺结构的氨基二硫代氨基甲酸酯类化合物(22, Scheme 10), 并评价了这些化合物的抗肿瘤活性、脂质过氧化、抗氧化、细胞凋亡、坏死, 抗有丝分裂、抗细胞增殖和抗血管生成等活性, 以及对瑞士白化小鼠的反应停作用和对由艾氏腹水瘤诱导的小鼠实体瘤的抑制作用。
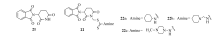 | Scheme 10 Dithiocarbamates containing thalidomide |
其中化合物22a和22c不仅对艾氏腹水癌细胞(EAC cells)表现出优秀的抑制活性((95.2± 3.3)%, (100± 0.0)%, c=10 mmol/L, 30 μ L)), 且对肝脏没有毒副作用, 但是用化合物23b处理小鼠, 能导致肝脏变性。 另外, 根据研究结果, 该课题组还推测该类化合物有可能通过抗氧化途径诱导自由基减少和抗氧化酶增加, 从而抑制肿瘤增殖。
以1, 3-二苯基丙烯酮为基本骨架结构的查尔酮类化合物, 是多种药用植物的有效成分, 具有广泛的生物学活性。2010年, Qian等[38]设计并合成了一系列含有查尔酮结构的氨基二硫代甲酸酯类化合物23(Scheme 11), 并评价了它们作为抗增殖剂和微管蛋白抑制剂的活性。 其中化合物23a不仅表现出最强的体外抗肿瘤活性(IC50=0.04 μ mol/L, MCF-7), 对微血管也表现出较强的抑制作用(IC50=6.8 μ mol/L)。
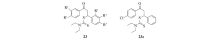 | Scheme 11 Dithiocarbamates containing chalcone scaffold |
黄酮类化合物作为一类植物次生代谢物, 其生理生化功能同样是天然产物研究的重点。 Huang等[39]将黄酮母核和氨基二硫代甲酸酯单元结合, 设计合成了一系列不同取代的含黄酮母核的氨基二硫代甲酸酯化合物(24, 25, 26, 27, Scheme 12), 并研究了他们的抗肿瘤活性。 构效关系研究结构表明, DTC取代在类黄酮2位的化合物25抗肿瘤活性明显优于其余位点取代的化合物, 其中化合物24a和24b(Scheme 12)由于优秀和广谱的抗肿瘤活性, 被认为是最具有活力的候选化合物。
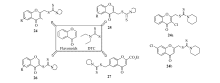 | Scheme 12 Dithiocarbamate containing chromones |
2012年, Bacharaju等[40]报道用一系列含苯并咪唑结构的氨基二硫代甲酸酯化合物28(Scheme 13), 活性评价表明虽然该类化合物的抗有丝分裂能力(IC50=1.662.29 μ mol/L)略小于顺铂(IC50=1.21 μ mol/L), 但毒性相对顺铂较小, 有望成为一类新型的抗有丝分裂试剂。
 | Scheme 13 Dithiocarbamates containing benzimidazole |
γ -丁烯内酯又叫2(5H)-呋喃酮, 是一类广泛存在于天然产物中的重要化学单元, 大部分该类化合物都表现出抗真菌、抗细菌、抗病毒和抗肿瘤等生物活性。 2011年, Wang等完成了完成了γ -丁烯内酯C-3, C-4位被不同氨基二硫代甲酸酯链取代的化合物29和30(Scheme 14)的合成, 通过抗肿瘤活性评价及构效关系研究发现, C-3位被氨基二硫代甲酸酯链取代的化合物29抗肿瘤活性明显优于C-4位取代产物30, 其中C-3位苄胺基二硫代甲酸酯取代的化合物29a29d活性最为突出, 对人前列腺癌细胞(PC-3)和人宫颈癌细胞(HeLa)等均有较好的抑制活性(IC50< 10 μ mol/L), 而且该类化合物对小鼠S180实体瘤抑瘤率与5-Fu相当, 毒性却明显小于5-Fu[41, 42]。
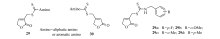 | Scheme 14 Dithiocarbamates containing butenolide |
2013年, Duan等[43, 44, 45, 46]报道了一系列含1, 2, 3-三氮唑结构的氨基二硫代甲酸酯类化合物的合成及抗肿瘤活性研究。 发现化合物31(Scheme 15)表现出广谱的抗肿瘤活性, 特别是当R为o-F和o-Cl时, 化合物31a和31b对被测的4种细胞株(MGC-803, MCF-7, SMMC-7721, EC-9706)的IC50值分别为0.7311.61 μ mol/L和0.4912.45 μ mol/L, 明显优于阳性对照药5-氟尿嘧啶。 另外, 流式细胞仪分析表明, 化合物31b与人胃癌细胞MGC-803作用, 能够使细胞周期阻滞在G2/M期, 从而导致胃癌细胞凋亡。
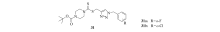 | Scheme 15 Dithiocarbamates containing 1, 2, 3-triazole |
β -内酰胺结构具有较好的抗菌活性, 特别是3-位有噻唑环的β -内酰胺抗菌剂32(Scheme 16 )。 Ohtake等[47]将化合物32中噻唑结构变为氨基二硫代甲酸酯结构(33, Scheme 16), 合成了一系列该类化合物并评价了它们的抗菌活性, 发现化合物33a和33b对金黄色葡萄球菌和上皮葡萄球菌等表现出明显优于万古霉素的活性。
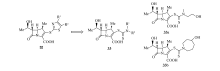 | Scheme 16 Dithiocarbamates containing β -lactams |
近年来, 小分子介导的微生物群体感应调节受到广泛关注, 其中N-酰化高丝氨酸内酯类化合物(OdDHL, Scheme 17)是菌群感应系统中最重要的一类信号分子, 能够调控许多生理特性的表达, 是目前研究的热点。 2013年, Liu等[48]报道了含高丝氨酸内酯结构的氨基二硫代甲酸酯类化合物34, 35(Scheme 17), 其中化合物34系列化合物对革兰氏阳性菌表现较好的抑制作用(例如R=— CF3, MIC50=1.443 μ g/mL), 而化合物35系列化合物除了n为0和1时, 对绿脓杆菌和大肠杆菌等革兰氏阴性菌表现出中等的抑制活性外, 其余化合物抗菌活性并不明显。
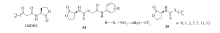 | Scheme 17 Dithiocarbamates as analogs of AHL |
康唑类药物, 例如, 氟康唑, 伏立康唑, 是目前临床上最有效的抗真菌药物。 然而, 该类药物由于毒性和耐药性等问题, 一定程度上限制了其临床应用。 2014年, Zou等[49]根据康唑类化合物的结构特点, 设计合成了一系列含氨基二硫代甲酸酯链的化合物(36, Scheme 18), 并考察了它们的体外抗真菌活性。 结果显示, 氨基二硫代甲酸酯侧链的引进能够有效的增加对该类化合物除曲霉菌以外大多数测试真菌的抑制活性, 特别是对念珠菌的抑制活性最好。 通过改变化合物36中的氨基, 发现二级胺比一级胺抗真菌活性普遍要好, 特别是当氨基为不同苯基取代的哌嗪基时, 抗真菌活性最好, 大部分活性优于对照药氟康唑和酮康唑。
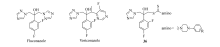 | Scheme 18 Dithiocarbamates containing triazoles moiety |
氨基糖苷类药物是一类抗菌谱广、应用广泛的一类抗生素, 例如链霉素是治疗肺结核的主要药物之一。 为了寻找新的抗结核分支杆菌药物, Horita等[50]分别以氨基葡萄糖, 氨基甘露糖和氨基半乳糖为原料, 合成了一些含糖环的氨基二硫代甲酸酯化合物(3740, Scheme 19), 并评价它们的抗结核杆菌活性, 其中化合物37对结核杆菌表现出较好的抑制作用, 构效关系研究表明, 二甲氨基二硫代甲酸酯取代在糖环1-位是影响活性的关键因素。
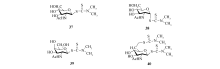 | Scheme 19 Dithiocarbamates containing aminosugar |
Gü zel等[51]合成了一系列含邻苯甲酰磺酰亚胺结构的氨基二硫代氨基甲酸酯类化合物41(Scheme 20), 并评价了它们的体外抗结核活性。 结果表明, 大部分该类化合物均能表现出优秀抗结核活性, 是一类潜在的抗结核药物。 另外, 该类化合物对白血病、卵巢癌和肺癌等也表现出较好的抑制作用。
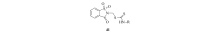 | Scheme 20 Dithiocarbamates containing saccharin |
2-甲基-5-硝基咪唑-1-乙醇(甲硝唑)(42, Scheme 21), 临床主要用于预防和治疗厌氧菌引起的感染, 另外, 它还是治疗多种疾病的神奇多面手, 比如治疗酒糟鼻、疥疮、银屑病等。最近有文献报道, 甲硝唑能够对缺氧的肿瘤细胞有放射敏感作用, 被选做制备放射性药物。 Giglio等[52]以甲硝唑(42)为母核, 合成了两个氨基二硫代甲酸钠配体— — 化合物43和44(Scheme 21), 将其制备成锝配合物并评价了它们潜在的放射性药物的缺氧组织成像能力, 发现化合物43与锝的配合物能有效地使放射性药物成像。
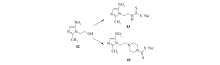 | Scheme 21 Dithiocarbamates containing 5-nitroimidazole |
氨基二硫代甲酸酯类化合物由于其独特的分子结构、丰富多样的生物活性以及较简单的合成方法, 特别是近些年来, 作为有效的化学防癌、抗癌化合物已经成为药物化学领域研究的热点之一。 但是关于该类化合物防癌、抗癌等生物活性的作用机制报道较少, 作用机理还不十分明确。 进一步明确该类化合物的作用机制, 进而指导设计、合成毒副作用小、活性作用强的新型先导化合物, 将是该领域今后研究的主要目标。 相信随着研究的不断深入, 作用机制会更加明确, 新的具有更高生物活性的氨基二硫代甲酸酯类化合物必将进一步被发现, 它们在现代药物化学中的应用必将进一步丰富和加强。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|
| [49] |
|
| [50] |
|
| [51] |
|
| [52] |
|