Suzuki偶联反应是构筑碳-碳单键的重要方法之一。 继有机硼酸后,有机三氟硼酸盐成为一种理想的、具有研究意义和使用价值的有机硼亲核试剂。 本文系统地综述了有机三氟硼酸钾参与的Suzuki偶联反应研究进展并对其研究前景进行了展望。
Suzuki coupling reaction is one of the most important methods to construct carbon-carbon bond. Recently, potassium organotrifluoroborate salts have emerged as an attractive and promising alternative to organoboronic acids. This article reviews the research progress in the Suzuki coupling reaction of potassium organotrifluoroborates and gives an outlook on the future research direction.
Suzuki偶联反应是指钯(0)催化下, 卤代烃、卤代芳烃或者烯基卤与有机硼试剂之间的反应[1]。 它是由日本北海道大学的Akira Suzuki教授首次发现, 并因此而得名。 有机硼试剂除具有操作简单、易于合成、稳定性好、官能团的兼容性强等特点外, 有机硼试剂及其副产物还具有毒性低, 对环境友好等特点。 因此, Suzuki偶联反应一直是构建碳-碳单键最重要方法之一, 已广泛应用于药物及其中间体、功能材料的合成中[2, 3]。
在Suzuki偶联反应中, 所使用的有机硼亲核试剂主要包括芳基硼酸、有机三氟硼酸钾、芳基硼酸新戊二醇酯和芳基硼酸频呐醇酯。 对于这4种亲核试剂的反应活性, Percec小组进行了系统的研究[4]。 他们发现, 在Ni的催化下, 在以ArOMs或ArOSO2NMe2作为亲电试剂的反应中, 4种有机硼亲核试剂表现出反应活性的差异。 芳基硼酸是最活泼且最具有原子经济性的有机硼试剂。 在水的存在下, 有机三氟硼酸钾则比相应的硼酸酯表现出更好的反应活性。 与芳基硼酸频呐醇酯相比, 芳基硼酸新戊二醇酯是具有较高原子经济性的试剂, 它价格较便宜, 活性较高。
近30年来, 人们在芳基硼酸参与的Suzuki反应中付出了极大的努力, 发展出多种多样的催化体系, 取得了一系列研究成果。 尽管如此, 芳基硼酸作为有机硼试剂却存在明显的不足和缺点[5]:1)硼酸常常不是单一物种, 而是以二聚或三聚酸酐的形式存在(Eq.1)。 虽然此特点对水相中Suzuki偶联反应没有太大影响, 但是却导致了硼酸纯化的困难。 因此, 大多数硼酸并非以晶体或自由粉末状固体存在, 而是以蜡状固体的形式存在; 2)硼酸容易发生自身偶联副反应, 在硼酸参与的Suzuki偶联反应中, 往往需要加入过量的硼酸(20%50%); 3)在有机合成中, 硼酸常常对一些常规合成条件敏感, 不能存在于底物结构的修饰中, 因此大大限制了Suzuki偶联反应在构建复杂分子中的应用。
人们于1960年认识有机三氟硼酸盐[6]。 直到1995年, 在Vedejs等[7]报道了此类物质的合成后, 它们才在Suzuki偶联反应中得到应用。 此后, 基于不同原料的多种合成方法被报道[8, 9, 10], 主要包括:1)三取代的有机硼试剂(RBY2)均可以KHF2为氟化剂高产率的转化为有机三氟硼酸钾(Eq.2); 2)以卤代烃等为起始原料, 格式试剂或锂试剂均可与B(OR)3发生反应, 进而转化为有机三氟硼酸盐(Eq.3); 3)烯烃或炔烃先发生硼氢化反应, 随后与KHF2反应转化为有机三氟硼酸钾(Eq.4)。
研究表明, 有机三氟硼酸盐能够克服有机硼酸的缺点, 正逐渐成为一种理想的、具有研究意义和使用价值的有机硼亲核试剂[8, 9]。 它们的优点主要表现在:1)易于制备, 纯化简单; 2)稳定性好, 易于操作; 3)不易发生自身偶联反应。 此特点减少了有机三氟硼酸钾在反应中的用量(11.2化学计量), 提高了原料的利用率; 4)可以承受多种常规有机反应条件, 如氧化反应、还原氨化反应、取代反应、缩合反应、1, 3-环加成等, 可以在保证C-C键合成不受影响的前提下对简单底物进行结构修饰。 尽管如此, 关于有机三氟硼酸盐在Suzuki偶联反应中的研究却显得不足。
1996年Genê t小组[11]报道了有机三氟硼酸钾作为亲核试剂在Suzuki偶联反应中的应用后, 有机三氟硼酸钾参与的Suzuki偶联反应才逐渐引起了研究者的兴趣。 研究发现, 除芳基三氟硼酸钾可参与Suzuki偶联反应外, 各种杂环取代的三氟硼酸钾、烯基三氟硼酸钾以及烷基三氟硼酸钾均可作为亲核试剂参与反应。 亲电试剂种类也从最初的芳基重氮四氟硼酸钾(ArN2BF4)扩展到卤代(杂环)芳烃、烯丙基卤素、ArOTf、ArOMs和ArOTs等。 文献报道的相关催化体系主要分为三类。 第一类是简单催化体系。 在此类催化体系中, 不需要任何配体的参与, 仅需要简单钯盐作为催化剂。 第二类是有配体参与的反应, 在所使用的配体中, 主要是含氮、含磷配体或者基于P, N的配体。 第三类催化体系是采用微波加热方法。 本文从以上3个方面分别展开。
1996年, Genê t课题组报道了芳基重氮四氟硼酸钾(ArN2BF4)与芳基或烯丙基三氟硼酸钾的Suzuki偶联反应(Eq.5)[11, 12, 13]。 此研究开创了有机三氟硼酸盐在Suzuki偶联反应中的应用先例。
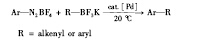 |
1999年, Chen Zhen-Chu小组报道了芳基碘鎓盐(ArI+Ar'B
2002年, Molander小组报道了芳基三氟硼酸钾与溴代芳烃的Suzuki偶联反应(Eq.6)[15, 16]。 研究发现, 以Pd(OAc)2为催化剂, 以MeOH为溶剂, 以K2CO3为碱, 各种不同取代的溴代芳烃均能顺利发生反应, 并获得较高产率。 如果底物中含有— OH或— COOH, 反应可以在纯水中进行。
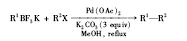 (6) (6) |
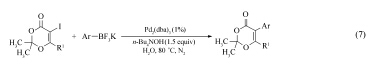
2010年, Stefani课题组报道了5-碘-1, 3-二恶英-4-酮与芳基三氟硼酸钾的Suzuki偶联反应, 为合成α -芳基-β -酮酯提供了一种新方法(Eq.7)[17]。 研究发现, 以纯水为反应介质, 以Pd2(dba)3为催化剂, 以n-Bu4NOH为碱, 5-碘-1, 3-二恶英4-酮可与各种芳基三氟硼酸钾发生反应。 美中不足的是, 该方法不适用于溴代底物的偶联。 当5-溴-1, 3-二恶英-4-酮参与反应时, 目标产物的产率仅为35%。 此外, 该方法操作比较繁琐, 整个反应需要在N2气的保护下进行。
最近, 我们课题组发现, 以水/聚乙二醇为反应介质, 以Pd(OAc)2为催化剂, 以Na2CO3为碱, 含有各种不同取代基的溴代芳烃均可顺利与芳基三氟硼酸钾发生反应并给出较高产率。 研究还发现, 此催化体系同样适用于溴代杂环芳烃的Suzuki偶联反应。 值得一提的是, 此催化体系可循环使用8次, 产率未见明显降低[18]。
较为简单的催化体系主要有
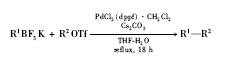
Molandar研究小组在三氟硼酸钾参与的Suzuki偶联反应的研究中做出了重大贡献。 除了发展出Pd(OAc)2/MeOH/K2CO3的催化体系外, 该小组还发展出其它一些催化体系, 这些催化体系需要配体的参与。 2001年, 该小组首次报道了芳基或烯丙基三氟甲磺酸酯作为亲电试剂与有机三氟硼酸钾的Suzuki偶联反应(Eq.8)[19]。 研究发现以THF/H2O为反应溶剂, 以Cs2CO3为碱, PdCl2(dppf)· CH2Cl2能有效的促进反应进行。
 (8) (8) |
2002年, 该课题组又发现, 以PdCl2(dppf)· CH2Cl2为催化剂, 以正丙醇为溶剂, 以NEt3为碱, 卤代芳烃、烯丙基卤素均能与烯基三氟硼酸钾发生反应(Eq.9)[16, 20]。 此研究扩大了有机三氟硼酸钾在Suzuki偶联反应中的应用范围。
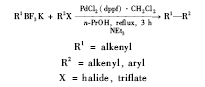 (9) (9) |
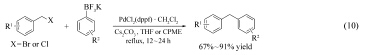
2006年, Molander等[21]报道了苄卤与芳基三氟硼酸盐的Suzuki偶联反应。 以THF或CPME的水溶液为反应介质, PdCl2(dppf)· CH2Cl2能有效的催化此反应的进行(Eq.10)。
除三氟硼酸钾盐能参与Suzuki偶联反应外, 2001年, Batey等报道了芳基三氟硼酸四烷基铵盐的合成方法, 并研究了它们在Suzuki偶联反应中的应用(Eq.11)。 研究发现, 以Pd(OAc)2为催化剂, 以dppb为配体, 各种不同取代的三氟硼酸盐均可与卤代芳烃发生反应[21]。
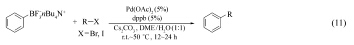
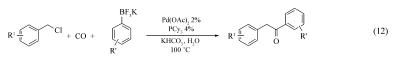
2011年, Neumann等[23]基于芳基三氟硼酸钾较强的亲核性, 以此代替相应硼酸报道了Pd(OAc)2/PCy3催化下的苄氯的加羰偶联反应(Eq.12), 取得了较高的产率。
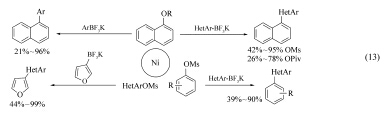
此外, 2011年Molander等[24]报道了Ni(COD)2(10%)催化下芳基三氟硼酸钾参与的Suzuki偶联反应(Eq.13)。 以PCy3HBF4(20%)为配体, 在K3PO4(7.2化学计量)的存在下, 各种不同种类的三氟硼酸钾均能顺利地发生反应。
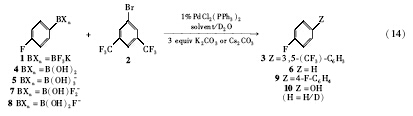
2010年, Lloyd-Jones小组[25]以对氟苯基三氟硼酸钾与3, 5-二(三氟甲基)溴苯的反应为模板反应, 以PdCl2(PPh3)2为催化剂, 在甲苯/水和THF/H2O介质中, 研究了有机三氟硼酸钾Suzuki偶联反应的机理(Eq.14)。 他们的研究表明, 以THF/H2O(体积比10∶ 1)为反应介质, 可以高产率的获得产物(> 95%), 副反应很少。而当以甲苯/水(体积比3∶ 1)为反应介质时, 仅有少量产物生成(≤ 32%), 而有55%的三氟硼酸钾转化为副产物6。 他们还发现, 有机三氟硼酸钾在THF/H2O中可发生原位水解, 生成相应的硼酸, 进而发生反应。 水的比例对有机三氟硼酸钾的两种水解产物(4和5)的含量有很大影响。 有机三氟硼酸钾作为亲核试剂比有机硼酸更高效, 主要不是表现在反应速率上, 而是体现在有机三氟硼酸钾能有效的防止去硼加氢、自身偶联等副反应的发生。
 |
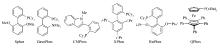
较为复杂催化体系大多以Pd(OAc)2为催化剂前体, 采用结构复杂的配体, 结构如图1所示。 这些配体如SPhos[26, 27, 28]、CMPhos[29]、DavePhos[30]、XPhos[31, 32]、RuPhos[33, 34, 35]等均能有效的促进有机三氟硼酸钾的Suzuki偶联反应。
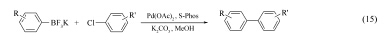
2004年, Buchwald课题组[26]发现, 以MeOH为溶剂, 以K2CO3为碱, Pd(OAc)2/S-Phos能有效的催化芳基三氟硼酸钾与氯苯的Suzuki偶联反应, 并获得了理想产率(Eq.15)。 这是首个催化芳基三氟硼酸钾与氯苯Suzuki偶联反应的催化体系。
2007年, 复旦大学吴劼课题组[27]发现, 以Pd(OAc)2为催化剂, 在S-Phos的存在下, 各种不同取代的ArOTs均可顺利地与芳基三氟硼酸钾发生反应(Eq.16)。

2012年, 郑州大学邹大鹏、吴豫生等[28]发现, Pd(OAc)2/SPhos还能有效催化2-吡啶三氟硼酸钾与卤代杂环芳烃的Suzuki偶联反应。
2010年, Kwong小组[29]发现以Pd-CM-phos为催化剂, 以t-BuOH为溶剂, 以K3PO4为碱, 芳基或杂环取代的甲基磺酸盐可与多种有机三氟硼酸盐反应Suzuki偶联反应(Eq.17)。

2009年, 该小组[30]报道了一系列噁唑啉取代的芳基三氟硼酸钾的合成。 并以此作为亲核试剂研究了它们在Suzuki偶联反应中的应用, 为合成噁唑啉取代的三芳环化合物提供了一种有效的方法(Eq.18)。
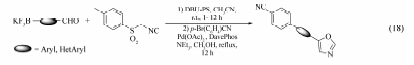
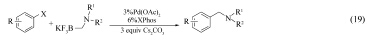
2008年, Molander小组[31]报道了以Pd(OAc)2为催化剂前体, 以XPhos为配体的催化体系(Eq.19)。 研究发现, 在THF/H2O中, 以Cs2CO3为碱, ArCl、ArI和ArOTf均可与有机三氟硼酸钾反应, 高产率的获得N, N-二烷基苄胺类化合物。 此后, 该小组又发现, Pd(OAc)2/XPhos还能有效的催化ArCl与环丙烷基三氟硼酸钾的Suzuki偶联反应[32]。
同年, 该小组[33]成功的制备出了含有酮、酯和酰胺的有机三氟硼酸钾, 并以Pd(OAc)2/RuPhos为催化体系, 以K2CO3为碱, 实现了这些有机三氟硼酸钾与卤代芳烃的Suzuki偶联反应(Eq.20)。

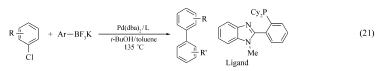
2012年, Kwong小组[36]发现基于苯并咪唑的含膦配体能够有效的促进氯代芳烃包括氯代杂环芳烃与芳基三氟硼酸钾盐的Suzuki偶联反应(Eq.21)。 反应条件为以Pd(dba)2为钯源, 以t-BuOH/toluene为溶剂, 以K3PO4· H2O为碱, N2气保护下, 反应温度为135 ℃, 反应时间为24 h。 研究发现, 各种不同的氯代芳烃均能给出较高产率(79%99%)。
此外, 还有一些环钯催化剂应用其中。 2008年, Né jera等[37]发现基于肟的环钯催化剂能有效的促进芳基三氟硼酸盐与氯苯的Suzuki偶联反应(Eq.22)。 在四丁基溴化铵(TBAB)的存在下, 以水为反应溶剂, 以K2CO3为碱, 不管是传统加热或是微波加热, 该催化剂均能有效的促进氯苯的Suzuki偶联反应。 苯基三氟硼酸钾上取代基的电子效应对反应产率有较大影响。 研究还表明, 在丙酮的水溶液中, 该催化剂还能有效的促进苯基三氟硼酸钾与烯丙基氯和苄氯的Suzuki偶联反应。 值得一提的是, 该催化剂可以循环使用3次。
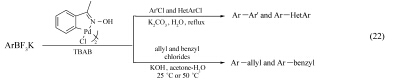
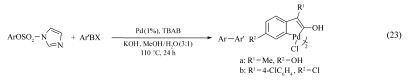
2011年, Né jera等[38]报道了芳基咪唑磺酸酯与三氟硼酸盐的Suzuki偶联反应, 为合成芳基-芳基化合物提供了一种新方法(Eq.23)。 他们的研究发现, 与相应的硼酸相比, 三氟硼酸盐表现出较低的反应活性。
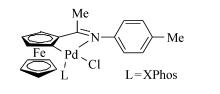
2011年, 郑州大学邹大鹏等[39]发展了一种新型催化剂(图2), 它能有效的催化卤代芳烃或卤代杂环芳烃与有机三氟硼酸钾的Suzuki偶联反应。
此外, 纳米钯也可用于催化芳基三氟硼酸钾的Suzuki偶联反应。 2012年, Cacchi等[40]报道了alginate/gellan稳定下的纳米钯催化的芳基重氮四氟硼酸盐与芳基三氟硼酸钾的Suzuki偶联反应。 同年, Masuyama等[41]通过离子交换法制备出了羟基磷灰石负载的钯催化剂(PdHAP), 并在MeOH中, 以K2CO3为碱, 以PPh3为配体, 顺利地促进了溴代芳烃与芳基三氟硼酸钾之间的Suzuki偶联反应。
近几年, 微波加热作为一种加热方法广泛地应用于有机反应中。 它不仅能够加速化学反应, 而且可以使某些在传统加热条件下不能发生的反应得以实现。 同样, 在有机三氟硼酸钾参与的Suzuki偶联反应中, 微波作为加热方法也引起了研究者的较多关注。
2005年, Kabalka小组[42]首次将微波加热引入到芳基三氟硼酸钾与碘代芳烃的Suzuki偶联反应中(Eq.24)。 研究发现, 以PdCl2(dppf)· CH2Cl2为催化剂, 以i-Pr2NEt为碱, 以异丙醇/水为混合溶剂, 各种取代的碘代芳烃均可与芳基三氟硼酸钾发生反应, 产率为50%100%。
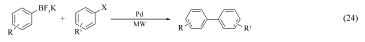
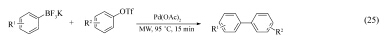
2006年, 该小组[43]又发现, 在微波加热下, 以乙醇/水为介质, Pd(OAc)2能有效催化芳基三氟甲基磺酸酯与芳基三氟硼酸钾的Suzuki偶联反应(Eq.25)。该体系中不需要任何碱和配体的参与。
2006年, Leadbeater小组[44]报道了微波促进下卤代芳烃与芳基三氟硼酸钾的Suzuki偶联反应(Eq.26)。 研究发现, 以EtOH/H2O为反应溶剂, 以Na2CO3为碱, 以TBAB为相转移催化剂, 钯(2.5× 10-6)能很好的催化溴代芳烃或碘代芳烃与有机三氟硼酸钾的Suzuki偶联反应。
 |
2007年, Crouch小组[45]同样利用微波作为加热手段, 发展了促进溴代芳烃与芳基三氟硼酸钾Suzuki偶联反应的催化体系。 该体系以PdCl2为催化剂, 以MeOH为溶剂, 以K2CO3为碱, 目标产物产率为43%99%。 研究发现, 水的存在能够促进反应的进行。
总之, 有机三氟硼酸钾正逐渐成为一种具有研究意义的亲核试剂。 由于具有易于制备、纯化简单、易于操作、稳定性强等优点, 有机三氟硼酸钾的种类丰富, 并且其结构也多种多样, 因此在有机合成上具有极大的应用潜力。 从已有的参考文献来看, 大多数的催化体系需要配体的参与。 在这些催化体系中, 能有效的促进氯代芳烃与有机三氟硼酸钾Suzuki偶联反应的催化体系还较少。 此外, 水是最理想的一种绿色溶剂, 水的存在能够促进有机三氟硼酸钾的Suzuki偶联反应, 因此发展水中能高效促进有机三氟硼酸钾的简单体系也是一个重要的研究内容。 然而, 目前对该试剂在Suzuki偶联反应中的研究却远远不够, 所发展的催化体系也很有限。 在实际研究中, 应注意这类物质在实际合成中的应用, 进一步开发该物质在合成复杂目标分子中的应用潜力。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|